Baterias
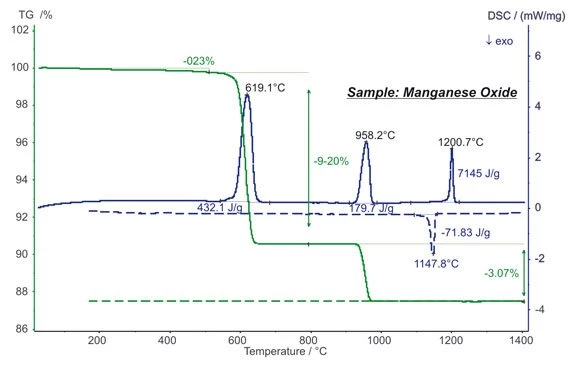
Óxido de Manganês — Redução
Óxido de manganês (MnO2), é frequentemente utilizado em química como oxidante mas também, por exemplo, como um material de catodo em baterias.
A medição STA mostra as etapas de perda de massa em aprox. 600 ° C e 950 ° C, que são devido à redução de MnO2 em Mn2O3 e finalmente em Mn3O4. Os valores de 9,20% e 3,07% correspondem exatamente aos valores estequiométricos refletindo a alta precisão do sistema de balança. Foram detectados, durante as etapas de redução, picos endotérmicos de DSC, com entalpias de 432 J / g, e de 180 J / g,. O pico EndotérmicoA sample transition or a reaction is endothermic if heat is needed for the conversion.endotérmico de DSC à 1200 ° C é devido a uma transformação estrutural reversível, a qual é observada à 1148 ° C, após resfriamento como pico ExotérmicoA sample transition or a reaction is exothermic if heat is generated.exotérmico (linhas tracejadas). (medição com STA 449 F1 Jupiter®®)