Полимеры
Отверждение эпоксидной смолы при частичной диффузии
Скорость химической реакции, в которой участвует более чем один реагкнт, определяется двумя факторами:
1. Скорость диффузии реагентов (характеризуется величиной Kdiff),
2. Скорость химической реакции (характеризуется величиной Kchem).
Эффективную скорость реакции можно рассматривать как среднее геометрическое значение обеих величин: 1/Keff = 1/Kdiff + 1/Kchem ( уравнение Рабиновича). Очевидно, что эффективное значение скорости реакции Keff равно скорости химической реакции Kchem, если скорость диффузии много больше скорости химической реакции Kdiff >> Kchem. Поэтому, в большинстве случаев действие диффузии не учитывается. Если температура реакции близка к температуре стеклования или ниже нее, то наблюдается исльное увеличение вязкости: происходит застекловывание материала. Тогда подвижность веществ становится ограниченной и скорость процесса будет определяться диффузией, т.к. в этом случае скорость химической реакции мого больше чем скорость диффузии Kchem >> Kdiff.
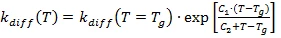
Все вычисления, моделирование и прогнозирование выполнено в программе NETZSCH Kinetics Neo.
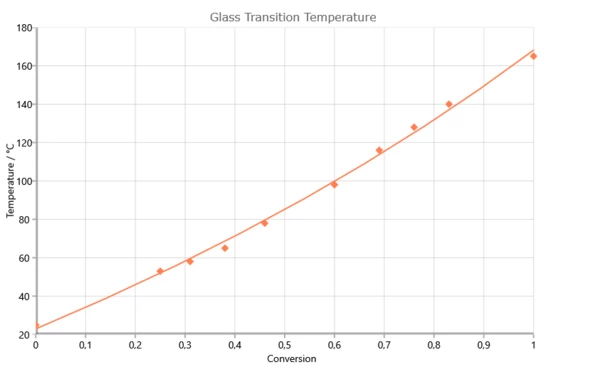
Температурная зависимость скорости химической реакции Kchem вычисляется согласно уравнению Аррениуса. Скорость же диффузии Kdiff обратно пропорциональна вязкости, поэтому используется выражение для зависимости вязкости от температуры. Если (а) кинетический анализ основан на измерениях ДСК, то температура перехода стеклования и ее зависимость от степени превращения используется для вычисления значения вязкости, согласно предложению, сделанному Wise [C.W.Wise, W.D.Cook, A.A.Goodwin: Polymer 38 (1997) 3251]. Здесь скорость диффузии вычислена посредством модифицированного уравнения WilliaМС-Landel-Ferry (WLF)
При температурах T ниже, чем температура стеклования Tg уравнение WLF превращается в уравнение Аррениуса при условиях непрерывности результата и его первой производной. Текущая энергия активации для T<Tg :
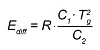
С другой стороны, если (b) кинетический анализ основан на измерениях вязкояти, то вычисленная вязкость используется в качестве контролирующего значения. Теперь вязкость вычисляется через уранение Аррениуса с различными энергиями активации для для неотвержденного и отвержденного материала.
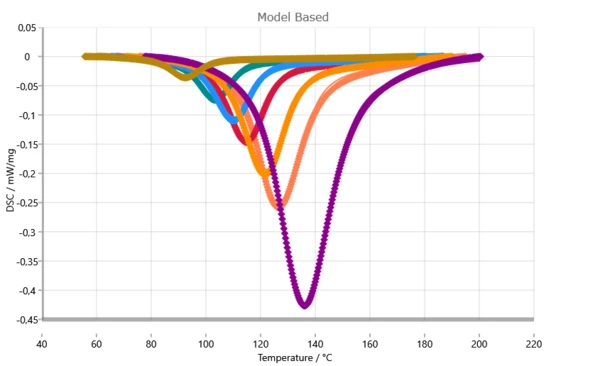
Сравнение между измеренными (точки) и вычисленными (сплошные линии) кривыми ДСК.
Если в кинетичсекой модели принимать во внимание влияние диффузии, то достигается практически идеальное совпадение между измеренными и симулированными данными. Высокое качество совпадения модели с измеренными данными является основным условием для прогнозирования с высоким уровнем доверия к прогнозируемому результату.
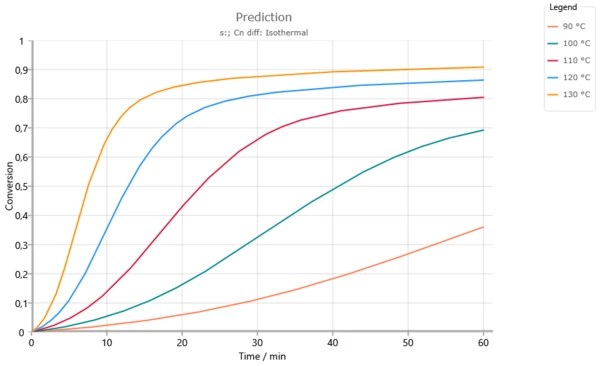
изотермическое прогнозирование при температурах более низких, чем температура стеклования Tg = 165°C. Увеличение степени превращения сильно замедляется при переходе через температуру стеклования, соответствующую текущей степени превращения (см. рис.). При отсутствии диффузии при температурах выше 120°C полная превращение было бы уже достигнуто через 60 мин.
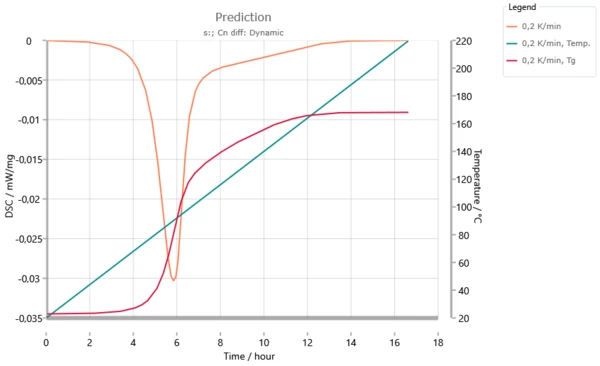
Это становится понятным на следующем графике моделирования для скорости нагрева 0.2 K/мин: температура стеклования достигает температуры реакции через 6 часов. Начиная с этого момента до момента времени 12 часов увеличение температуры стеклования соответствует увеличению температуры реакции. На этом интервале скорость реакции контролируется диффузией.
Динамическое прогнозирование для скорости нагрева of 0.2 K/мин. Температура стеклования достигает температуры реакции через 6 часов. Сигнал ДСК резко падает до постоянного значения. После момента времени 12 часов температура стеклования Tg увеличивается медленнее, чем температура реакции. В системе заканчивается условие для застекловывания.