نصائح وحيل
كيفية تجنب النتائج غير الصحيحة بسبب التحضير غير السليم للعينة
يقيس ميزان قياس الثقل الحراري تغيرات الكتلة في العينة خلال برنامج درجة الحرارة/الزمن (DIN 51005). ونتيجة لذلك، من الممكن تحديد درجات حرارة العمليات الكيميائية والفيزيائية التي تحفز تغير الكتلة.
وتشمل العمليات التبخير، والتسامي، والتحلل الحراري، والتحلل الحراري والتأكسدي، من بين عمليات أخرى.
من المعروف أن منحنى قياس الثقل الحراري يتأثر بالعوامل التالية:
- معدل التسخين
- هندسة العينة
- كتلة العينة
على سبيل المثال، في حالة زيادة معدل التسخين وكتلة العينة، على سبيل المثال، يتم أيضًا تحويل تأثيرات TGA المكتشفة إلى درجات حرارة أعلى. ومع ذلك، من الممكن أيضًا التلاعب بعاملي معدل التسخين وكتلة العينة، من أجل الحصول على أكبر قدر ممكن من المعلومات من منحنى القياس: فصل أفضل للتأثيرات المتداخلة عن طريق تغيير معدل التسخين و/أو كتلة العينة، وتضخيم التأثيرات صغيرة النطاق عن طريق زيادتها، إلخ.
يمكن أن يكون الإعداد غير السليم للعينة سببًا لأكثر من مجرد تحول في خسائر الكتلة التي يرصدها TGA: يمكن أن يؤدي إلى نتائج مختلفة بشكل كبير. باستخدام قياس الثقل الحراري، يمكن قياس العينات الصلبة كمسحوق أو قطعة من قرص؛ ويمكن قياس السوائل أيضًا. ومع ذلك، يجب أن يكون المرء على دراية بأنه لا يمكن الحصول على منحنيات TGA القابلة للتكرار إلا باستخدام نفس تحضير العينة (شكل العينة) وظروف القياس باستمرار. وعلى وجه الخصوص، يؤثر سطح العينة على عمليات معينة، والتي يمكن رؤيتها في تبخر المذيبات أو في التحلل التأكسدي (الاحتراق). ونتيجة لذلك، ترتبط هذه التأثيرات بدرجات حرارة مختلفة اعتمادًا على حالة العينة التي تم فحصها هل هي مسحوق أو مكونة من قطعة واحدة. فيما يلي، تُستخدم قياسات قياس الثقل الحراري لإجراء التحليل الحركي للتفاعل. يوضح هذا المثال مدى أهمية إعداد العينة لاستخلاص الاستنتاجات الصحيحة.
قياسات TGA-FT-الأشعة تحت الحمراء على قرص الإيبوبروفين
أُجريت القياسات على قرص إيبوبروفين Ibu 400 akut، الذي تسوقه شركة 1A Pharma®. يحتوي هذا القرص على الإيبوبروفين كمكون صيدلاني نشط (API)؛ وهو أحد أكثر مضادات الالتهاب غير الستيرويدية (NSAIDs) استخدامًا. وعلاوة على ذلك، فإنه يحتوي أيضًا على سواغات تعمل كمواد مالئة ومواد تشحيم ومواد تفكك، إلخ.
أُجريت القياسات بمعدلات تسخين مختلفة تتراوح بين 5 و20 كلفن/الدقيقة باستخدام مقياس TG 209 F1 نيفيو الحراري في جو نيتروجين ديناميكي. استُخدمت بوتقات أكسيد الألومنيوم. تراوحت كتل العينة من 9.93 مجم إلى 10.09 مجم. تم نقل الغازات المتصاعدة أثناء التسخين مباشرةً إلى خلية الغاز في مطياف FT-IR بواسطة Bruker Optics.
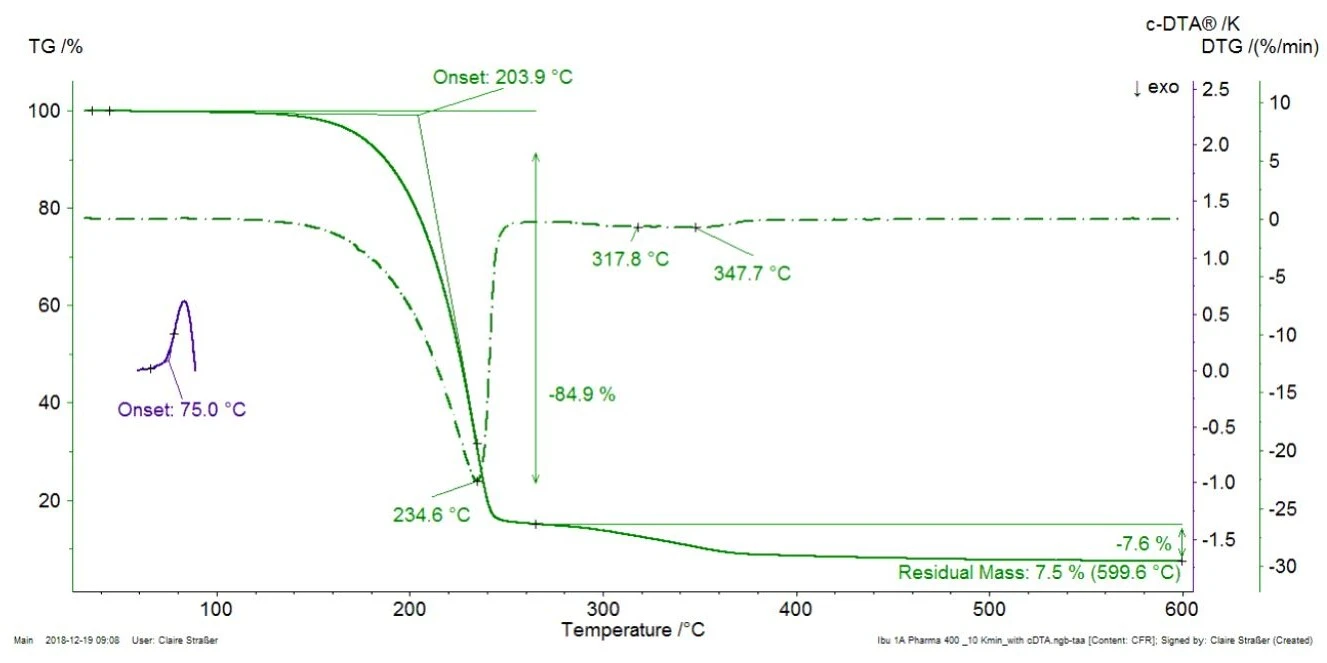
ويعرض الشكل 1 قياس TGA على قرص الإيبوبروفين التجاري بمعدل تسخين 10 كلفن/الدقيقة إلى جانب منحنى DTG (المشتق الأول لمنحنى TGA). وبالإضافة إلى ذلك، يتم عرض إشارة DTA المحسوبة (c-DTA®®، الفرق بين درجة حرارة الفرن ودرجة حرارة العينة) بين 70 درجة مئوية و100 درجة مئوية (المنحنى الأزرق).
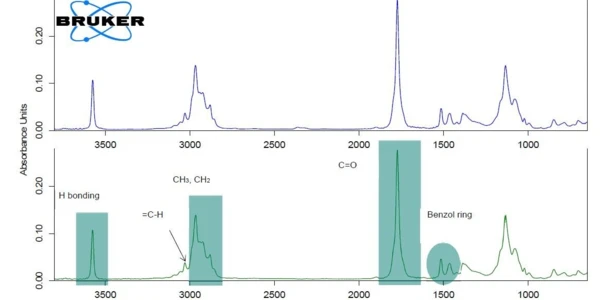
For better readability of the plot, the c-DTA®® signal was only displayed in the temperature range of the ibuprofen melting. لا ترتبط الذروة المكتشفة عند درجة حرارة 75 درجة مئوية (درجة حرارة البداية الاستقرائية) بفقدان الكتلة؛ فهي لا تنتج عن التحلل أو التبخر، الذي من شأنه أن يحدث تغيرات في الكتلة في منحنى TGA، ولكن من ذوبان الإيبوبروفين. تبلغ نسبة فقدان الكتلة الأولى مع درجة حرارة بداية استقرائية تبلغ 204 درجة مئوية 85%. يشير ذلك إلى تحلل أو تبخر أحد المكونات الموجودة في القرص، وعلى الأرجح تبخر المكون النشط، الإيبوبروفين [1]. لأغراض التحقق، تم قياس الإيبوبروفين النقي أيضًا عن طريق TGA-FT-IR (الشكل 2). كانت أطياف الغازات المنبعثة عند درجة حرارة 232 درجة مئوية متشابهة جدًا للمادتين.
وهذا يثبت أن الفقد الكتلي المكتشف عند درجة حرارة 235 درجة مئوية (ذروة DTG، الشكل 1) في Ibu 400 akut ناتج فعليًا عن تبخر المادة الفعالة (الإيبوبروفين) وليس بسبب تحلل أحد السواغات. في الشكل 1، يُظهر Ibu 400 akut خطوتين إضافيتين لفقدان الكتلة بين 250 درجة مئوية و400 درجة مئوية متداخلتين جزئيًا. وربما يرجع ذلك إلى التحلل الحراري للسواغات الموجودة في القرص مثل السليلوز الجريزوفولفيني أو ستيرات المغنيسيوم [2].
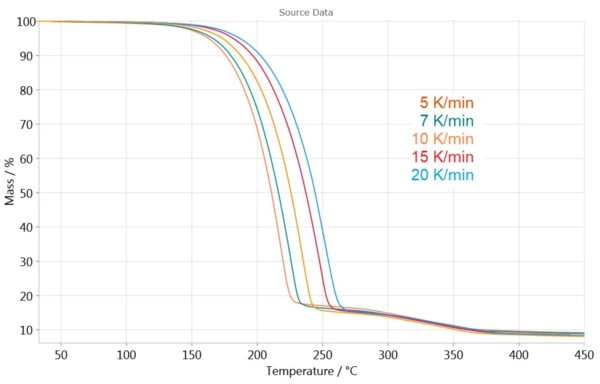
يوضح الشكل 3 قياسات TGA عند معدلات تسخين مختلفة. تنتقل التأثيرات إلى درجات حرارة أعلى مع زيادة معدلات التسخين. يسمح هذا الاعتماد لمنحنى TGA على معدل التسخين بتحديد حركية التفاعل.
تحديد حركية التفاعل عن طريق الحركية الجديدة
تُعد منحنيات TGA التي تم الحصول عليها أساسًا للتقييم الحركي للتفاعلات التي تحدث في نطاق درجة الحرارة المقاسة. ولهذا الغرض، تم استخدام برنامج NETZSCH Kinetics Neo. وهو يسمح بنمذجة حركية التفاعلات أحادية إلى متعددة الخطوات.
يمكن لهذا البرنامج تعيين كل خطوة على حدة لأنواع مختلفة من التفاعلات مع المعلمات الحركية الخاصة بها، مثل طاقة التنشيط وترتيب التفاعل وعامل ما قبل الأسي. واستنادًا إلى النتائج، يستطيع برنامج Kinetics Neo محاكاة التفاعل (التفاعلات) لبرامج درجات الحرارة التي يحددها المستخدم.
للتنفيذ، يتم استيراد منحنيات قياس الثقل الحراري أولاً إلى برنامج Kinetics Neo. بعد ذلك، يتم اختيار نموذج تفاعل لكل خطوة (على سبيل المثال: تفاعل من الدرجة التاسعة ). استنادًا إلى نموذج التفاعل المختار، يحسب البرنامج منحنيات قياس الجاذبية الحرارية. يتم تقييم مدى ملاءمة النموذج من خلال معامل الارتباط بين المنحنيات المقاسة والمحسوبة.
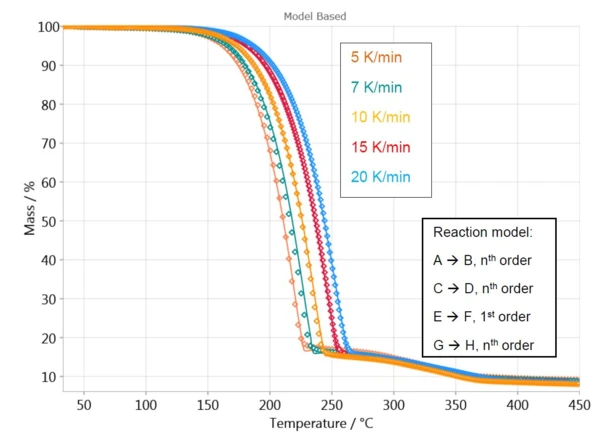
بالنسبة لفقدان الكتلة الأولى، يحسب البرنامج منحنى بنموذج تفاعل من خطوة واحدة، A → B. يوصف سلوك العينة في نطاق درجة الحرارة من 250 درجة مئوية إلى 450 درجة مئوية بثلاث خطوات مستقلة (C → D وE → F وG → H) لأن هذا هو أفضل ما يتناسب مع البيانات المقاسة في نطاق درجة الحرارة هذا.
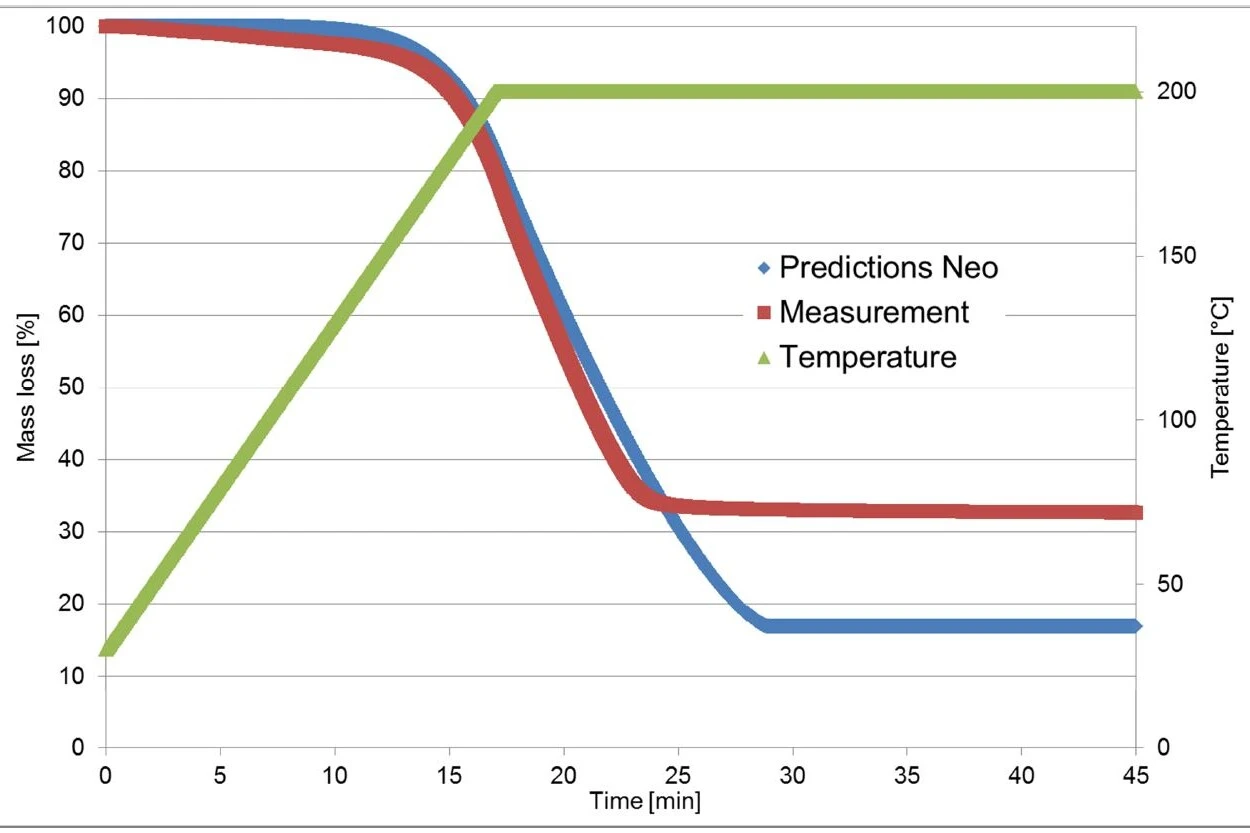
يعرض الشكل 4 مقارنة بين المنحنيات المقاسة والمحسوبة لهذا النموذج. مع معامل ارتباط أعلى من 0.999، يصف النموذج الحركي عملية التفاعل بشكل جيد للغاية.
لكل خطوة من خطوات التفاعل، يحسب Kinetics Neo المعلمات الحركية: طاقة التنشيط، وترتيب التفاعل، ومساهمة الخطوة في العملية الشاملة، إلخ. يعرضها الجدول 1 لجميع الخطوات الأربع.
علامة التبويب. 1. المعلمات الحركية للخطوات الأربع
| التفاعل | أ → ب | ج → د | ه → و | G → H |
| نوع التفاعل | الرتبة التاسعة | الرتبة التاسعة | الرتبةالأولى | الرتبة التاسعة |
| طاقة التنشيط [كيلوجول/مول] | 77.823 | 181.866 | 148.941 | 460.643 |
| لوغاريتم (ما قبل الإكسب) [لوغاريتم (1/ث)] | 6.814 | 14.911 | 10.511 | 38.543 |
| ترتيب التفاعل | 0.286 | 1.332 | 1 | 13.410 |
| المساهمة | 0.912 | 0.022 | 0.034 | 0.033 |
ما سبب الاختلاف الملحوظ؟
تم إجراء قياسات قياس الثقل الحراري المستخدمة للحساب في Kinetics Neo على قطعة من قرص Ibu 400 akut. وعلى النقيض من ذلك، تم إجراء قياس التحقق من الصحة على مسحوق ناتج عن سحق القرص.
كما ذكرنا من قبل، ترجع الخطوة الأولى لفقدان الكتلة إلى تبخر الإيبوبروفين، والذي يعتمد على سطح العينة [1]. يمكن للمرء أن يتوقع أن يكون لسطح العينة الأكبر المرتبط بالمادة المسحوقة تأثير كبير على منحنى TGA.
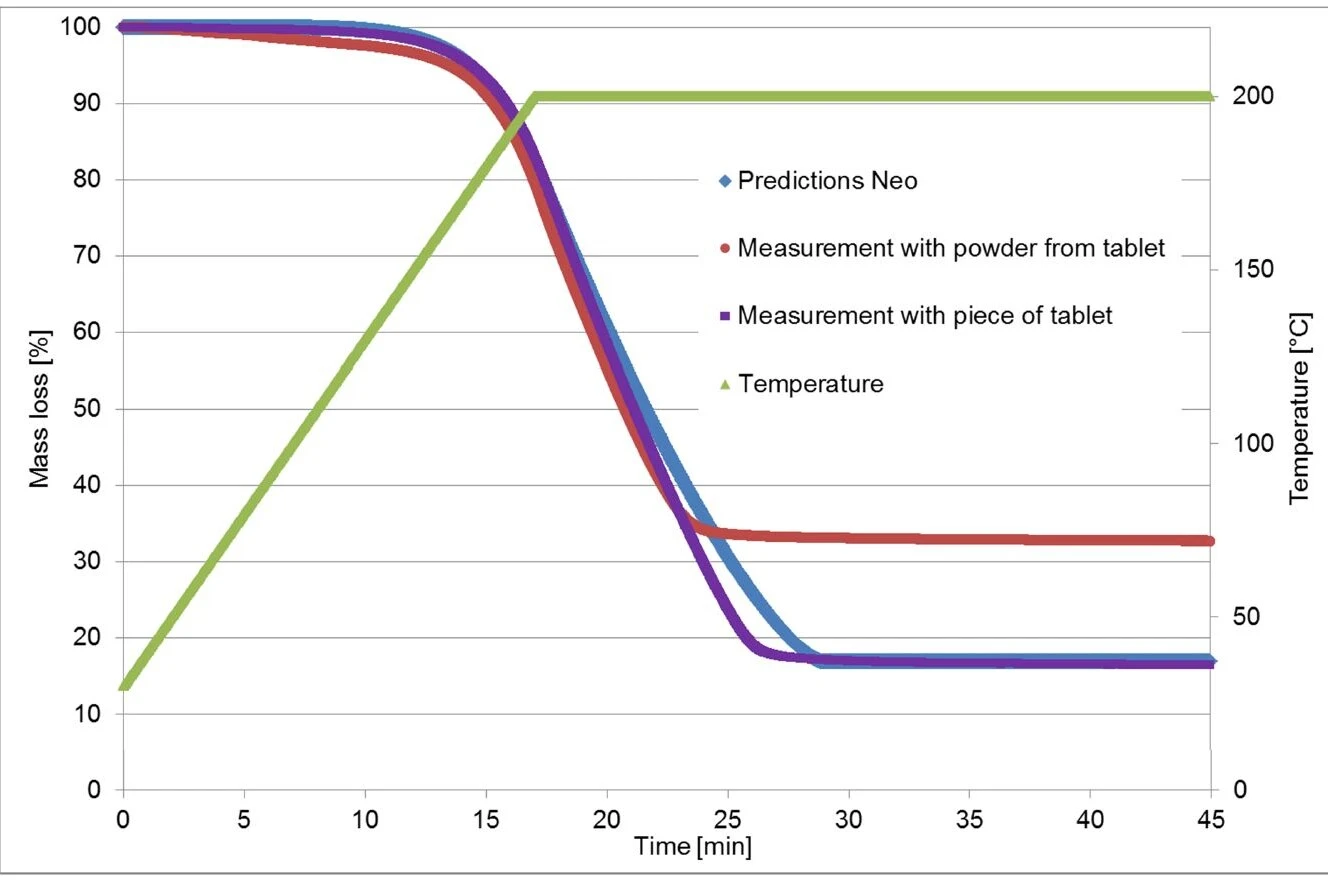
في تجربة ثانية، تم إجراء القياس السابق (التسخين إلى 200 درجة مئوية ومتساوي الحرارة) مرة أخرى، ولكن هذه المرة باستخدام قطعة من القرص. يتوافق منحنى قياس الثقل الحراري الجديد الآن بشكل جيد للغاية مع المنحنى المحسوب بواسطة Kinetics Neo! (انظر الشكل 6.)
الخاتمة
أُجريت قياسات TGA على قرص إيبوبروفين (الاسم التجاري: Ibu 400): قياس على قطعة صلبة وقياس على مسحوق. تمكنت قياسات FT-IR من إثبات أن الخطوة الأولى لفقدان الكتلة تنتج عن تبخر المادة الفعالة. وبالإضافة إلى ذلك، تعتمد هذه العملية اعتمادًا كبيرًا على سطح العينة، وبالتالي فإن نتائج القياسات التي أجريت على قطعة من القرص تختلف عن تلك التي أجريت على المسحوق. وهذا أيضًا له تأثير كبير على التحليل الحركي. يعد هذا التحليل الحركي مفيدًا بشكل خاص عند دراسة الاستقرار الحراري للمستحضرات الصيدلانية.
المراجع
[1] دراسة تحليل حراري للإيبوبروفين، س. ليرد كانشانابورن ود. دوليمور، مجلة التحليل الحراري، المجلد 49 (1997)، العدد 2، ص 879-886
[2] ملاحظة تطبيق NETZSCH 120: دراسات التوافق على ديكلوفيناك الصوديوم - سريع وسهل مع التحليل الحراري؛ الشكلان 5 و9