Введение
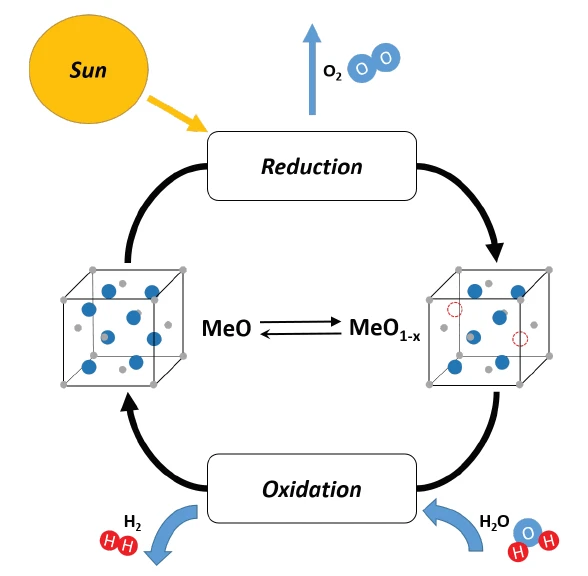
Термохимическое расщепление воды - это процесс производства водорода с использованием высокотемпературного тепла (от 500°C до 2000°C) и ряда химических реакций. Химические вещества, используемые в процессе, повторно используются в каждом цикле, создавая замкнутый цикл, в котором потребляется только вода и производятся водород и кислород. Таким образом, термохимическое производство водорода является экологически чистой альтернативой системам производства водорода на основе ископаемого топлива [1].
Условия измерения
Для исследования термохимического расщепления воды на LSC20 (La0.8Sr0.2CoO3) были проведены термогравиметрические измерения (ТГА) на термоанализаторе NETZSCH STA 449 F3 Jupiter® . Для интерпретации результатов термоанализатор был дополнительно сопряжен с квадрупольным масс-спектрометром NETZSCH QMS Aëolos® Quadro. Подробный перечень условий проведения измерений приведен в таблице 1.
Таблица 1: Параметры измерения
| Параметр | Термохимическое расщепление воды на LSC20 |
|---|---|
| Устройство | STA 449 F3 Jupiter® |
| Аксессуары | Печь для получения водяного пара и генератор пара |
| Носитель образцов | TGA, тип S |
| Крюсиль | Пластина ТГА из Al2O3 диаметром 17 мм |
| Вес образца | 215.46 мг порошкообразного образца) |
| Программа измерений | От RT до 1200°C, 15 K/мин, 4% H2 в аргоне 90 минут изотермы при 1200°C, 4% H2 в аргоне 1200°C - 600°C, 15 К/мин, 4% H2 в аргоне 30 мин изотерма @ 600°C, аргон 60 мин изотерма @ 600°C, 33% H2Oв аргоне 30 мин изотерма @ 600 °C, аргон |
Результаты и обсуждение
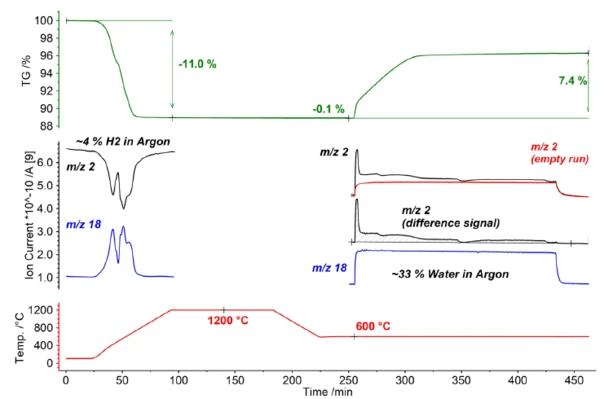
На первом этапе исследования LSC20 был активирован с помощью восстановительной атмосферы (4% H2 в аргоне). При этом материал образца демонстрирует выраженную потерю массы -11,0 %. Кроме того, расход водорода (масса 2) с одновременным выделением воды (масса 18) можно четко наблюдать с помощью масс-спектрометра с одновременной связью (см. синюю и черную кривые на рис. 2).
Собственно термохимическое расщепление воды происходит во второй части исследования. Для этого образец охлаждался до 600 °C, а затем подвергался воздействию газовой атмосферы, содержащей воду (33 % H2Oв аргоне). Это привело к окислительному увеличению массы на 7,4 % с одновременным выделением водорода (см. массу № 2 на рис. 2). По резким изменениям кривой массы, а также кривой тока масс-спектрометра Ionic видно, что расщепление воды является многоступенчатым процессом; это предполагает прямую поверхностную реакцию в качестве начального этапа реакции, а также диффузионно-контролируемую реакцию в дальнейшем.
Резюме
Концепция платформы NETZSCH STA 449 F3 Jupiter® обеспечивает отличную основу для воспроизведения сложных тепловых процессов и явлений. В представленном примере целевое исследование термохимической реакции расщепления воды было успешно воспроизведено с помощью специально разработанной печи для водяного пара и парогенератора.
В данном примере были не только точно измерены изменения веса (гравиметрическая регистрация), но и проанализированы и интерпретированы процессы, происходящие в ходе реакции. Для этого использовалась масс-спектрометрия с сопряжением для исследования газов, выделяющихся в ходе реакции.
Сочетание этих приборов - STA, печи для получения водяного пара, парогенератора и масс-спектрометра со связью - создает идеальную установку для всесторонней характеристики протекающих реакций, участвующих в термохимическом расщеплении воды.