مقدمة
تتشكل الهيدروكربونات العطرية متعددة الحلقات (PAHs) أثناء العمليات الطبيعية والبشرية المنشأ مثل الانفجارات البركانية أو حرائق الغابات أو تكرير النفط أو إنتاج الصلب. ونتيجةً لذلك، يتم إطلاقها في الغلاف الجوي، وبسبب كرهها للماء، فإنها تتراكم في التربة وبالتالي قد تدخل السلسلة الغذائية. وقد أظهرت تجارب مختلفة أن الهيدروكربونات العطرية العديدة الحلقات هي مواد مطفرة ومسرطنة قوية [1]. يمكن بسهولة رصد عملية الامتزاز الحراري لإزالة تلوث الهيدروكربونات العطرية العطرية العديدة الحلقات من التربة عن طريق التحليل الحراري [2]. يوثق الجمع بين DSC وقياس الجاذبية الحرارية الذوبان وفقدان الكتلة كمؤشر على تبخر المواد المتطايرة. وفي هذا العمل، تم إجراء التحليل الحراري المتزامن باستخدام أجهزة STA 449 Jupiter® من أجل الحصول على درجات الذوبان والغليان وكذلك ضغط البخار لثلاثة مركبات نموذجية من الهيدروكربونات العطرية العطرية المتعددة الحلقات وهي النفثالين والأنثراسين والبنزو (أ) بيرين.
تم شراء هذه المركبات العطرية من شركة ألفا أيسار بنقاوة عالية (النفثالين 99.6%، والأنثراسين 99%، والبنزو (أ) بيرين 96%).
نقاط الانصهار والغليان
استُخدِم جهاز التحليل الحراري المتزامن من طراز NETZSCH STA 449 F3 Jupiter®Jupiter®، المزود بحامل عينة TG-DSC من النوع S، لتحديد درجات الانصهار والغليان. تم استخدام بوتقات ألومنيوم محكمة الغلق ذات ثقب يبلغ 50 ميكرومتر لهذه القياسات. استند القياس الحراري لأداة STA إلى معايرة بمعايير ذوبان الإنديوم والألومنيوم والذهب، وتم التحقق من دقة قياس الحرارة باستخدام الزنك في حدود 1 كلفن. استُخدم النيتروجين كغاز تطهير بمعدل تدفق 70 مل/دقيقة وتم التسخين حتى 600 درجة مئوية بمعدل تسخين ثابت قدره 10 كلفن/دقيقة. كانت كتلة العينة 20 مجم تقريبًا.
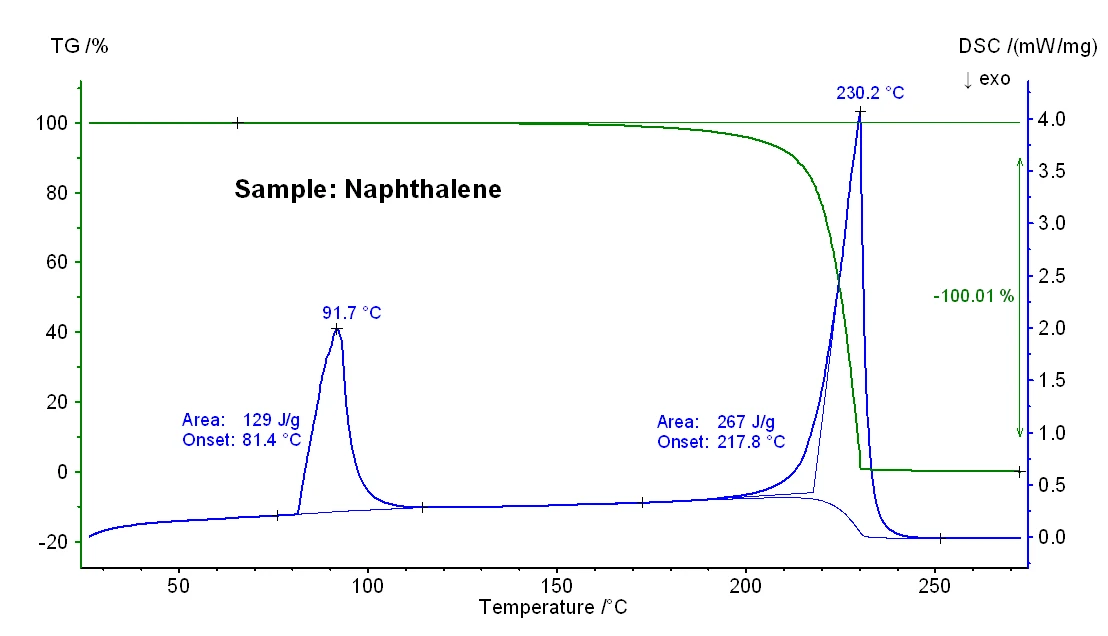
يوضح الشكل 1 التغيرات الكتلية المعتمدة على درجة الحرارة وإشارة DSC لعينة النفثالين. عند درجة حرارة بداية استقرائية تبلغ 81 درجة مئوية، تم اكتشاف تأثير ماص للحرارة في التذبذب الحراري الدوراني الكهرومغناطيسي مع إنثالبي 129 جول/غرام، وهو ما يرجع إلى الذوبان. تتوافق درجة حرارة البداية الاستقرائية مع درجة حرارة الانصهار، وعند درجة حرارة الذروة البالغة 92 درجة مئوية تكون العينة منصهرة بالكامل. حدثت خطوة فقدان للكتلة بنسبة 100% بين حوالي 150 درجة مئوية و230 درجة مئوية وهو ما يعكس تبخر العينة. وكان هذا التأثير مصحوبًا بذروة ماصة للحرارة في التذبذب الحراري الحراري المانع للحرارة مع إنثالبي 267 جول/غرام ودرجة حرارة بداية استقرائية تبلغ 218 درجة مئوية. ويعكس هذا الأخير درجة غليان العينة.
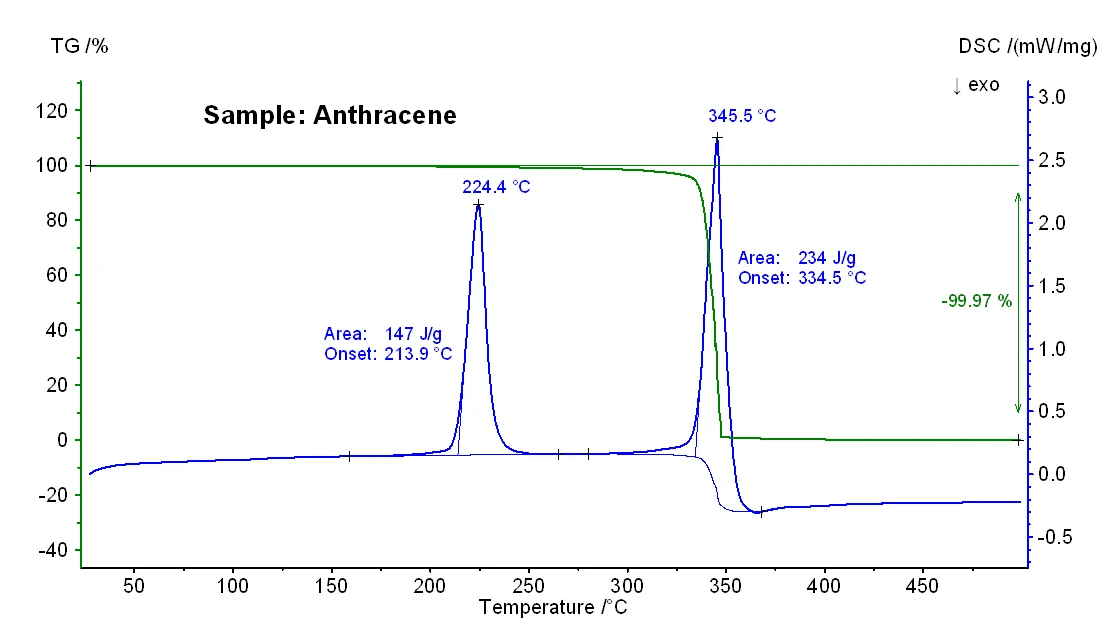
وتظهر نتائج TG-DSC التي تم الحصول عليها لعينات الأنثراسين والبنزو (أ) بيرين في الشكلين 2 و3، ويمكن رؤية درجات الحرارة الهامة للذوبان والغليان في الجدول 1 أدناه. وبوجه عام، من المعروف أن درجات حرارة الغليان التي يتم الحصول عليها من قياس DSC قد تعتمد بشكل خاص على معدل التسخين، وكتلة العينة الأولية وأيضًا على تحضير العينة [3].
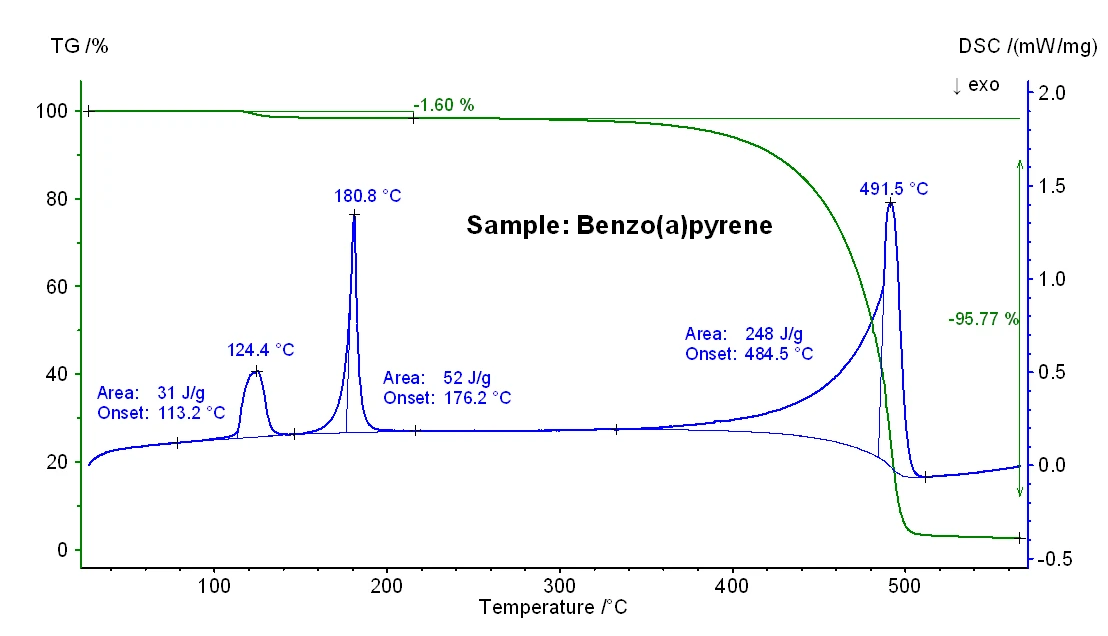
وعلاوة على ذلك، تجدر الإشارة إلى أنه لوحظت خطوة فقدان كتلة إضافية بنسبة 1.6٪ بالإضافة إلى تأثير ماص للحرارة مع إنثالبي 31 جول/غرام لعينة البنزو (أ) بيرين (انظر الشكل 3) والذي يرجع على الأرجح إلى إطلاق الرطوبة. تتوافق هذه النتيجة مع النقاء الاسمي الأقل لهذه العينة (انظر المقدمة).
الجدول 1: مقارنة بين درجات الحرارة الاسمية (بين قوسين، مقدمة من المورد ألفا أيزار) ودرجات حرارة الانصهار والغليان المقاسة
| نفتالين | الأنثرازين | بنزو(أ) بيرين | |
|---|---|---|---|
| درجة حرارة الذوبان | 81°C (80 درجة مئوية - 82 درجة مئوية) | 214°C (214 درجة مئوية - 218 درجة مئوية) | 176°C (177 درجة مئوية - 180 درجة مئوية) |
| درجة حرارة الغليان | 218°C (218°C) | 335°C (340 درجة مئوية - 342 درجة مئوية) | 484°C (495°C) |
ضغط البخار
تم تحقيق تحديد ضغط البخار باستخدام جهاز التحليل الحراري المتزامن STA 449 F1 Jupiter®. وبدلاً من البوتقة القياسية، تم تركيب خلية Knudsen على حامل عينة TG مع مزدوج حراري من النوع S (انظر الشكل 4).
يمكن الحصول على ضغط البخار وفقًا لطريقة انصباب Knudsen [4]. تصف هذه الطريقة تبخر مادة العينة من خلال ثقب محدد لخلية كنودسن في تفريغ عالي. لذلك تم تفريغ جهاز STA بشكل دائم أثناء القياس باستخدام مضخة جزيئية توربينية تصل إلى حوالي 10-5 ملي بار خارج خلية كنودسن. يكون الضغط داخل خلية كنودسن مساويًا لضغط بخار العينة.
تتدفق مادة العينة المتبخرة عبر فتحة خلية Knudsen مما يؤدي إلى معدل فقدان الكتلة Δm/Δt وهي كمية القياس. يمكن حساب ضغط البخار وفقًا للمعادلة الأدبية:
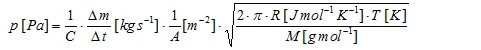
والتي يمكن تحويلها بعد ذلك إلى
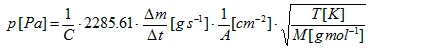
حيث C هو ما يسمى بعامل تصحيح Clausing [4]. يمكن تقريب هذا المعامل الذي يعتمد على النسبة بين نصف القطر r وعمق الثقب l للثقوب الأسطوانية:
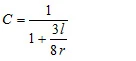
A هي مساحة الثقب، وR هي ثابت الغاز العام، وT هي درجة الحرارة، وM هي الكتلة المولية للعينة [4]. إن طريقة انصباب كنودسن محدودة بشكل عام بقياس معدل فقدان الكتلة المحدود ولكن أيضًا بسبب الفراغ العالي الإجباري خارج خلية كنودسن. قد يؤدي معدل فقدان الكتلة المرتفع للغاية إلى انهيار الفراغ.
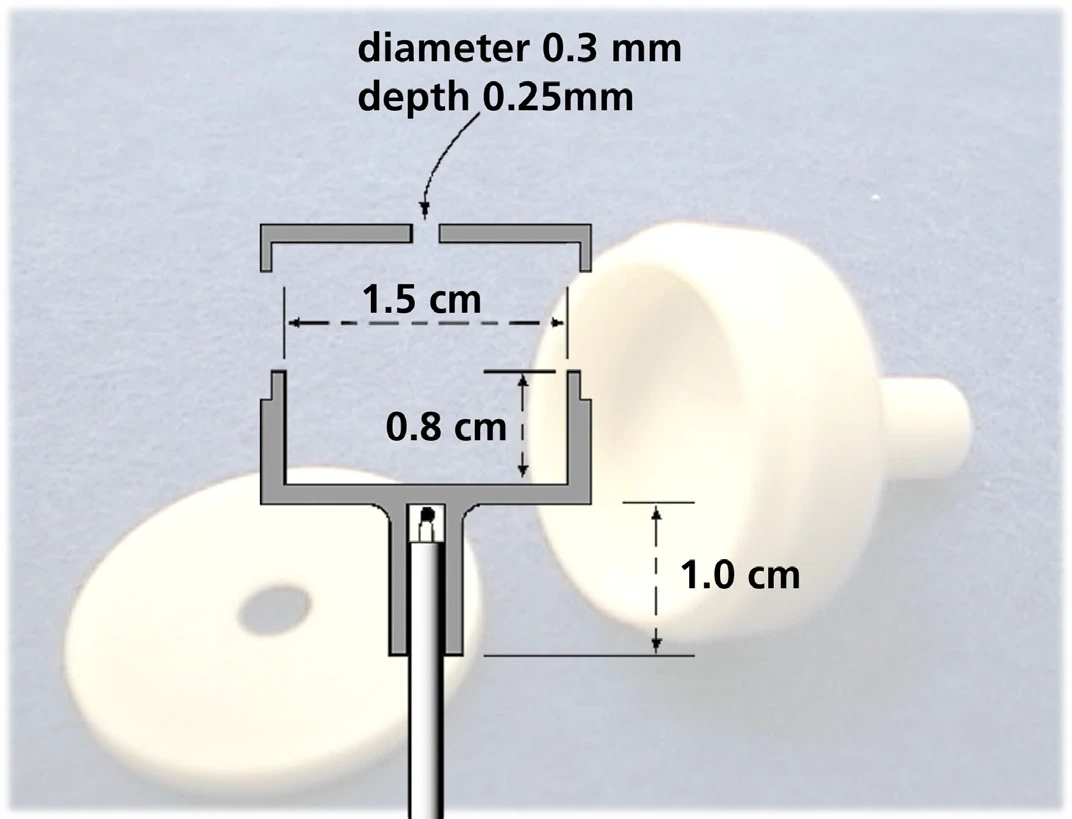
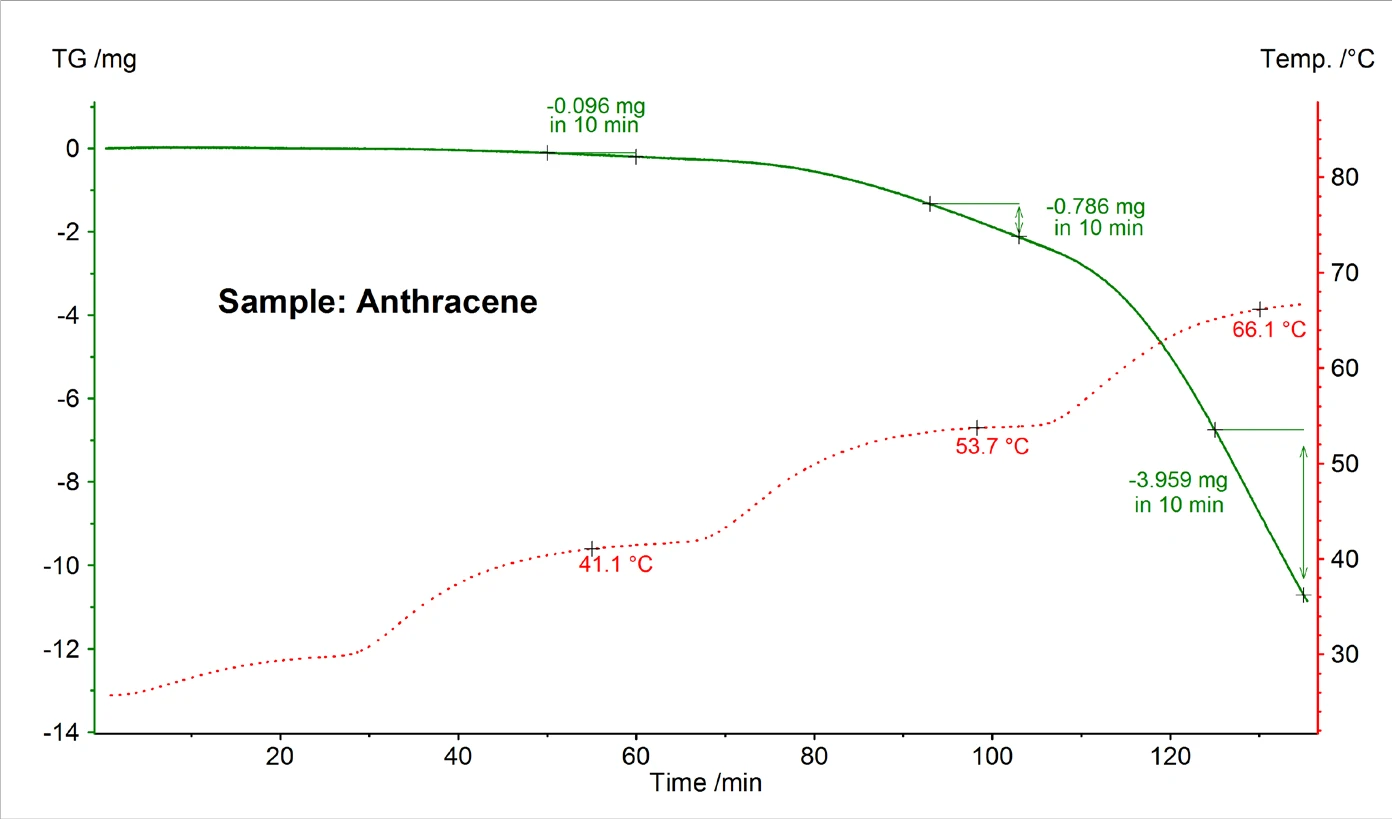
ويوضح الشكل 5 نتيجة قياس نموذجي للغازات الجزيئية للأنثراسين الذي تم إجراؤه في تفريغ عالي باستخدام خلية Knudsen بقطر ثقب 0.285 سم. من معدل فقدان الكتلة المكتشفة عند درجات حرارة ثابتة مختلفة، تم حساب ضغط البخار باستخدام الصيغتين (2) و(3).
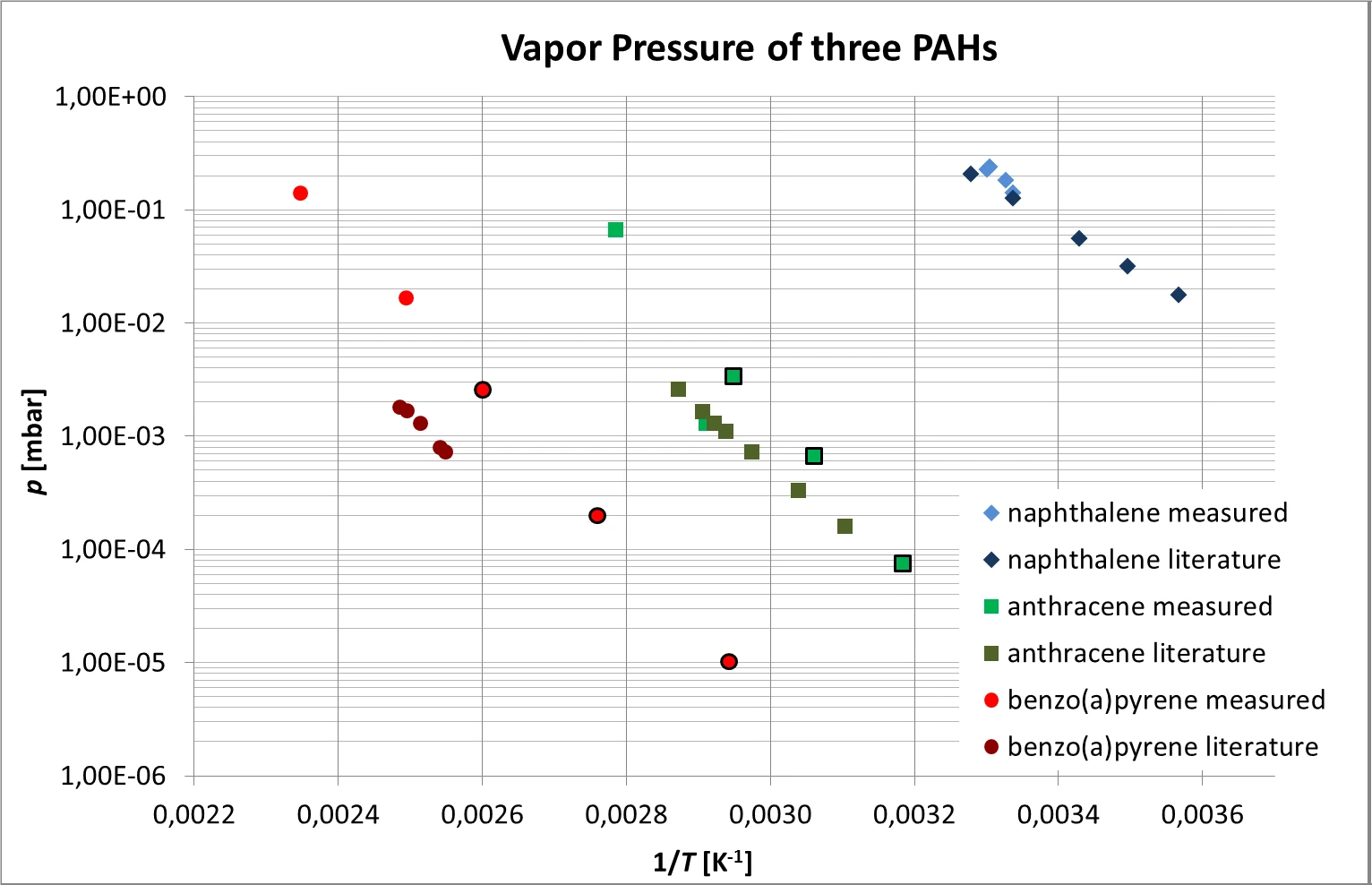
يمكن رؤية النتائج المجمعة التي تم الحصول عليها للأنثراسين والنفتالين والبنزو (أ) بيرين التي تتبع الاعتماد الأسي المتوقع لدرجات الحرارة في الشكل 6. نظرًا لضغط البخار المرتفع نسبيًا، لا يمكن قياس تبخر النفثالين إلا بالقرب من درجة حرارة الغرفة.
كما تظهر المقارنة مع القيم الأدبية [4، 5] في الشكل 6. تم العثور على تباين كبير نسبيًا بين القيم المقاسة والقيم الأدبية بحوالي رتبة واحدة من حيث الحجم في حالة البنزو (أ) بيرين.
الملخص
أمكن تحديد درجات الذوبان والغليان للأنثراسين والنفتالين والبنزو (أ) بيرين عن طريق التحليل الحراري المتزامن. وعلاوة على ذلك، تم تحديد قيم ضغط البخار من خلال تطبيق طريقة انصباب كنودسن. كانت جميع النتائج التي تم الحصول عليها باستخدام أجهزة STA 449 Jupiter® متقاربة بشكل جيد مع القيم الاسمية والأدبية.