مقدمة
في مجال الصيدلة، لا يكاد يوجد أي عنصر نشط كُتب عنه أكثر مما كُتب عن حمض أسيتيل الساليسيليك (أو ASA اختصارًا؛ وفي البلدان الناطقة بالإنجليزية والألمانية، غالبًا ما يُستخدم الاسم التجاري Aspirin™ كمرادف له). وقد بدأت قصة نجاحه في نهاية القرن التاسع عشر عندما قام الدكتور فيليكس هوفمان بتصنيع هذه المادة في مختبرات باير لأول مرة بدون شوائب. في الوقت الحاضر، لا يزال أحد أكثر المستحضرات الصيدلانية شيوعًا، ويستخدم في نطاق علاجي واسع. وهو ينتمي إلى مجموعة العقاقير غير الستيرويدية المضادة للالتهابات (NSAIDs) ويستخدم لعلاج الألم والحمى والالتهابات. بالإضافة إلى ذلك، يُستخدم للوقاية من تكرار النوبة القلبية أو السكتة الدماغية لدى المرضى المعرضين لخطر الإصابة. في عام 1977، تمت إضافة ASA كمسكن إلى "قائمة الأدوية الأساسية" لمنظمة الصحة العالمية (منظمة الصحة العالمية). [1]
هذه هي المذكرة الأخيرة من أربع مذكرات تطبيقية تدرس بمزيد من التفصيل السلوك الحراري لحمض أسيتيل الساليسيليك؛ حيث تناولت المذكرات الثلاث الأولى التحلل في أجواء غازية مختلفة، وحركية التحلل، وأنواع الغازات الناتجة [2، 3، 4].
تجريبي
وللتحقق من التحلل الحراري لحمض أسيتيل الساليسيليك، أُجريت قياسات قياس الثقل الحراري (TGA) باستخدام جهاز NETZSCH TG 209 Libra® تحت جو من الهيليوم. وللتفسير الداعم، اقترن المحلل الحراري بالإضافة إلى ذلك بمطياف الكتلة الرباعي الأقطاب 403 Aëolos® رباعي الأقطاب. شروط القياس الدقيقة مفصلة في الجدول 1.
الجدول 1: معلمة القياس
| المعلمة | حمض أسيتيل الساليسيليك |
|---|---|
| المحلل | TG 209 Libra® مع QMS 403 Aëolos® |
| حامل العينة | TGA، النوع S |
| بوتقة | Al2O3، 85 ميكرولتر، مفتوح |
| كتلة العينة | 8.35 مجم |
| برنامج درجة الحرارة | من RT إلى 500 درجة مئوية، معدل التسخين 10 كلفن/دقيقة |
| الغلاف الجوي | هيليوم* (100 مل/دقيقة) |
*في هذا العمل، كان جو الهيليوم في هذا العمل متوافقًا مع القياسات المدرجة في الملاحظات التطبيقية السابقة 208 و209 و210 (الجزء 1 إلى 3).
نتائج القياس والمناقشة
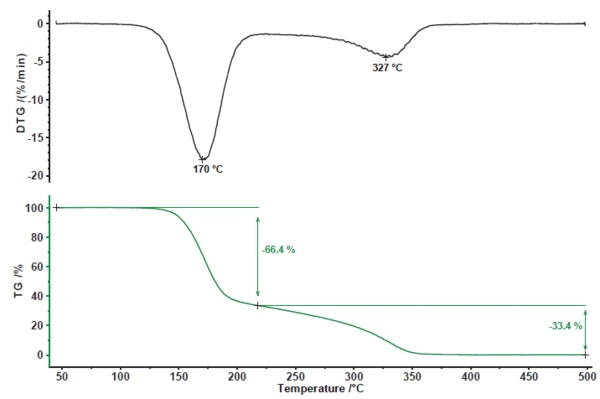
يُظهر الانحلال الحراري لحمض أسيتيل الساليسيليك خطوتين لفقدان الكتلة (الشكل 1). ترتبط خطوة فقدان الكتلة الأولى بنسبة 66.4% بذروة في معدل فقدان الكتلة (DTG) عند 170 درجة مئوية. وتبلغ خطوة فقدان الكتلة الثانية 33.4% مع ذروة في منحنى معدل فقدان الكتلة عند 327 درجة مئوية.
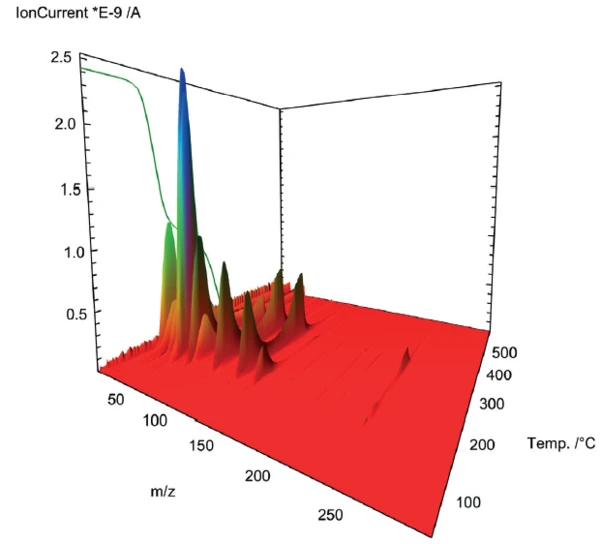
يُظهر اقتران مطياف الكتلة المستخدم لاكتساب نظرة أعمق في التحلل الحراري لحمض أسيتيل الساليسيليك صورة معقدة للغازات الخارجة في خطوتي فقدان الكتلة (الشكل 2). ومن أجل الفحص الدقيق، تم استخراج أطياف الكتلة للخطوات المعنية وإخضاعها لمقارنة قاعدة البيانات مع "NIST MS Library".
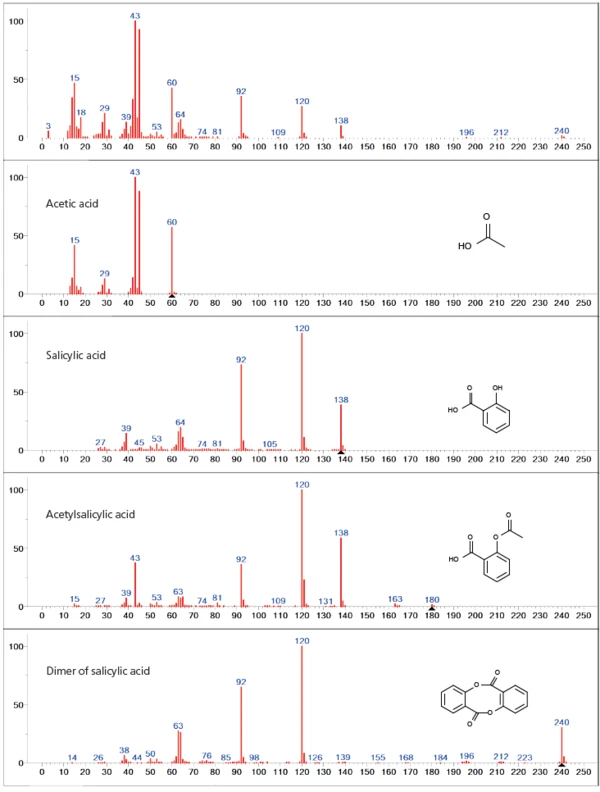
يُظهر تحليل قاعدة البيانات لخطوة فقدان الكتلة الأولى بشكل أساسي إطلاقًا متداخلًا لحمض الأسيتيل وحمض الساليسيليك، مما يشير إلى تحلل وظيفة الأسيتيل لحمض الأسيتيل الساليسيليك (الشكل 3). وبالإضافة إلى الناتجين الرئيسيين للغازات الخارجة، توجد أيضًا أعداد كتلية أعلى (> 138 ش) في الطيف، والتي يمكن أن تُعزى إلى ثنائي حمض الساليسيليك. وبالإضافة إلى ذلك، لا يمكن استبعاد التبخر الجزئي لحمض أسيتيل الساليسيليك غير المتحلل ضمن خطوة فقدان الكتلة الأولى كاحتمال لأن جميع الكتل الرئيسية لطيف حمض أسيتيل الساليسيليك (43، 60، 92، 120، 138 ش) متداخلة مع نواتج التحلل المذكورة سابقًا.
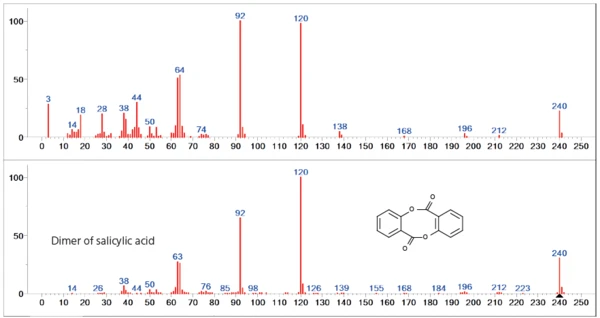
يهيمن على خطوة فقدان الكتلة الثانية بشكل أساسي إطلاق ثنائي حمض الساليسيليك. ومع ذلك، يمكن رؤية اختلافات في طيف قاعدة البيانات خاصةً في نطاق الكتلة الأدنى (<60u)، مما يشير إلى إطلاق أنواع غازية إضافية (الشكل 4).
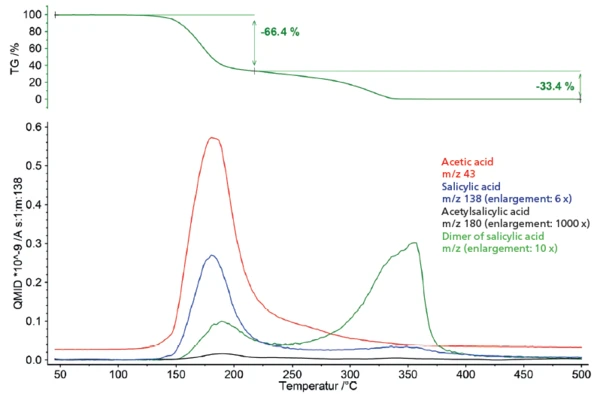
وبسبب نواتج الغازات الخارجة المكتشفة، يمكن تجميع عرض يعتمد على درجة الحرارة لسلوك الغازات الخارجة. ولتحقيق هذه الغاية، تم تحديد الأعداد الكتلية المحددة لنواتج الغازات المنفردة selectورسمها بالمقارنة مع منحنى فقدان الكتلة (الشكل 5). ويوضح العرض المقابل تداخل التحلل الحراري لحمض أسيتيل الساليسيليك وتبخر حمض الساليسيليك المتكون كمنتج تحلل ضمن خطوة فقدان الكتلة الأولى. ويتضح أيضًا أن تكوين وتبخر القلة القليلة من حمض الساليسيليك يبدأ بالفعل في نفس نطاق درجة الحرارة وهو عملية التحلل المهيمنة في مسار درجة الحرارة التالية.
الملخص
ويُعد الجمع بين قياس الثقل الحراري وقياس الطيف الكتلي أداة قوية للحصول على نظرة عميقة في عمليات التحلل الحراري والغازات المنبعثة. يتيح الاقتران بمطياف الكتلة الحصول على نظرة عامة على نواتج الغازات المنبعثة المعتمدة على درجة الحرارة والتي تتسم بجودة عالية مماثلة لطريقة الجمع بين قياس الجاذبية الحرارية والتحليل الطيفي بالأشعة تحت الحمراء. ومع ذلك، نظرًا للطابع الأكثر تحديدًا لأطياف الكتلة، يسمح الاقتران بمقياس الطيف الكتلي باستخلاص استنتاجات أكثر دقة فيما يتعلق بأنواع الغازات المنبعثة.
وباختصار، يحدث التحلل الحراري لحمض أسيتيل الساليسيليك في جو الهيليوم في عملية من خطوتين تتألف من فصل وظيفة الأسيتيل وما يرتبط بها من إطلاق حمض الأسيتيك إلى جانب تبخر حمض الساليسيليك في شكل قليل الأسيتيل (على سبيل المثال، ثنائي الميكر). وأثبتت النظرة التحليلية الغازية لخطوات فقدان الكتلة ذات الصلة تداخلًا جزئيًا بين العمليتين بسبب الإطلاق المتزامن لحمض الأسيتيك وحمض الساليسيليك في وقت واحد ضمن خطوة فقدان الكتلة الأولى.
يشير التحليل التفصيلي لأطياف MS التي تم الحصول عليها إلى أنه لا يمكن الوصول إلى جميع نواتج الغازات الخارجة عن طريق الاقتران المباشر ل TGA بمقياس الطيف الكتلي. وهكذا، خاصةً في خطوة الفقد الثانية، كان من الممكن فقط تعيين أجزاء من الأعداد الكتلية المرصودة بوضوح. ومع ذلك، يتميز الجمع بين كروماتوغرافيا الغاز وقياس الطيف الكتلي (GC-MS)، كما هو موضح بالفعل في الجزء 3 من سلسلة الملاحظات التطبيقية هذه، بمنهجية اقتران أكثر تخصصًا، والتي تم تطويرها خصيصًا لهذا النوع من المهام [4].