Introdução
Desde sua descoberta em 1965 pelo químico James L. Schlatter, os cientistas discutem sobre esse adoçante polêmico. Ele é permitido corretamente em bebidas e outros produtos dietéticos ou é um perigo para a nossa saúde?
Aqui, ele foi medido por meio de DSC e TGA-FT-IR a fim de obter informações sobre algumas de suas propriedades térmicas, como Temperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica).ponto de fusão e temperatura de degradação.
Resultados do teste
Para a medição de DSC, uma amostra foi preparada em um cadinho Concavus® com tampa perfurada e aquecida entre a temperatura ambiente e 300°C a uma taxa de aquecimento de 10 K/min. Os resultados do aquecimento são apresentados na figura 2.
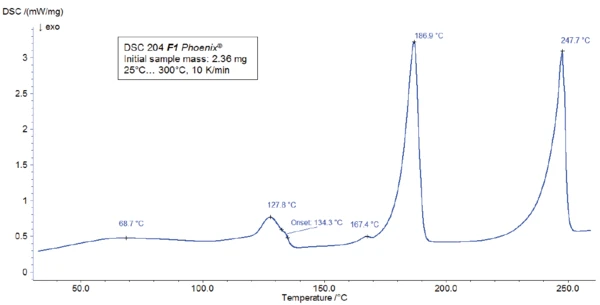
A medição TGA-FT-IR foi realizada em uma amostra de 7,46 mg preparada em um cadinho de óxido de alumínio e aquecida a 700°C a 10 K/min em uma atmosfera dinâmica de nitrogênio. Os gases que evoluíram durante a medição de TGA foram injetados diretamente no espectrômetro FT-IR da Bruker Optics. A curva de TGA é mostrada na figura 3. Um amplo efeito EndotérmicoUma transição de amostra ou uma reação é endotérmica se for necessário calor para a conversão.endotérmico entre 25°C e 100°C (figura 3) está associado a uma perda de massa de 1,4%. Um segundo efeito EndotérmicoUma transição de amostra ou uma reação é endotérmica se for necessário calor para a conversão.endotérmico detectado a 128°C (temperatura de pico) leva a uma perda de massa de 1,5%. Os espectros FT-IR correspondentes a 60°C e 123°C (veja a figura 4) revelam que a substância liberada é água em ambos os casos (provavelmente água absorvida na primeira etapa e água de hidratação na segunda etapa).
O pico detectado a 187°C (DSC), correspondente à etapa de TGA com uma perda de massa de 12,5%, é devido à degradação do aspartame. O espectro FT-IR detectado a 184°C é apresentado na Figura 5 (curva azul). Ele corresponde muito bem ao espectro do PNNL library para metanol (curva vermelha).
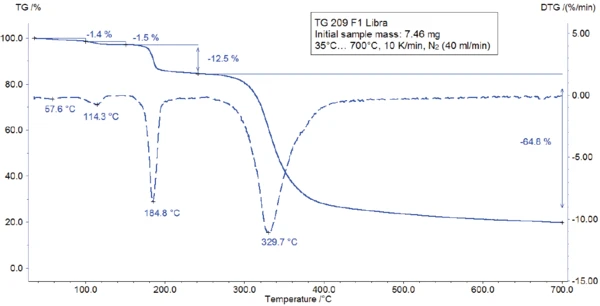
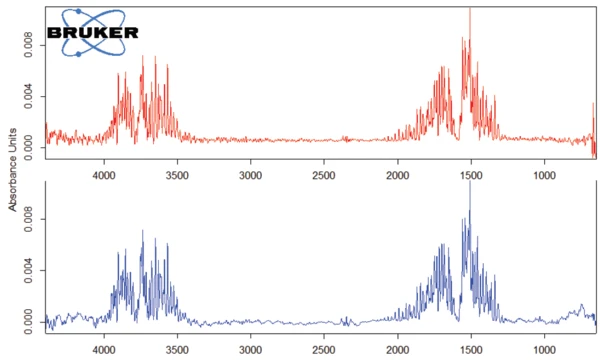
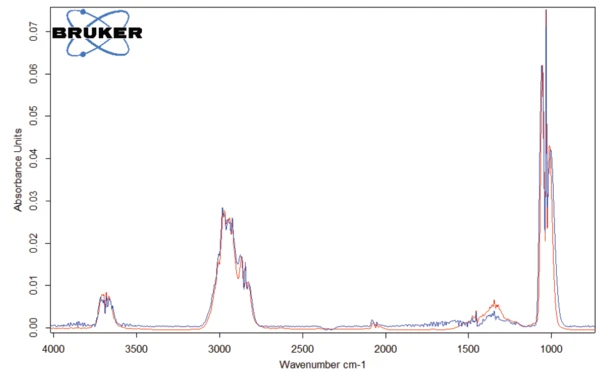
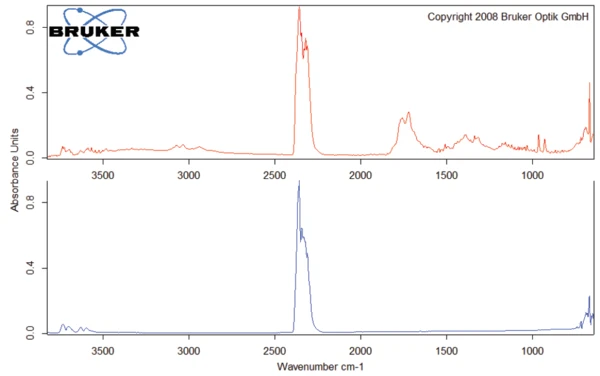
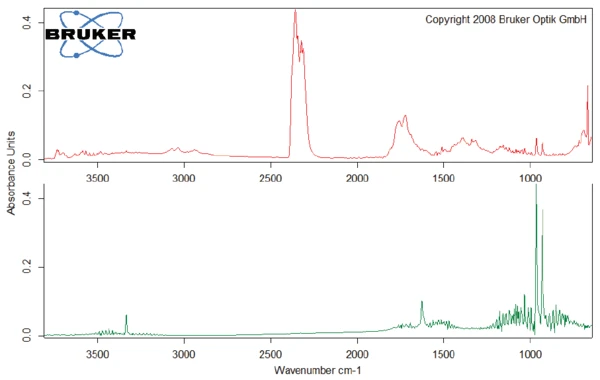
Essa degradação térmica do aspartame, associada à liberação de metanol, leva à formação de uma nova substância, presumivelmente a 2,5-dioxopiperazina [2]. O pico a 248°C na curva DSC pode ser atribuído à Temperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica). fusão da substância formada. Segue-se a degradação desse produto (pico de TGA a 330°C - fig. 3). As Figuras 6, 7 e 8 mostram o espectro FT-IR dos produtos liberados a 329°C (curva vermelha) em comparação com os espectros FT-IR de diferentes compostos, sugeridos pelo banco de dados NIST-EPA. Durante a degradação, o dióxido de carbono e a amônia são liberados (espectro azul na figura 6; espectro verde na figura 7). As outras bandas detectadas são provavelmente causadas por grupos funcionais contendo ligações aromáticas, nitrogênio e oxigênio.
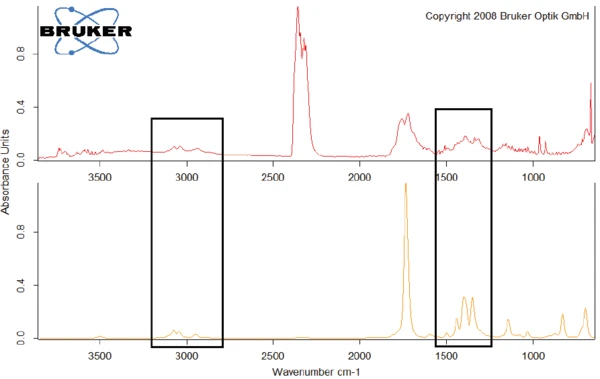
Como exemplo, a figura 8 compara o espectro FT-IR a 329,1 °C com o espectro de N-benzil-maleimida, com o qual mostra conformidade nas faixas de comprimento de onda em torno de 3000 cm-1 e entre 1250 cm-1 e 1500 cm-1.
Conclusão
A análise com os métodos complementares de DSC e TGA revela a quantidade de componentes voláteis em uma amostra, juntamente com suas temperaturas de Temperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica). fusão e degradação. Além disso, o acoplamento FT-IR fornece informações sobre as substâncias liberadas durante o aquecimento: No caso do aspartame, a água evapora primeiro e, depois, a substância se degrada com a liberação de metanol.
Embora causada por outro tipo de mecanismo, a degradação do aspartame no corpo após seu consumo também leva à liberação de metanol, entre outras emissões. Isso pode causar dor de cabeça e tontura [3], se a substância for ingerida em grandes quantidades. Essa é uma das razões para a recomendação de consumir aspartame apenas com cautela.