Termos e origem
O chocolate já era conhecido pela humanidade desde os astecas, mas na forma de uma bebida que continha cacau. O termo "chocolate" é derivado da palavra asteca Xocolatl , que significa água amarga ou água de cacau. A bebida era feita com as sementes da planta do cacau e água fria e era considerada inebriante. No mundo asteca, ela era reservada para homens adultos de ascendência nobre e não era considerada adequada para mulheres e crianças. O rei asteca, Montezuma, teria bebido large quantidades de cacau. Durante seu reinado, as sementes de cacau também eram usadas como moeda.
Em 1528, os conquistadores espanhóis da época de Hernán Cortés levaram o cacau para a Europa; a bebida foi degustada pela primeira vez na corte espanhola em 1544. Em 1673, o holandês Jantz von Huesden serviu chocolate ao público pela primeira vez em Bremen. No entanto, foi somente nos séculos XVIII e XIX que as sementes de cacau foram tratadas em largequantidades. Como eram muito caros, somente a nobreza rica podia comprá-los.
Em 1804, A. Miehte fundou a Halloren Chocolate Factory, a mais antiga fábrica de chocolate da Alemanha, na cidade de Halle an der Saale.
A primeira fábrica de chocolate suíça foi fundada por François-Louis Cailler em 1819, em Vevey, seguida por Philippe Suchard (1824), Jean Tobler (1830), Rudolf Sprüngli (1845) e Daniel Peter e Henri Nestlé (1875). O processo de conchagem, que largemuito contribuiu para a excelente reputação do chocolate suíço, remonta a Rudolphe Lindt.
Nibs de cacau, massa de cacau, manteiga de cacau e cacau em pó
O nome botânico do cacaueiro, Theobroma cacao, é derivado do grego (theos: "Deus"; broma: "alimento"). Esse nome expressa o grande apreço por essa planta. O Theobroma cacao é uma planta cauliflorosa e, portanto, desenvolve suas flores e, posteriormente, seus frutos no tronco já lignificado (figura 1).

Os frutos amarelos de 15 a 20 cm de comprimento pesam aproximadamente meio quilo e contêm de 30 a 60 sementes brancas. Após a colheita, elas são separadas, fermentadas e secas. Durante a fermentação, que leva aproximadamente 10 dias, muitas substâncias amargas são decompostas e as sementes de cacau desenvolvem seu sabor e cor característicos.

A Figura 2 mostra os grãos fermentados e sem casca. Normalmente, é nesse estado que os grãos são enviados para outros países, onde são transformados em chocolate. A massa de cacau, que é importante para a produção de chocolate, é obtida quando as amêndoas são quebradas e transformadas em pó de cacau e manteiga de cacau.
A massa de cacau é, na verdade, o termo para os nibs de cacau que permanecem depois que os grãos são secos e as partes da casca são removidas. Quando esses nibs são moídos, a gordura contida neles - a manteiga de cacau - flui para fora e une os nibs em uma massa viscosa e marrom-escura. Quando essa massa de cacau é prensada, a manteiga de cacau se desprende e o bolo prensado pode ser moído e transformado em cacau em pó. Dependendo do teor de gordura residual, esse pó é designado como fortemente desengordurado (aprox. 11% a 12% de gordura) ou levemente desengordurado (aprox. 20% a 22% de gordura).
Ingredientes e efeitos
Além do teor relativamente alto de gordura (54% de manteiga de cacau), o cacau também contém algumas substâncias conhecidas por terem um efeito de melhora do humor. São elas a serotonina, a dopamina e a teobromina (3,7-dimetil xantina, C7H8N4O2), uma substância da classe das metilxantinas muito semelhante à cafeína. Embora apenas small concentrações desses ingredientes estejam contidas no cacau, eles devem ser a razão por trás do conceito comum de que "o chocolate faz você feliz". Os aspectos de saúde do consumo de cacau ainda não foram determinados de forma conclusiva e ainda são objeto de pesquisa atualarch. Entretanto, os efeitos de promoção da saúde foram confirmados em vários estudos separados, especialmente para o chocolate com alto teor de cacau (> 50%). Esses efeitos positivos incluem a redução de depósitos nos vasos sanguíneos, a diminuição da pressão arterial e dos níveis de colesterol LDL e a melhora da funcionalidade da pele e do desempenho físico geral.
A Figura 3 mostra uma variedade de barras de chocolate com diferentes níveis de teor de cacau.

Polimorfismo da manteiga de cacau
Quimicamente, a manteiga de cacau é composta principalmente de triglicerídeos de diferentes ácidos graxos, principalmente ácido palmítico, ácido esteárico, ácido oleico e ácido linoleico. Devido ao PolimorfismoPolimorfismo é a capacidade de um material sólido de formar diferentes estruturas cristalinas (sinônimos: formas, modificações).polimorfismo acentuado da manteiga de cacau, sabe-se que ela tem seis estruturas cristalinas que derretem na faixa de temperatura entre 17°C e 36°C. Para a produção de chocolate, é particularmente importante que o polimorfo V - a chamada "modificação ß" - seja formado durante a solidificação da massa líquida de chocolate. Isso é obtido por meio de um tratamento térmico especial chamado "temperagem". Durante a têmpera, a massa de chocolate é submetida a um resfriamento definido e, em seguida, é reaquecida para derreter novamente os cristais indesejáveis de baixo Temperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica).ponto de fusão. É difícil encontrar a temperatura correta aqui, pois a formação de núcleos de CristalizaçãoA cristalização é o processo físico de endurecimento durante a formação e o crescimento de cristais. Durante esse processo, o calor da cristalização é liberado.cristalização na manteiga de cacau ocorre muito lentamente, ou seja, o processo de CristalizaçãoA cristalização é o processo físico de endurecimento durante a formação e o crescimento de cristais. Durante esse processo, o calor da cristalização é liberado.cristalização é muito lento e a massa de chocolate pode ser resfriada em excesso antes que a CristalizaçãoA cristalização é o processo físico de endurecimento durante a formação e o crescimento de cristais. Durante esse processo, o calor da cristalização é liberado.cristalização se torne perceptível. No entanto, nos casos de aquecimento em que as formas de cristais de baixo Temperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica).ponto de fusão já se liquefizeram, mas quantidades suficientes de cristais de alto Temperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica).ponto de fusão - que são a modificação ß mais estável em termos termodinâmicos - ainda permanecem, elas acabam servindo como núcleos de CristalizaçãoA cristalização é o processo físico de endurecimento durante a formação e o crescimento de cristais. Durante esse processo, o calor da cristalização é liberado.cristalização para o resfriamento subsequente. Portanto, durante o resfriamento, é quase exclusivamente a modificação ß desejada que é formada.
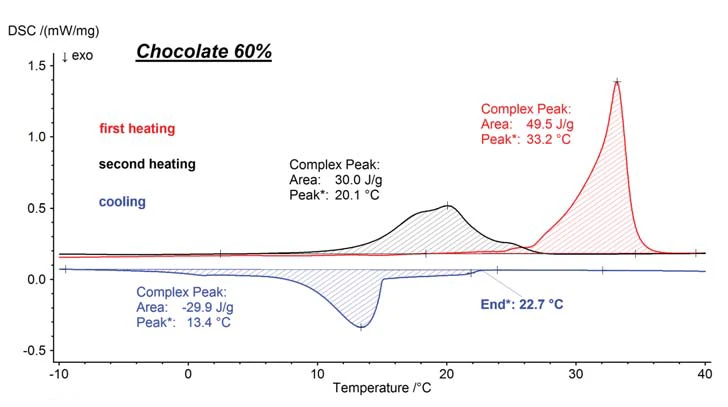
Esse processo pode ser facilmente reproduzido e analisado por meio da Calorimetria Exploratória Diferencial (DSC). O comportamento de derretimento de um determinado chocolate (com 60% de teor de cacau) é apresentado na figura 4. Para a modificação ß que é visada durante a produção do chocolate, a Temperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica). fusão começa lentamente em torno de 25°C e atinge seu pico máximo no primeiro aquecimento (vermelho) a 33,2°C. Durante o resfriamento (azul), o início da CristalizaçãoA cristalização é o processo físico de endurecimento durante a formação e o crescimento de cristais. Durante esse processo, o calor da cristalização é liberado.cristalização a 22,7°C pode ser detectado como um conjunto final extrapolado.
No entanto, parte da massa fundida pode ser resfriada em excesso a 15°C antes que essas porções comecem a cristalizar. Em uma taxa de resfriamento de 5 K/min, essa amostra leva até aproximadamente -5°C para finalizar a CristalizaçãoA cristalização é o processo físico de endurecimento durante a formação e o crescimento de cristais. Durante esse processo, o calor da cristalização é liberado. cristalização. Já pode ser visto na forma de pico da curva de resfriamento que, em contraste com a situação anterior de produção industrial, ocorreram várias modificações na manteiga de cacau que derretem em temperaturas mais baixas como resultado do resfriamento no instrumento DSC. Isso também é confirmado pelos resultados do segundo aquecimento (preto).
As modificações formadas no instrumento DSC durante o resfriamento começam a derreter já a pouco mais de 10 °C, o que é mostrado pelo calor EndotérmicoUma transição de amostra ou uma reação é endotérmica se for necessário calor para a conversão.endotérmico da reação. O derretimento já está concluído a 28 °C, uma temperatura na qual o chocolate original mal começou a derreter durante o primeiro aquecimento. Outra descoberta importante é fornecida pela integral das áreas de Temperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica). fusão e CristalizaçãoA cristalização é o processo físico de endurecimento durante a formação e o crescimento de cristais. Durante esse processo, o calor da cristalização é liberado. cristalização. Elas são proporcionais aos valores de calor latente e, portanto, são uma medida do Cristalinidade / Grau de cristalinidadeA cristalinidade refere-se ao grau de ordem estrutural de um sólido. Em um cristal, o arranjo de átomos ou moléculas é consistente e repetitivo. Muitos materiais, como vidro, cerâmica e alguns polímeros, podem ser preparados de forma a produzir uma mistura de regiões cristalinas e amorfas. grau de cristalinidade da amostra. Embora as partes cristalinas da amostra em seu estado original tenham levado a uma entalpia de Temperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica). fusão de 49,5 J/g (primeiro aquecimento, curva vermelha), foi detectada uma entalpia de Temperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica). fusão de apenas 30,0 J/g (curva preta).
Isso corresponde ao Cristalinidade / Grau de cristalinidadeA cristalinidade refere-se ao grau de ordem estrutural de um sólido. Em um cristal, o arranjo de átomos ou moléculas é consistente e repetitivo. Muitos materiais, como vidro, cerâmica e alguns polímeros, podem ser preparados de forma a produzir uma mistura de regiões cristalinas e amorfas. grau de cristalinidade que foi obtido durante a curva de resfriamento (compare a curva de resfriamento, azul). Isso significa não apenas que, durante o resfriamento no DSC a uma taxa linear de 5 K/min, ocorreram diferentes modificações de baixo Temperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica).ponto de fusão em comparação com as circunstâncias originais de produção do chocolate, mas também que o Cristalinidade / Grau de cristalinidadeA cristalinidade refere-se ao grau de ordem estrutural de um sólido. Em um cristal, o arranjo de átomos ou moléculas é consistente e repetitivo. Muitos materiais, como vidro, cerâmica e alguns polímeros, podem ser preparados de forma a produzir uma mistura de regiões cristalinas e amorfas. grau de cristalinidade diminuiu sensivelmente. Isso, por sua vez, confirma que, conforme mencionado acima, é necessário um tratamento especial de temperatura para a geração direcionada de uma proporção de large modificação ß de alto Temperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica).ponto de fusão.
Variação do grau de cristalização do chocolate por meio da têmpera
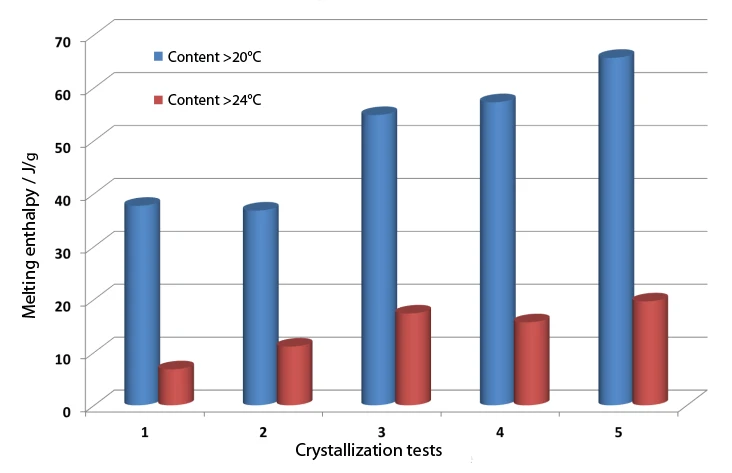
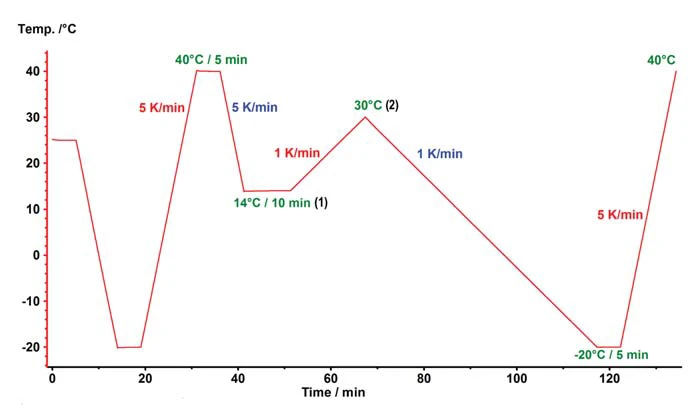
Na produção industrial de chocolate, a massa de chocolate líquido é submetida a um tratamento mecânico e térmico para obter especificamente a modificação ß de alto derretimento desejada e para suprimir a CristalizaçãoA cristalização é o processo físico de endurecimento durante a formação e o crescimento de cristais. Durante esse processo, o calor da cristalização é liberado. cristalização da manteiga de cacau. A simulação de tal tratamento pode ser parcialmente realizada no instrumento DSC, mas, compreensivelmente, sem o componente mecânico. A Figura 5 mostra a alteração nas porções da área do pico de Temperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica). fusão acima de 20 °C e acima de 24 °C para uma série de testes de têmpera. O teste de cristalização 1 descreve os resultados quando é usada uma taxa de resfriamento linear de 5 K/min. Os testes 2 a 5 variam a temperatura de envelhecimento (1) e a temperatura na qual os núcleos de cristalização do PolimorfismoPolimorfismo é a capacidade de um material sólido de formar diferentes estruturas cristalinas (sinônimos: formas, modificações).polimorfismo indesejado são novamente fundidos (2). O teste de cristalização 5 mostra um claro aumento na Cristalinidade / Grau de cristalinidadeA cristalinidade refere-se ao grau de ordem estrutural de um sólido. Em um cristal, o arranjo de átomos ou moléculas é consistente e repetitivo. Muitos materiais, como vidro, cerâmica e alguns polímeros, podem ser preparados de forma a produzir uma mistura de regiões cristalinas e amorfas. cristalinidade em comparação com o resfriamento linear. Isso foi obtido temperando a amostra por 10 minutos a 14° e, em seguida, aquecendo-a a 30°C. O programa de temperatura correspondente é apresentado na figura 6.
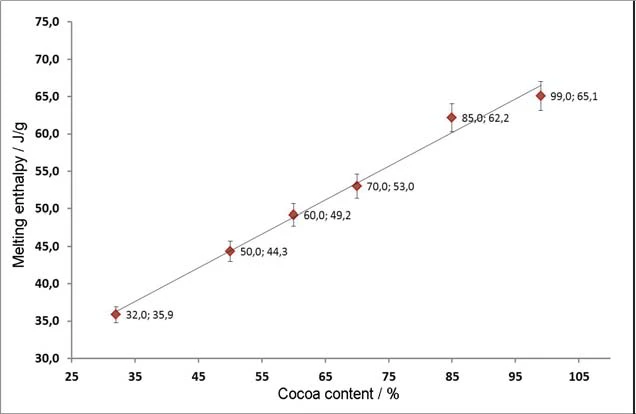
Relação entre o teor de cacau e o derretimento Entalpia
Ao investigar chocolates com vários níveis de teor de cacau, pode-se observar que a relação entre eles é largely linear. À medida que o teor de cacau aumenta, a quantidade de manteiga de cacau cristalina também aumenta e, portanto, também aumenta a quantidade de energia necessária para a fusão. A entalpia de fusão pode ser determinada diretamente a partir da área do pico do primeiro aquecimento. Aplicando o teor nominal de cacau e a entalpia de fusão detectada, obtém-se uma relação linear, que é mostrada na Figura 7. Os valores listados são os valores médios de cinco medições cada. As barras de erro mostradas não representam os erros reais de medição, mas apenas ilustram que essa relação linear se aplica com uma correlação de + 3%.
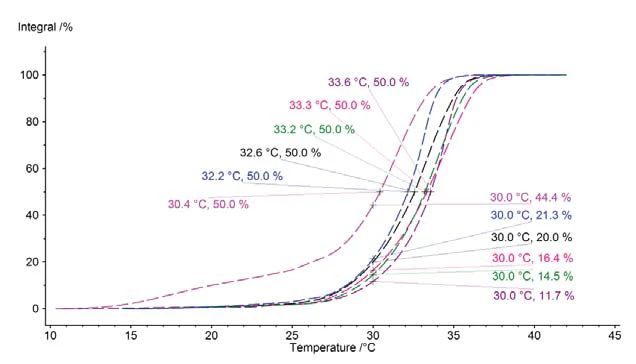
Como a área do pico de fusão ajuda não apenas a quantificar o comportamento de fusão de diferentes amostras de chocolate, mas também - usando a posição e a forma do pico - a determinar a faixa de temperatura e o processo de fusão, é possível especificar, para cada amostra individualmente, quanto da gordura (manteiga de cacau) contida ainda está sólida na temperatura correspondente e quanto já está líquida. Essa informação também é conhecida como Índice de Gordura Sólida (SFI). É fácil chegar a essa afirmação se a área do pico for dimensionada para 100% e o curso for representado como uma integral de superfície. Essa aplicação é mostrada para todas as amostras de chocolate investigadas na Figura 8. Em primeiro lugar, pode-se ver claramente a que temperatura exatamente metade do conteúdo de gordura correspondente ainda está sólido; e, em segundo lugar, pode-se deduzir facilmente que parte da gordura contida já está derretida em uma determinada temperatura (aqui 30°C).
A literatura contém muitos exemplos que destacam as informações oferecidas pelos resultados das medições de DSC, além dos mostrados aqui, para a investigação do comportamento de fusão e cristalização do chocolate. Cammenga et al. descrevem o uso da Calorimetria Exploratória Diferencial para doces em geral. O açúcar e seus substitutos geralmente constituem a maior parte desses produtos em massa, e as propriedades mensuráveis, como a temperatura de transição vítrea, a Cristalinidade / Grau de cristalinidadeA cristalinidade refere-se ao grau de ordem estrutural de um sólido. Em um cristal, o arranjo de átomos ou moléculas é consistente e repetitivo. Muitos materiais, como vidro, cerâmica e alguns polímeros, podem ser preparados de forma a produzir uma mistura de regiões cristalinas e amorfas. cristalinidade, a Temperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica). temperatura de fusão e as entalpias de transformação de fase - para citar apenas algumas - têm grande influência nas propriedades físico-químicas e tecnológicas, bem como na estabilidade do armazenamento [1].
Em uma série de trabalhos, Ziegleder et al. descrevem a estabilidade de longo prazo [2] e a formação de bloom de gordura no chocolate [3].
Chapman et al. [4] e Merken et al. [5] concentraram-se no PolimorfismoPolimorfismo é a capacidade de um material sólido de formar diferentes estruturas cristalinas (sinônimos: formas, modificações).polimorfismo e na processabilidade do chocolate em seus trabalhos, enquanto Tscheuschner et al. [6] e Ziegleder et al. [7] realizaram várias investigações sobre as condições de resfriamento e a cristalização do chocolate e da massa de chocolate.
Resumo
A manteiga de cacau se cristaliza em seis estruturas diferentes (PolimorfismoPolimorfismo é a capacidade de um material sólido de formar diferentes estruturas cristalinas (sinônimos: formas, modificações).polimorfismo), das quais uma - a chamada modificação ß - é a preferida para a produção de chocolate. Para obter esse resultado, é necessário um procedimento especial de tratamento de temperatura chamado "temperagem". Com a ajuda da DSC (Calorimetria Exploratória Diferencial), é possível não apenas determinar a Temperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica). temperatura de fusão da manteiga de cacau, o que fornece informações sobre as modificações que ocorrem durante a produção, mas também determinar a entalpia de transformação (entalpia de fusão), o que permite a quantificação das porções cristalinas da manteiga de cacau. Ao investigar vários chocolates com teor de cacau entre 32% e 99%, foi possível confirmar que há uma relação largelinear entre o teor de cacau especificado e a entalpia de fusão, conforme determinado por meio de DSC. Além disso, foi demonstrado que também é possível investigar a influência da têmpera sobre a quantidade e a diferenciação das modificações cristalinas individuais da manteiga de cacau. A taxa de resfriamento em conexão com as fases isotérmicas e qualquer reaquecimento subsequente de curto prazo da massa de chocolate têm influência sobre o Cristalinidade / Grau de cristalinidadeA cristalinidade refere-se ao grau de ordem estrutural de um sólido. Em um cristal, o arranjo de átomos ou moléculas é consistente e repetitivo. Muitos materiais, como vidro, cerâmica e alguns polímeros, podem ser preparados de forma a produzir uma mistura de regiões cristalinas e amorfas. grau de cristalinidade resultante. Portanto, é possível recriar a têmpera da massa de chocolate que ocorre na produção em uma análise DSC por meio da variação do controle de temperatura. Além do controle flexível da temperatura dos programas de medição em uma análise de DSC, as informações contidas nos resultados de DSC oferecem várias outras possibilidades de proteção para a produção de chocolate em áreas como inspeção de entrada de mercadorias, controle de produção e controle de qualidade.