Begriffe und Herkunft
Bereits die Azteken kannten Schokolade, verstanden darunter allerdings ein kakaohaltiges Getränk. Der Begriff Schokolade leitet sich wohl vom aztekischen Xocolatl ab, was so viel wie bitteres Wasser oder Kakaowasser bedeutete. Das Getränk wurde aus den Samen der Kakaopflanze und kaltem Wasser zubereitet und galt als berauschend. Nach dem Verständnis der Azteken war es erwachsenen, dem Adel entstammenden Männern vorbehalten und für Frauen und Kinder ungeeignet. Der Aztekenkönig Montezuma soll große Mengen an Kakao zu sich genommen haben. Unter ihm galten die Kakaobohnen auch als Zahlungsmittel.
1528 brachten die spanischen Eroberer um Hernán Cortés Kakao nach Europa mit, 1544 wurde das Getränk erstmals am spanischen Hofe getrunken. In Bremen schenkte 1673 der Holländer Jan Jantz von Huesden erstmals öffentlich Schokolade aus. Größere Mengen an Kakaobohnen wurden in Bremen aber erst im 18. und 19. Jahrhundert gehandelt. Sie waren sehr teuer, daher konnten sich Schokolade nur die reichen Adeligen leisten.
1804 gründete A. Miehte in Halle an der Saale die Halloren Schokoladenfabrik, die älteste Schokoladenfabrik in Deutschland.
Auf die erste schweizer Schokoladenfabrik, von François-Louis Cailler 1819 in Vevey gegründet, folgten Philippe Suchard (1824), Jean Tobler (1830), Rudolf Sprüngli (1845) sowie Daniel Peter und Henri Nestlé (1875). Auf Rodolphe Lindt geht das Conchierverfahren zurück, das wesentlich zum Ruf der Schweizer Schokolade betrug.
Kakaobruch, Kakaomasse, Kakaobutter und Kakaopulver
Der botanische Name des Kakaobaums Theobroma cacao leitet sich aus dem Griechischen ab (theos: „Gott“; broma: „Speise“). Durch diese Namensgebung kommt die außerordentliche Wertschätzung dieser Pflanze zum Ausdruck. Theobroma cacao gehört zu den kaulifloren Pflanzen, die die Blüten sowie die später daraus entstehenden Früchte am bereits verholzten Stamm tragen (Abbildung 1).

Die 15 bis 20 cm langen gelben Früchte sind etwa ein halbes Kilogramm schwer und enthalten 30 bis 60 weiße Samenbohnen. Diese werden bei der Ernte herausgelöst, fermentiert und getrocknet. Während der etwa zehn Tage dauernden Fermentation werden viele Bitterstoffe abgebaut und die Kakaobohnen entwickeln ihren typischen Geschmack und die Farbe.

Abbildung 2 zeigt fermentierte ungeschälte Kakaobohnen. Üblicherweise werden die Bohnen in diesem Zustand in die Länder verschifft, in denen sie zu Schokoloade verarbeitet werden. Durch Brechen der Bohnen werden die für die Schokoladenherstellung wichtige Kakaomasse und daraus das Kakaopulver sowie die Kakaobutter hergestellt.
Als Kakaomasse bezeichnet man den Kakaobruch, der nach Trocknen der Bohnen und Abtrennen der Schalenteile verbleibt. Wird dieser Kakaobruch gemahlen, tritt das enthaltene Fett, die Kakaobutter aus und bindet die Bruchstücke zu einer zähflüssigen dunkelbraunen Kakaomasse. Wird die Kakaomasse gepresst, fließt die Kakaobutter ab und der Presskuchen kann zu Kakaopulver zermahlen werden. Je nach verbleibendem Fettgehalt bezeichnet man dieses Pulver als stark entölt (ca. 11 bis 12 % Fett) oder schwach entölt (ca. 20 bis 22 % Fett).
Inhaltsstoffe und Wirkung
Kakao enthält neben dem vergleichsweise hohen Gehalt an Fett (Kakaobutter 54 %) einige Substanzen, denen eine stimmungsaufhellende Wirkung bescheinigt wird. Dazu gehören Serotonin, Dopamin und Theobromin (3,7-Dimethylxanthin, C7H8N4O2), eine dem Coffein sehr ähnliche Substanz aus der Klasse der Methylxanthine. Obwohl diese Inhaltsstoffe nur in geringen Konzentrationen im Kakao enthalten sind, geht auf diese wohl die Feststellung „Schokolade macht glücklich“ zurück. Die gesundheitlichen Aspekte des Kakaokonsums sind bis heute nicht abschließend geklärt und daher weiterhin Gegenstand aktueller Forschungsarbeiten. Trotzdem wurden in zahlreichen Einzelstudien gesundheitsfördernde Wirkungen belegt, besonders für Schokoladen mit einem hohen Kakaoanteil (> 50 %). Diese positiven Wirkungen reichen von der Verminderung von Ablagerungen in Gefäßen, über die Senkung des LDL-Cholesterinspiegels, Förderung der Hautfunktionen, Leistungssteigerung bis hin zu einer Senkung des Blutdrucks.
Abbildung 3 zeigt ein Sortiment von Schokoladentafeln mit verschiedenen Kakaogehalten.

Polymorphie der Kakaobutter
Die Kakaobutter besteht chemisch vorwiegend aus Triglyceriden verschiedener Fettsäuren, hauptsächlich Palmitinsäure, Stearinsäure, Ölsäure und Linolsäure. Auf Grund der ausgeprägten PolymorphiePolymorphie ist die Fähigkeit eines festen Materials, verschiedene kristalline Strukturen (Synonym: Formen, Modifikationen) auszubilden.Polymorphie der Kakaobutter sind sechs im Temperaturbereich zwischen 17° C und 36 °C schmelzende Kristallstrukturen bekannt. Für die Herstellung von Schokolade ist es wichtig, dass bei dem Erstarren flüssiger Schokoladenmasse vorwiegend das Polymorph V, die sogenannte ß-Modifikation gebildet wird. Das wird durch eine spezielle Wärmebehandlung, das sogenannte Temperieren, erreicht. Dabei wird die Schokoladenmasse definiert abgekühlt und anschließend wieder erwärmt, um unerwünschte, niedrigschmelzende Kristalle wieder zu schmelzen. Das Auffinden der richtigen Temperatur ist hierbei schwierig, da bei Kakaobutter die Bildung von Kristallisationskeimen sehr träge erfolgt, das heißt, dass der Kristallisationsprozess sehr langsam verläuft und sich die Schokoladenmasse stark unterkühlen lässt, bevor die KristallisationAls Kristallisation bezeichnet man den physikalischen Vorgang der Verhärtung bei der Bildung und beim Wachstum von Kristallen. Bei diesem Prozess wird Kristallisationswärme frei.Kristallisation merklich einsetzt. Sind jedoch nach dem Erwärmen die niedrigschmelzenden Kristallformen bereits geschmolzen, aber noch ausreichende Mengen der hochschmelzenden Kristalle, der thermodynamisch stabilsten ß-Modifikation, vorhanden, so dienen diese gezielt als Impfkristalle für die anschließende Abkühlung. So entsteht bei der erneuten Abkühlung fast ausschließlich die gewünschte ß-Modifikation.
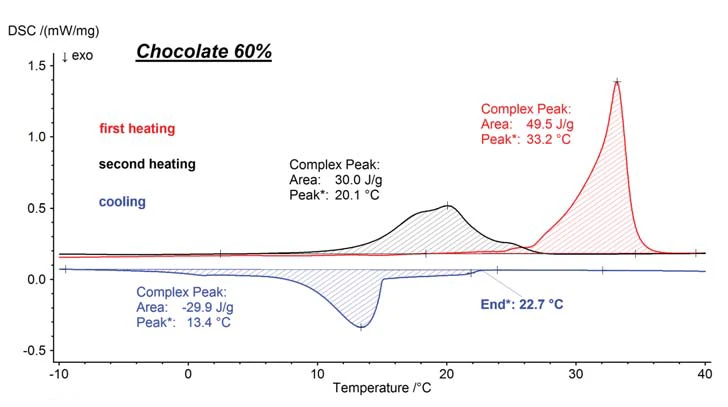
Dieser Sachverhalt lässt sich leicht mit Hilfe der Differential Scanning Calorimetry (DSC) nachvollziehen. In Abbildung 4 ist das Schmelzverhalten einer Schokolade (60 % Kakaogehalt) gezeigt. Die bei der Schokoladenherstellung gezielt erzeugte ß-Modifikation beginnt bei etwa 25 °C langsam zu schmelzen und erreicht das Peakmaximum in der ersten Aufheizung (rot) bei 33,2 °C. Während der Abkühlung (blau) kann der Kristallisationsbeginn bei 22,7 °C als extrapolierter Endset detektiert werden.
Ein Teil der Schmelze lässt sich jedoch bis auf etwa 15 °C unterkühlen, bevor auch diese Anteile kristallisieren. Bei einer Abkühlrate von 5 K/min dauert es bei dieser Probe bis zum Erreichen von etwa -5 °C, bis die KristallisationAls Kristallisation bezeichnet man den physikalischen Vorgang der Verhärtung bei der Bildung und beim Wachstum von Kristallen. Bei diesem Prozess wird Kristallisationswärme frei.Kristallisation abgeschlossen ist. Aus der Peakform der Abkühlkurve ist bereits ersichtlich, dass – im Gegensatz zu der vorangegangenen industriellen Fertigung – durch die Abkühlung in der DSC-Apparatur mehrere bei niedrigeren Temperaturen schmelzende Modifikationen der Kakaobutter entstanden sind. Belegt wird dies außerdem durch die Resultate der zweiten Aufheizkurve (schwarz).
Die während der Abkühlung in der DSC-Apparatur entstandenen Modifikationen beginnen bereits bei knapp über 10 °C zu schmelzen, was durch die endotherme Wärmetönung angezeigt wird. Das Schmelzen ist bereits bei 28 °C abgeschlossen, bei einer Temperatur, bei der die ursprüngliche Schokolade während der ersten Aufheizung gerade erst mit dem Schmelzen beginnt. Ein weiterer wichtiger Befund wird durch die Integrale der Schmelz- und Kristallisationsflächen geliefert. Diese sind proportional zu den Umwandlungswärmen und liefern so ein Maß für den Kristallinitätsgrad der Probe. Führen die kristallinen Anteile der Probe in ihrem Ausgangszustand zu einer Schmelztemperaturen und SchmelzenthalpienDie Schmelzenthalpie einer Substanz, auch bekannt als latente Wärme, stellt ein Maß der Energiezufuhr dar, typischerweise Wärme, welche notwendig ist, um eine Substanz vom festen in den flüssigen Zustand zu überführen. Der Schmelzpunkt einer Substanz ist die Temperatur, bei der die Substanz von einem festen (kristallinen) in den flüssigen Zustand (isotrope Schmelze) übergeht.Schmelzenthalpie von 49,5 J/g (erste Aufheizung, rote Kurve), so ist in der zweiten Aufheizung lediglich eine Schmelztemperaturen und SchmelzenthalpienDie Schmelzenthalpie einer Substanz, auch bekannt als latente Wärme, stellt ein Maß der Energiezufuhr dar, typischerweise Wärme, welche notwendig ist, um eine Substanz vom festen in den flüssigen Zustand zu überführen. Der Schmelzpunkt einer Substanz ist die Temperatur, bei der die Substanz von einem festen (kristallinen) in den flüssigen Zustand (isotrope Schmelze) übergeht.Schmelzenthalpie von 30,0 J/g detektiert worden (schwarze Kurve).
Das entspricht dem Kristallinitätsgrad, der während der Abkühlkurve erreicht werden konnte (vgl. Abkühlkurve, blau). Das bedeutet nicht nur, dass während der Abkühlung in der DSC-Apparatur bei einer linearen Abkühlrate von 5 K/min andere niedrigschmelzende Modifikationen entstanden sind als bei der ursprünglichen Herstellung der Schokolade, sondern auch, dass sich der Kristallinitätsgrad merklich verringert hat. Das belegt wiederum, dass, wie oben ausgeführt, für die gezielte Erzeugung eines hohen Anteils an hochschmelzender ß-Modifikation eine spezielle Temperaturbehandlung notwendig ist.
Variation des Kristallinitätsgrads von Schokolade durch Temperierung
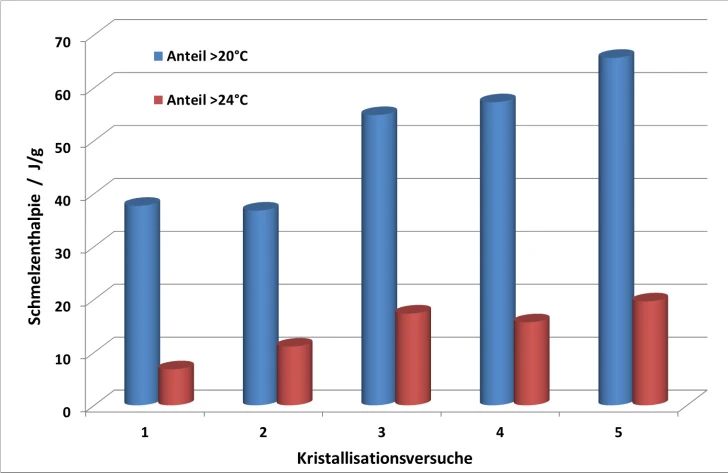
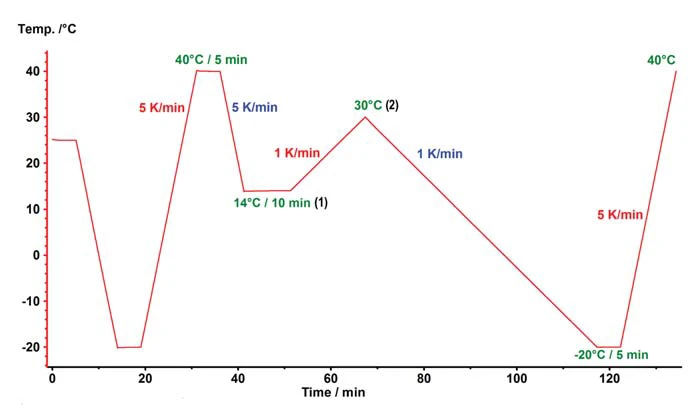
In der industriellen Fertigung von Schokolade wird die flüssige Schokoladenmasse einer mechanischen und thermischen Behandlung unterzogen, um gezielt die gewünschte hochschmelzende ß-Modifikation zu erhalten und die Kristallisation der übrigen Kakaobuttermodifikationen zu unterdrücken. Teilweise gelingt die Simulation einer solchen Behandlung auch innerhalb der DSC-Apparatur, jedoch verständlicherweise ohne die mechanische Komponente. Abbildung 5 zeigt die Veränderung der Schmelzpeakflächenanteile oberhalb von 20 °C und oberhalb von 24 °C für eine Reihe von Temperversuchen. Mit Kristallisationsversuch 1 ist dabei das Ergebnis aus einer linearen Abkühlrate von 5 K/min beschrieben. Die Versuche 2 bis 5 variieren die Auslagerungstemperatur (1) sowie die Temperatur, bei der die Kristallisationskeime der unerwünschten PolymorphiePolymorphie ist die Fähigkeit eines festen Materials, verschiedene kristalline Strukturen (Synonym: Formen, Modifikationen) auszubilden.Polymorphie wieder geschmolzen werden (2). Kristallisationsversuch 5 zeigt gegenüber der linearen Abkühlung eine deutliche Zunahme der Kristallinität. Dies konnte durch eine Temperierung der Probe von 10 Minuten bei 14 °C und einer anschließenden Erwärmung auf 30 °C erreicht werden. Das zugehörige Temperaturprogramm ist in Abbildung 6 gezeigt.
Zusammenhang zwischen Kakaogehalt und Schmelzenthalpie
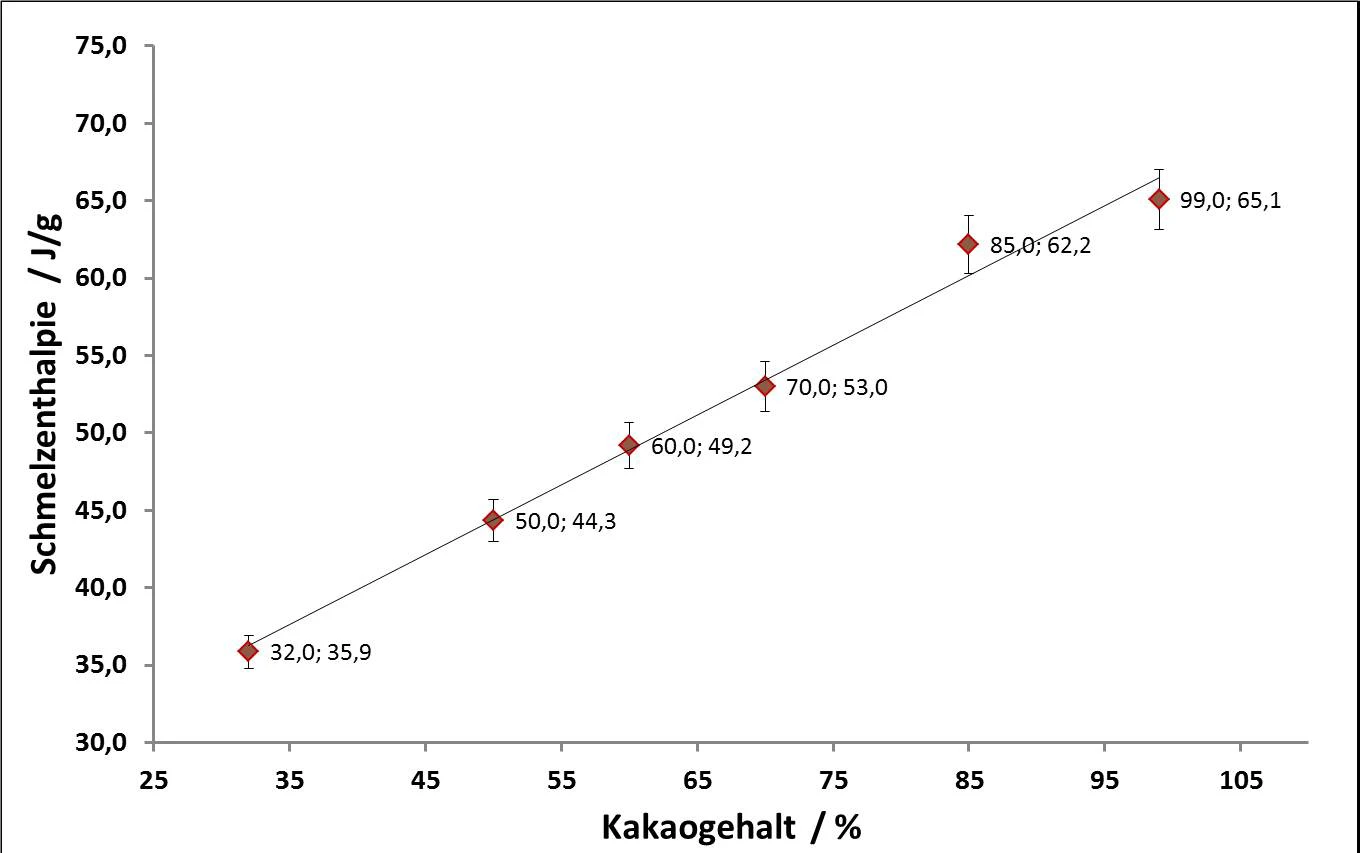
Untersucht man Schokoladen mit verschiedenen Kakaogehalten, so erkennt man einen weitgehend linearen Zusammenhang. Mit steigendem Kakaogehalt nimmt die Menge an kristalliner Kakaobutter zu und somit auch die zum Schmelzen notwendige Energie. Die Schmelzenthalpie kann aus der Peakfläche der ersten Aufheizung direkt ermittelt werden. Die Auftragung von nominellem Kakaogehalt und der detektierten Schmelzenthalpie ergibt einen linearen Zusammenhang, der in Abbildung 7 dargestellt ist. Die angegebenen Werte stellen Mittelwerte von jeweils fünf Messungen dar. Die angegebenen Fehlerbalken geben nicht die eigentlichen Messfehler an, sondern veranschaulichen lediglich, dass dieser lineare Zusammenhang mit einer Korrelation von + 3 % gilt.
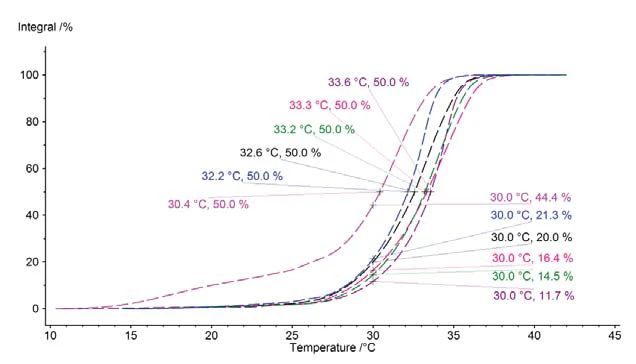
Da mit Hilfe der Fläche des Schmelzpeaks das Schmelzverhalten der verschiedenen Schokoladenproben nicht nur quantifiziert werden kann, sondern aus der Lage und der Peakform auch der Temperaturbereich und der Schmelzverlauf hervorgeht, ist es möglich, für jede Probe individuell anzugeben, wie viel des enthaltenen Fetts (Kakaobutter) bei der jeweiligen Temperatur noch fest ist und wie viel bereits flüssig vorliegt. Diese Information ist auch als Solid Fat Index (SFI) bekannt. Eine solche Aussage ist leicht zugänglich, wenn die Peakfläche auf 100 % normiert wird und der Verlauf als Flächenintegral dargestellt wird. Eine solche Auftragung ist in Abbildung 8 für alle untersuchten Schokoladenproben gezeigt. So lässt sich einerseits direkt ablesen, bei welcher Temperatur genau die Hälfte des jeweiligen Fettanteils noch fest vorliegt, und es ist andererseits leicht abzutragen, welcher Anteil des in der jeweiligen Probe enthaltenen Fetts bei einer bestimmten Temperatur (hier 30 °C) bereits geschmolzen ist.
Neben den hier exemplarisch gezeigten Möglichkeiten der Untersuchung des Schmelz- und Kristallisationsverhalten von Schokolade finden sich in der Literatur zahlreiche weitere Beispiele, die den Informationsgewinn von DSC-Messergebnissen unterstreichen. Cammenga et al. beschreiben den Nutzen der Differential Scanning Calorimetry für Süßwaren im Allgemeinen. In der Regel machen Zucker und Zuckeraustauschstoffe den größten Massenanteil solcher Produkte aus und messbare Eigenschaften, wie die GlasübergangstemperaturDer Glasübergang gilt als eine der wichtigsten Eigenschaften amorpher und teilkristalliner Materialien, wie z.B. anorganische Gläser, amorphe Metalle, Polymere, Pharmazeutika und Lebensmittel, usw., und bezeichnet den Temperaturbereich, in dem sich die mechanischen Eigenschaften des Material von einem harten und spröden Zustand in einen weicheren, verformbaren oder gummiartigen Zustand ändern.Glasübergangstemperatur, Kristallinität, Schmelztemperaturen und SchmelzenthalpienDie Schmelzenthalpie einer Substanz, auch bekannt als latente Wärme, stellt ein Maß der Energiezufuhr dar, typischerweise Wärme, welche notwendig ist, um eine Substanz vom festen in den flüssigen Zustand zu überführen. Der Schmelzpunkt einer Substanz ist die Temperatur, bei der die Substanz von einem festen (kristallinen) in den flüssigen Zustand (isotrope Schmelze) übergeht.Schmelztemperatur und Phasenumwandlungsenthalpien, um hier nur einige zu nennen, haben einen maßgeblichen Einfluss auf die physikochemischen und technolgischen Eigenschaften sowie die Lagerstabilität [1].
In einer ganzen Serie von Arbeiten beschreiben Ziegleder et al. die Langzeitstabilität [2] sowie die Fettreifbildung von Schokoladen [3].
Chapman et al. [4] sowie Merken et al. [5] widmen sich in ihren Arbeiten der Polymorphie und der Verarbeitbarkeit von Schokoladen, wohingegen Tscheuschner et al. [6] und Ziegleder et al. [7] zahlreiche Untersuchungen zu den Abkühlbedingungen und der Kristallisation von Schokoladen und Schokoladenmassen durchgeführt haben.
Zusammenfassung
Die Kakaobutter kristallisiert in sechs verschiedenen Kristallstrukturen (Polymorphie), wovon eine, die sogenannte ß-Modifikation, bei der Schokoladenproduktion bevorzugt gebildet werden sollte. Dazu ist ein spezielles Verfahren zur Temperaturbehandlung nötig, das sogenannte Temperieren. Mit Hilfe der DSC lassen sich nicht nur die Schmelztemperaturen und SchmelzenthalpienDie Schmelzenthalpie einer Substanz, auch bekannt als latente Wärme, stellt ein Maß der Energiezufuhr dar, typischerweise Wärme, welche notwendig ist, um eine Substanz vom festen in den flüssigen Zustand zu überführen. Der Schmelzpunkt einer Substanz ist die Temperatur, bei der die Substanz von einem festen (kristallinen) in den flüssigen Zustand (isotrope Schmelze) übergeht.Schmelztemperaturen der Kakaobutter bestimmen, die eine Aussage über die bei der Fertigung gebildeten Modifikationen liefern, sondern es ist darüber hinaus auch die Umwandlungsenthalpie (Schmelzenthalpie) zugänglich, die eine Quantifizierung der kristallinen Anteile der Kakaobutter erlaubt. Durch die Untersuchung von Schokoladen mit Kakaoanteilen zwischen 32 % und 99 % konnte belegt werden, dass ein weitgehend linearer Zusammenhang zwischen dem angegebenen Kakaogehalt und der mit Hilfe der DSC ermittelten Schmelzenthalpie besteht. Ferner wurde gezeigt, dass es auch möglich ist, den Einfluss des Temperierens auf die Quantität und die Unterscheidung der einzelnen kristallinen Modifikationen der Kakaobutter zu untersuchen. Die Abkühlgeschwindigkeit in Verbindung mit Isothermphasen und eventuell anschließendem kurzzeitigem Wiedererwärmen der Schokoladenmasse beeinflusst den resultierenden Kristallinitätsgrad. Somit besteht durch die Variabilität der Temperaturführung innerhalb der DSC-Analytik die Möglichkeit, das Temperieren der Schokoladenmasse in der Produktion nachzustellen. Neben der flexiblen Temperaturführung der Messprogramme einer DSC Untersuchung ergeben sich durch die Aussagekraft der Resultate weitere zahlreiche Möglichkeiten, die Wareneingangskontrolle, die Produktionsüberwachung oder auch die Qualitätskontrolle der Schokoladenproduktion mit Hilfe der Differential Scanning Calorimetry (DSC) abzusichern.