Introdução
O sorbitol é um álcool de açúcar encontrado em frutas que é frequentemente usado como adoçante em produtos alimentícios. Ele existe em quatro fases cristalinas anidras mais o hidrato. Esse PolimorfismoPolimorfismo é a capacidade de um material sólido de formar diferentes estruturas cristalinas (sinônimos: formas, modificações).polimorfismo influencia as propriedades dessa substância: Cada forma se comporta de maneira diferente com relação à fusão e à absorção de água [1].
Condições de teste
Uma amostra de sorbitol (massa: 3,81 mg) da Sigma-Aldrich foi preparada em um cadinho Concavus® e medida com o DSC 204 F1 Nevio . Um aquecimento inicial foi realizado entre -80°C e 150°C a uma taxa de aquecimento de 10 K/min. Em seguida, a amostra foi resfriada a 10 K/min e aquecida novamente na mesma faixa de temperatura. Depois disso, o cadinho foi mantido por 24 horas em temperatura ambiente, antes de ser medido uma terceira vez entre -80°C e 150°C sob as mesmas condições. As medições de DSC foram realizadas em uma atmosfera dinâmica de nitrogênio.
Além disso, foram realizadas medições de PXRD em dois estados de amostra:
- Amostra como recebida
- Amostra após aquecimento a 150°C e 24 horas em temperatura ambiente
Essas medições foram realizadas com o difratômetro Bruker D8 Advance na solid-chem GmbH.
Resultados do teste
A Figura 2 exibe as curvas DSC do sorbitol durante as três execuções de aquecimento. O pico EndotérmicoUma transição de amostra ou uma reação é endotérmica se for necessário calor para a conversão.endotérmico com uma temperatura de início extrapolada de 91°C, detectado durante o primeiro aquecimento, resulta daTemperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica). fusão da amostra. Essa temperatura é típica da modificação conhecida como forma gama, que é a mais adequada para aplicações comerciais por ser a mais estável.
Após o resfriamento a 10 K/min, nenhum pico deTemperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica). fusão foi detectado no segundo aquecimento subsequente: A amostra não apresenta mais nenhuma fase cristalina e está em um estado amorfo com a Temperatura de transição do vidroA transição vítrea é uma das propriedades mais importantes dos materiais amorfos e semicristalinos, por exemplo, vidros inorgânicos, metais amorfos, polímeros, produtos farmacêuticos e ingredientes alimentícios etc., e descreve a região de temperatura em que as propriedades mecânicas dos materiais mudam de duras e quebradiças para mais macias, deformáveis ou emborrachadas.transição vítrea a -1°C (temperatura média).
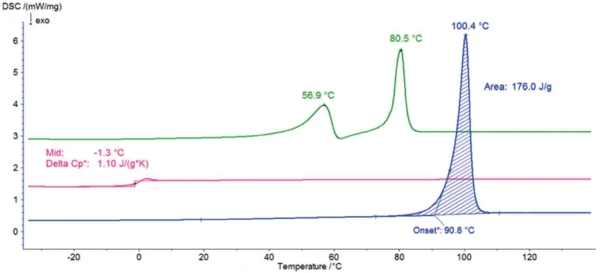
Um dia em temperatura ambiente é suficiente para que ocorra a CristalizaçãoA cristalização é o processo físico de endurecimento durante a formação e o crescimento de cristais. Durante esse processo, o calor da cristalização é liberado.cristalização. No entanto, os picos detectados a 57°C e 81°C (temperaturas de pico) comprovam que se trata de uma forma cristalina diferente daquela detectada durante o primeiro aquecimento. Essa curva de DSC é típica para a modificação chamada deTemperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica). fusão cristalizada. Essa forma é mais higroscópica do que a forma gama. No entanto, ela é usada comercialmente devido à sua aparência transparente e vítrea, por exemplo, na produção de balas duras.
As temperaturas deTemperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica). fusão das formas cristalinas medidas neste trabalho são comparadas com diferentes fontes da literatura na tabela 1.
Tabela 1: Temperaturas de pico das formas cristalinas: fusão cristalina, alfa, gama e temperaturas de Temperatura de transição do vidroA transição vítrea é uma das propriedades mais importantes dos materiais amorfos e semicristalinos, por exemplo, vidros inorgânicos, metais amorfos, polímeros, produtos farmacêuticos e ingredientes alimentícios etc., e descreve a região de temperatura em que as propriedades mecânicas dos materiais mudam de duras e quebradiças para mais macias, deformáveis ou emborrachadas.transição vítrea da forma amorfa para este trabalho e diferentes fontes.
| Forma/Temperatura [°C] | Este trabalho | Fonte [1] | Fonte [3] | Fonte [4] | Fonte [5] |
|---|---|---|---|---|---|
| Derretimento cristalizado (1º pico) | 56.9 | 54.5 | 55 | - | - |
| Massa fundida cristalizada (2º pico) | 80.5 | 70.8 | 75 | - | - |
| Alfa | - | 85.9 | 86 | 88.5 | - |
| Gama | 100.4 | 98.0 | 97 | 100 | 101.7 |
| Amorfo | -1.3 | - | - | - | -0.4 |
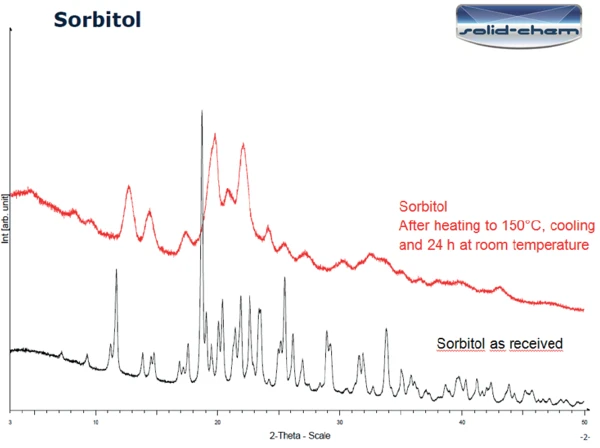
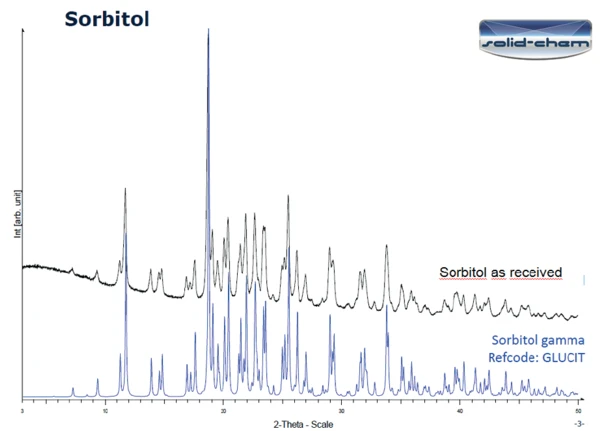
A Figura 3 exibe os resultados de PXRD na amostra como recebida (parte inferior) e na amostra após aquecimento a 150 °C seguido de 24 horas em temperatura ambiente (parte superior). As duas curvas diferem significativamente. Os picos detectados na medição da amostra como recebida correspondem à forma gama do sorbitol (Figura 4). De acordo com a literatura ([1], figura 6 [padrão de difração de pó de raios X do polimorfo deTemperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica). fusão cristalizada do sorbitol]), a curva após o aquecimento a 150 °C e um dia em temperatura ambiente pode de fato ser classificada como a fusão cristalizada do sorbitol.
Conclusão
Apenas um único aquecimento com o DSC 204 F1 Nevio permite a identificação da forma polimórfica do sorbitol fornecido. Durante o resfriamento da forma gama a 10 K/min a partir da fusão, o sorbitol não se cristaliza, mas forma uma fase amorfa. Essa estrutura amorfa pode se cristalizar à temperatura ambiente como uma nova modificação chamada de fusão cristalizada. Esses resultados foram confirmados por medições de PXRD.
Cada uma das modificações do sorbitol tem propriedades físicas diferentes. É por isso que elas precisam ser caracterizadas antes do processamento. O DSC 204 F1 Nevio fornece os resultados necessários de forma fácil, rápida e confiável.
Reconhecimento
NETZSCH gostaria de agradecer à solid-chem GmbH em Bochum, Alemanha, por realizar as medições e a avaliação de PXRD.