Введение
Солома - это общий термин для обмолоченных, высушенных стеблей зерновых и листьев растений, используемых для производства масел и волокон. Помимо использования в сельском хозяйстве, солома также может стать важным энергоносителем,нейтральным по отношению к CO2, в будущем. Она является прекрасным видом биомассы, поскольку представляет собой побочный продукт земледелия. В отличие от других видов биотоплива, для его выращивания не требуется никаких специальных мер или дополнительных земель. Кроме того, летучая зола, образующаяся в процессе сжигания, может быть использована в качестве удобрения для почвы на местных фермах.
Термогравиметрический анализ (ТГА) или одновременный термический анализ (STA), который подразумевает одновременное проведение ТГА и дифференциальной сканирующей калориметрии (ДСК), особенно хорошо подходят для исследования процессов пиролиза или горения. Можно быстро получить информацию о термической стабильности большинства твердых топлив в терминах температур реакции, а также о кинетике горения. Кроме того, можно количественно оценить потерю массы при пиролизе или сгорании и содержание золы.
Описанное здесь измерение изучает поведение соломы при разложении [1]. Газы, выделяющиеся при разложении, определяются с помощью ИК-Фурье спектроскопии с использованием полностью интегрированной системы STA-FT-IR NETZSCH Perseus STA 449 (см. рис. 1).

Результаты измерений
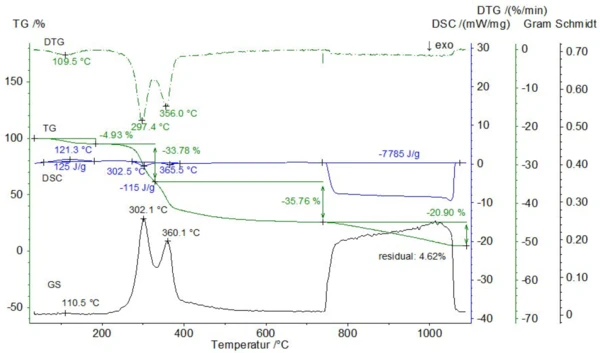
Порошкообразный образец соломы неизвестного происхождения с начальной массой 28,64 мг был измерен в платиновом тигле с проколотой крышкой при скорости нагрева 20 К/мин. Газовая атмосфера менялась с чистого азота на воздух при температуре 740°C (расход газа составлял 70 мл/мин). Ниже 740°C происходили три ступени потери массы 4,9%, 33,8% и 35,8%, которые сопровождались одним эндотермическим и двумя перекрывающимися экзотермическими эффектами с энтальпиями 125 Дж/г и -115 Дж/г (см. рис. 2). Во время этих этапов потери массы сигнал Грамма-Шмидта, отражающий сумму всех ИК-Фурье поглощений для всех номеров волн, показал максимумы при 111°C, 302°C и 360°C, которые хорошо коррелируют с кривой ДТГ. Еще одна ступень потери массы на 20,9%, а также экзотермический эффект с общей энтальпией -7,79 кДж/г произошли после перехода на воздух при 740°C. Эти эффекты обусловлены сгоранием так называемой пиролитической сажи, оставляющей остаточную массу 4,6%, которая отражает содержание золы.
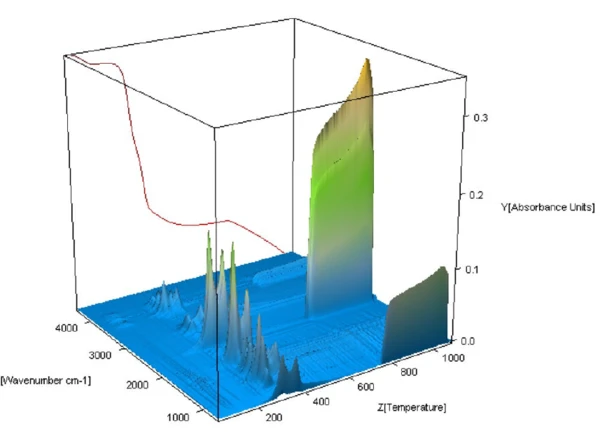
На рисунке 3 показано трехмерное изображение ИК-Фурье спектров выделившихся газов, собранных в процессе разложения соломы. Особый интерес представляют спектры ниже 740°C, где происходил пиролиз образца. Сильное ИК-Фурье поглощение при более высоких температурах обусловлено выделениемCO2 в результате сгорания.
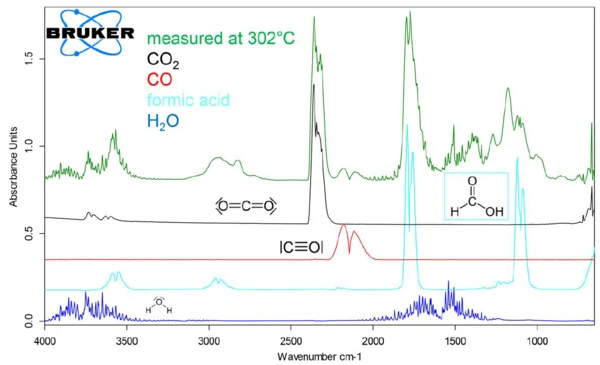
Выделяющиеся газы были идентифицированы путем сравнения отдельных, извлеченных двумерных спектров при определенных температурах со спектрами library. Например, на рисунке 4 показано, что спектр газов, выделившихся при 302°C, соответствует смеси, содержащейCO2, CO, H2Oи муравьиную кислоту (HCOOH). Эволюция отдельных видов газов в процессе разложения образца может быть прослежена путем интегрирования характерного диапазона ИК-Фурье поглощения для молекул и наложения кривой значений интегрирования в зависимости от температуры на кривые ТГА и ДТГ, полученные в результате анализа. Диапазон между 2200 и 2450 см-1 был интегрирован дляCO2, между 1950 и 2150 см-1 для CO, между 1300 и 1600 см-1 для H2Oи между 1000-1150 см-1 для HCOOH.
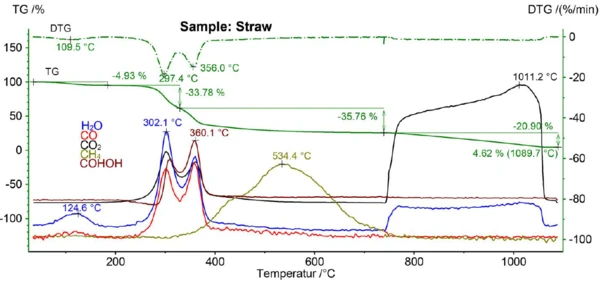
Как видно из рисунка 5, H2Oвыделялась на1-м этапе потери массы (испарение влаги) и на2-м и3-м этапах потери массы (пиролиз), во время которых также выделялись CO,CO2 и HCOOH. CH4 выделялся в широком диапазоне температур с максимумом при 534°C, аCO2 был обнаружен выше 740°C в результате сжигания образца на воздухе.
Заключение
Продемонстрировано использование очень компактной системы сопряжения STA-FT-IR NETZSCH Perseus STA 449 для определения характеристик пиролиза и горения соломы [1]. Наблюдалась хорошая корреляция между обнаруженными этапами потери массы и выделением газов, что свидетельствует о преимуществе прямого интерфейса связи. Идентификация выделяющихся газов с помощью базы данных search позволяет детально интерпретировать химический состав, вовлеченный в этапы потери массы, связанные с пиролизом, в частности.