مقدمة
استخدمت الثقافات الراقية المبكرة لحاء الصفصاف بالفعل كعلاج للحمى والألم [1]؛ فقد اعتبر العالم الروماني بلينيوس الأكبر لحاء الصفصاف دواءً، كما أنتج التيوتونيون والكلتيون مستخلصات بطبخ لحاء الصفصاف، وكانت مكوناته مرتبطة كيميائياً بحمض أسيتيل الساليسيليك الاصطناعي [2]. على الرغم من أن العديد من الكيميائيين تمكنوا من إنتاج الساليسين وحمض الساليسيليك في القرن التاسع عشر، إلا أن فيليكس هوفمان لم ينجح في تصنيع حمض أسيتيل الساليسيليك بدون شوائب حتى عام 1897 في مقر شركة باير في فوبرتال-إلبيرفيلد بألمانيا. اختبر كورت فيتاور (الشكل 2) هذا الدواء على المرضى في السنوات التالية إلى أن تقدمت شركة باير (الشكل 1) أخيرًا للحصول على براءة الاختراع المقابلة في عام 1921. بدأ مسكن الألم هذا يحقق نجاحًا باهرًا في جميع أنحاء العالم، واليوم تنتج باير أكثر من 50,000 طن من حمض أسيتيل الساليسيليك سنويًا [4].


تتوفر الأدوية التي تحتوي على المادة الفعالة حمض أسيتيل الساليسيليك في أشكال صيدلانية مختلفة وتستخدم ليس فقط بسبب تأثيرها المسكن ولكن أيضًا بسبب خصائصها المضادة للالتهابات وخافضة للحرارة ومضادة للصفيحات.
حمض أسيتيل الساليسيليك النقي عبارة عن مسحوق أبيض نقي ضعيف الذوبان في الماء، وتبلغ درجة انصهاره 136 درجة مئوية ويتحلل في درجات حرارة أعلى. تم استخدام طرق مختلفة للتحليل الحراري والتحليل الطيفي بالأشعة تحت الحمراء ومزيج من الاثنين في هذا العمل لدراسة نواتج التحلل الغازي.
الطرق والتحضير
تم الحصول على حمض أسيتيل الساليسيليك (CAS: 50-78-2) من شركة سيجما ألدريتش بدرجة نقاء > 99%. وللتحقق من المادة الأصلية، استُخدم جهاز BRUKER TENSOR II لقياس العينات بالانعكاس الكلي الموهن (ATR). ولتحديد سلوك الذوبان، استُخدم جهاز NETZSCH DSC 214 Polyma. ولتحديد الخصائص الحرارية للغازات المنطلقة، اقترن الميزان الحراري بمطياف الأشعة تحت الحمراء - NETZSCH TG 209 F1 Libra® إلى Bruker Equinox 55/S. ويرد في الجداول من 1 إلى 3 ملخص لظروف القياس للتحليل الحراري والتحليل الطيفي.
الجدول 1: شروط القياس لفحص DSC لحمض أسيتيل الساليسيليك
| حمض أسيتيل الساليسيليك | |
|---|---|
| كتلة العينة | 2.08 مجم |
| مادة البوتقة | ألومنيوم، مثقوب |
| كتلة البوتقة | 52.75 مجم |
| نطاق درجة الحرارة | 25 ... 160°C |
| معدل التسخين | 7 كلفن/دقيقة |
| الغلاف الجوي | نيتروجين (50 مل) |
الجدول 2: شروط القياس لفحص قياس الثقل الحراري لأقراص الأسبرين® بواسطة TGA-FT- IR
| الأسبرين® | |
|---|---|
| كتلة العينة | 9.141 مجم |
| مادة البوتقة | ألومينا، مفتوحة |
| كتلة البوتقة | 162.75 مجم |
| نطاق درجة الحرارة | 25 ... 600°C |
| معدل التسخين | 10 كلفن/دقيقة |
| الغلاف الجوي | نيتروجين (40 مل) |
| المسح | 32 |
| الدقة | 4 سم-1 |
| النطاق الطيفي | 650 - 4500 سم-1 |
الجدول 3: شروط القياس للفحص الطيفي (ATR) لحمض أسيتيل الساليسيليك
| حمض أسيتيل الساليسيليك | |
|---|---|
| الكاشف | DTGS |
| المسح | 32 |
| الدقة | 4 سم-1 |
| النطاق الطيفي | 650 - 4500 سم-1 |
النتائج والمناقشة
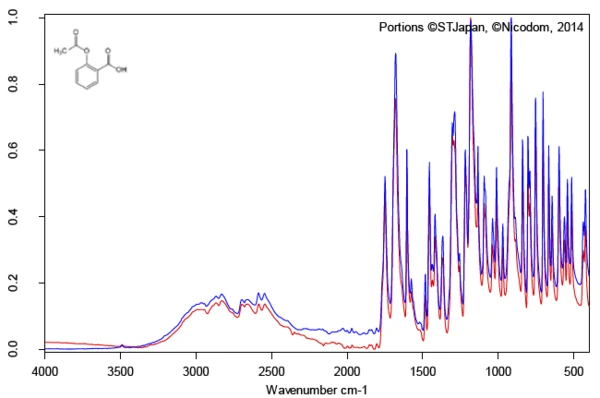
أسفر فحص المادة الفعالة حمض أسيتيل الساليسيليك بمساعدة التحليل الطيفي بالأشعة تحت الحمراء FT-IR عن طيف الأشعة تحت الحمراء في درجة حرارة الغرفة والذي يتوافق بشكل جيد مع طيف المكتبة (Bruker ATR-LIBPolymers-1-472-2) (الشكل 3). تشير الشركة المصنعة إلى أن نطاق انصهار حمض أسيتيل الساليسيليك يتراوح بين 134 درجة مئوية و136 درجة مئوية. يوفر الفحص عن طريق قياس المسح التفاضلي للسعرات الحرارية (DSC) إنثالبي ذوبان يبلغ 178 جول/غرام ودرجة حرارة للبداية الاستقرائية تبلغ 138.5 درجة مئوية. وكما يتضح أيضًا من الشكل 4، تشير إشارة التدفق الحراري إلى بداية عملية ذوبان العينة بالفعل عند درجات حرارة أقل بكثير من تلك التي يحددها التقييم المتوافق مع المعايير للبداية المستقراة. في الأدبيات، تم وصف شكلين متعددي الأشكال من حمض أسيتيل الساليسيليك: الشكل الأول بدرجة حرارة انصهار 144.9 درجة مئوية والشكل الثاني بدرجة حرارة انصهار 135.5 درجة مئوية [5، 6].
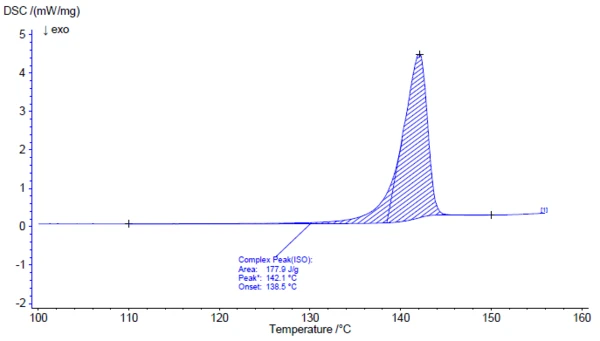
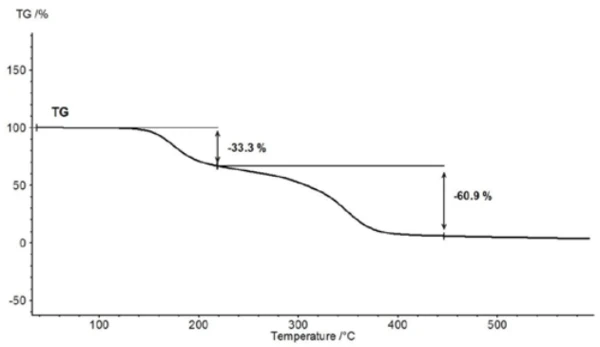
ويبدأ التحلل الحراري لحمض أسيتيل الساليسيليك فوق 150 درجة مئوية تقريبًا. ولذلك، فإن قياس الثقل الحراري (TGA) هو الأنسب لمزيد من التوصيف فوق نقطة الانصهار (الشكل 5).
لتوصيف التحلل الحراري، تم فحص قطعة من قرص الأسبرين بمساعدة اقتران TGA-FT-الأشعة تحت الحمراء. على الرغم من أن نتائج قياس الثقل الحراري بين 150 درجة مئوية و450 درجة مئوية تُظهر تفاعل تحلل حراري من خطوتين ويمكن تحديد كميات الغازات المنطلقة كمياً، إلا أنه لا يمكن تحديد الغازات المسؤولة عن فقدان الكتلة المكتشفة دون تحليل طيفي. في حالة إجراء قياس يقترن فيه الميزان الحراري بمطياف الأشعة تحت الحمراء، يمكن فحص المرحلة الغازية بشكل مستمر خلال القياس بأكمله. يتم عرض جميع أطياف الأشعة تحت الحمراء في ترتيب ثلاثي الأبعاد، مقياس درجة الحرارة، في الشكل 6. يمكن أيضًا رؤية نتائج قياس الثقل الحراري في المنطقة الخلفية اليسرى.
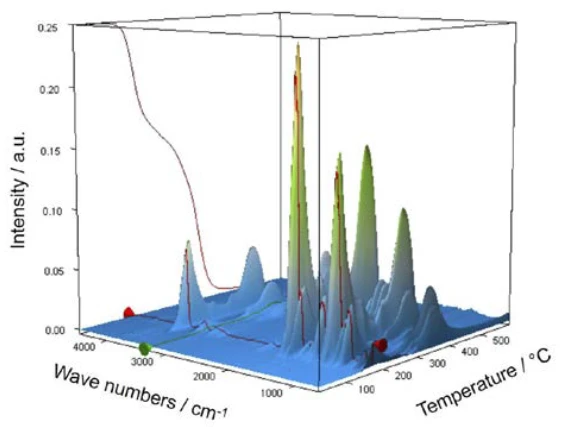
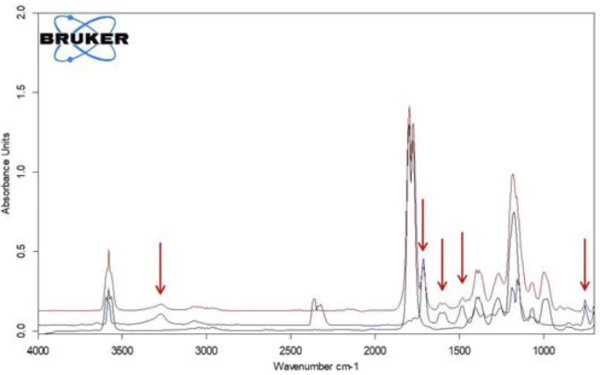
إذا تم استخراج أطياف فردية من هذا العرض عند درجات الحرارة ذات أعلى كثافة امتصاص، يمكن تحديد الغازات المنطلقة بمساعدة أطياف المقارنة من مكتبات الطور الغازي. يتوافق الطيف الفردي لخطوة فقدان الكتلة الأولى عند درجة حرارة 180 درجة مئوية، وهو طيف مميز، بشكل جيد للغاية مع طيف حمض الأسيتيك من مكتبة الطور الغازي EPANIST (الشكل 7). تشير الأسهم الحمراء إلى نطاقات الامتصاص التي لا تتطابق مع حمض الأسيتيك، ولكنها تتوافق بشكل جيد للغاية مع نطاقات الامتصاص لحمض الساليسيليك (EPA-NIST). ويؤدي ذلك إلى افتراض أن حمض أسيتيل الساليسيليك، كما في معادلة التفاعل 1، يتحلل حراريًا إلى حمض الساليسيليك وحمض الخليك (المعادلة 1). عند درجة حرارة 180 درجة مئوية، يكون حمض الأسيتيك المتكون غازياً بالفعل، بينما يبدأ حمض الساليسيليك الذي تبلغ درجة انصهاره 159 درجة مئوية في التبخر. وهذا بالتأكيد هو السبب أيضًا في أن خطوة فقدان الكتلة الأولى تنتقل مباشرةً إلى الخطوة التالية. يؤكد الجمع بين التحلل والتبخر آلية التحلل التي اقترحها ريبيرو وآخرون [7]. وبالاقتران مع شكل قرص حمض أسيتيل الساليسيليك المكون النشط، يتم التأكيد على تأثير الرطوبة على نواتج تفاعل التحلل الحراري إلى جانب المواد المضافة مثل النشا ومونوهيدرات ستيرات المغنيسيوم. ومع ذلك، يشير جوبتشوب وآخرون إلى أن المادة الفعالة الجافة لحمض أسيتيل الساليسيليك يمكن أن تضمن في حد ذاتها وجود الماء من خلال التمازج بمعنى التكثيف [8].
عند مقارنة طيفين لحمض الأسيتيك وحمض الساليسيليك، يلاحظ أن نطاقات الامتصاص في النطاق بين 1760 سم-1 و1820 سم-1 يمكن أن تعزى فقط إلى حمض الأسيتيك، في حين أن نطاقات الامتصاص بين 1460 سم-1 و1500 سم-1 تمثل حمض الساليسيليك. إذا تم حساب مسار كثافة نطاقات الامتصاص كدالة لدرجة الحرارة، يتم الحصول على "آثار" لكل مادة، وهي تتناسب مع الكميات المقابلة المنطلقة كدالة لدرجة الحرارة.
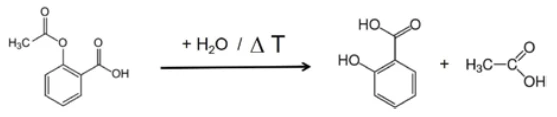
(المعادلة 1)
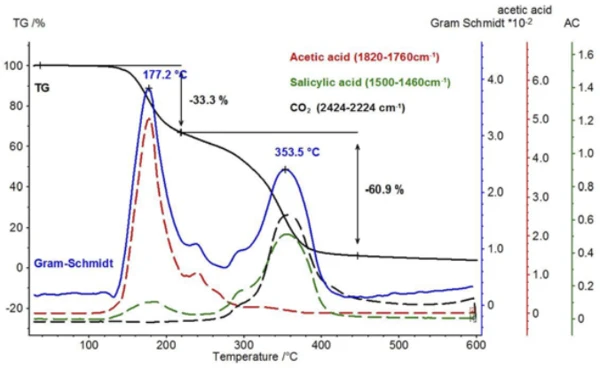
وتظهر مقارنة هذه الآثار المعتمدة على درجة الحرارة لحمض الأسيتيك وحمض الساليسيليك في الشكل 8 مع أثر جرام-شميت (مجموع الشدة التي لا تعتمد على الطول الموجي) وإشارة TGA. كما هو الحال مع إشارة TGA، يكشف تتبع جرام-شميت أن خطوة فقدان الكتلة الأولى تمر مباشرة وبدون هضبة إلى خطوة فقدان الكتلة الثانية. يمكن العثور على السبب في ذلك في آثار المنتجين، والتي تُظهر أنه يمكن اكتشاف إطلاق حمض الأسيتيك حتى حوالي 300 درجة مئوية، وبالإضافة إلى ذلك، يبدأ تبخر حمض الساليسيليك بالفعل في درجات حرارة منخفضة.
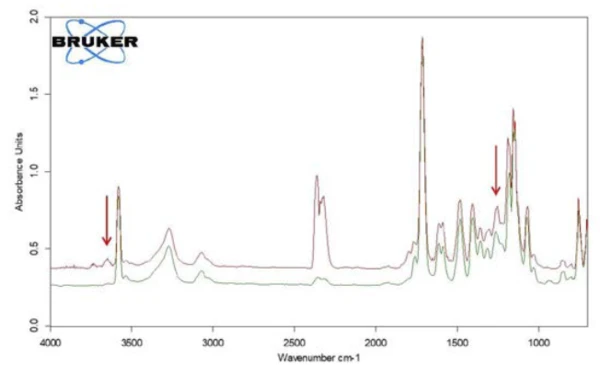
إلى جانب حمض الساليسيليك، يمكن أيضًا اكتشاف تكوين ثاني أكسيد الكربون عن طريق المسار المعتمد على درجة الحرارة لشدة الامتصاص. وهذا ما يؤكده الطيف الفردي المستخرج عند درجة حرارة 360 درجة مئوية (الشكل 9).
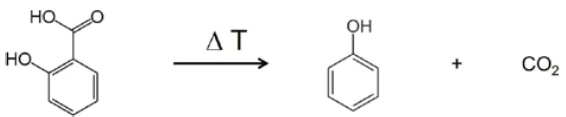
في النطاق بين أرقام الموجات 2424 و2224، تظهر بوضوح نطاقات امتصاص CO2. بالإضافة إلى ذلك، هناك مؤشرات على تكوُّن الفينول. تم تحديد مواضع نطاقات الامتصاص الأكثر كثافة للفينول بأسهم حمراء. لذلك يمكن افتراض أنه - إلى جانب تبخر حمض الساليسيليك - تحدث أيضًا عملية تحلل؛ وهذا يشير إلى تكوين الفينول وثاني أكسيد الكربون كما هو موضح في المعادلة 2.
(المعادلة 2)
الملخص
تم فحص حمض أسيتيل الساليسيليك باستخدام التحليل الطيفي بالأشعة تحت الحمراء للأشعة تحت الحمراء في درجة حرارة الغرفة (ATR)، واستخدمت أطياف الأشعة تحت الحمراء للأشعة تحت الحمراء للأشعة تحت الحمراء التي تم الحصول عليها لتحديد الهوية عن طريق المقارنة مع مكتبة أطياف. استُخدم DSC لفحص سلوك الذوبان. Additionally, the thermal behavior of Aspirin® was characterized by means of TGA-FT-IR. تمت مقارنة أطياف الغازات المنبعثة أثناء المعالجة الحرارية بمكتبة الطور الغازي لتحديد النواتج. وهكذا أمكن تأكيد آليات التحلل المعروفة من الأدبيات كما تبين أيضًا أن المواد المضافة الشائعة المستخدمة في تصنيع أقراص الأسبرين® لا يبدو أن لها تأثيرًا يمكن اكتشافه على تكوين نواتج التحلل الغازي.