مقدمة
الدولوميت هو معدن يتكون من كربونات الكالسيوم المغنيسيوم، المعروف كيميائياً باسم CaMg(CO3)2. وهو مورد طبيعي أساسي ذو أهمية تقنية كبيرة في مختلف الصناعات. ومن أبرز تطبيقاته في صناعة البناء والتشييد، حيث يُستخدم الدولوميت كمادة بناء وركام في الخرسانة. صلابته ومتانته تجعله مكونًا مثاليًا لقاعدة الطرق والكتل الخرسانية والأسفلت. كما تعزز مقاومة الدولوميت للعوامل الجوية والتآكل من قيمته في مشروعات البنية التحتية.
ويُعد فهم نسبة الكالسيوم إلى المغنيسيوم في الدولوميت أمرًا بالغ الأهمية لتحسين استخداماته. يمكن أن يؤثر اختلاف نسب هذين العنصرين بشكل كبير على الخصائص الفيزيائية والكيميائية للمعدن مثل قابلية الذوبان ومعدلات التفاعل والبنية البلورية. من خلال معرفة هذه النسبة والتحكم فيها، يمكن للمصنعين تكييف الدولوميت لتطبيقات محددة، مما يضمن الخصائص والأداء المطلوب.
النتائج والمناقشة
للتحقق من نسبة Ca/Mg في الدولوميت، أُجريت قياسات باستخدام جهاز NETZSCH STA 449 F3 Jupiter® باستخدام أجواء غازية مختلفة. يمكن الاطلاع على تجميع مفصل لظروف القياس في الجدول 1.
الجدول 1: معلمات القياس
| الأداة | STA 449 F3 جوبيتر |
| فرن | فرن كربيد السيليكون |
| جهاز الاستشعار | أنواع TG-DSC |
| بوتقة | 85 ميكرولتر Al2O3 بغطاء مثقوب |
| برنامج درجة الحرارة | 40 درجة مئوية - 1200 درجة مئوية عند كلفن/دقيقة |
| الغلاف الجوي | 70 مل/الدقيقة من الهواء الاصطناعي أو ثاني أكسيد الكربون |
| كتلة العينة | حوالي 40 مجم |
السلوك الحراري للدولوميت تحت الهواء
عندما يتم تسخين الدولوميت في وجود الأكسجين، فإنه يخضع للتحلل الحراري. يمكن تمثيل تفاعل التحلل على النحو التالي:
CaMg(CO3)2 → CaO + MgO + 2 CO2 (1)
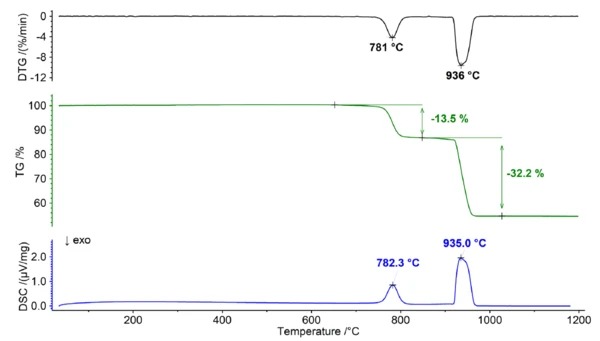
أثناء عملية التحلل هذه (انظر الشكل 1)، يتحلل الدولوميت الصلب إلى أكسيد الكالسيوم (CaO) وأكسيد المغنيسيوم (MgO) وغاز ثاني أكسيد الكربون (CO2). ويحدث هذا التفاعل عند درجات حرارة أعلى من 700 درجة مئوية وينتج عنه خطوة فقدان كتلة واسعة النطاق تُظهر قممًا متعددة ضمن إشارة DTG وDSC. وتعيق خاصية التداخل في فقدان الكتلة بشكل كبير القدرة على تعيين خطوات متميزة في منحنى TGA، مما يجعل من المستحيل تحديد أي معلومات إضافية بشأن نسبة الكالسيوم/المغنيسيوم في الدولوميت.
السلوك الحراري للدولوميت في جو من ثاني أكسيد الكربون
في وجود الغلاف الجوي المحتوي على ثاني أكسيد الكربون، يُظهر الدولوميت سلوكًا مختلفًا بسبب الطبيعة الانعكاسية لتفاعل التحلل وتفاوت ثبات الكربونات المتضمنة. يمكن أيضًا تمثيل تفاعل التحلل (1) كتفاعلي توازن فرديين على النحو التالي:
MgCO3 → MgO + CO2 (2)
CaCO3 → CaO + CO2 (3)
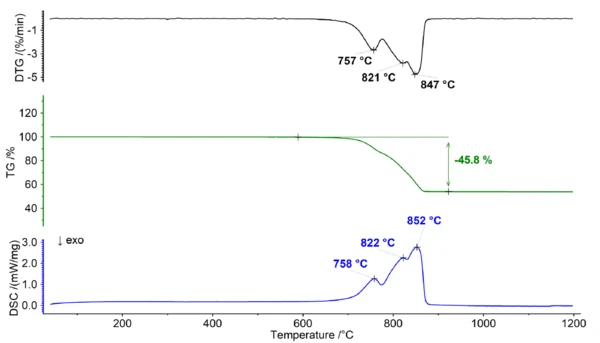
يتأثر التوازن بين المتفاعلات ونواتج التفاعل بعوامل مختلفة، بما في ذلك درجة الحرارة وتركيزات ثاني أكسيد الكربون. عندما يكون ثاني أكسيد الكربون موجودًا باستمرار، يكون له تأثير على التوازن، مما يتسبب في تحول نحو استقرار الكربونات ويؤدي إلى ارتفاع درجة حرارة التحلل. يكون هذا التأثير أكثر بروزًا بالنسبة لكربونات الكالسيوم منه بالنسبة لكربونات المغنيسيوم نظرًا لكونها أكبر. طاقة جيبس للتكوين. ونتيجةً لذلك، يمكن التمييز بوضوح بين تحلل كربونات الكالسيوم وكربونات المغنيسيوم عند قياسها تحت جو من ثاني أكسيد الكربون النقي (انظر الشكل 2). ويوفر هذا الفصل فرصة لتحديد نسبة Ca/Mg بدقة في الدولوميت، حيث يمكن أن تُعزى الخطوة الأولية إلى تحلل MgCO3 (التفاعل 2)، بينما تتوافق الخطوة اللاحقة مع تحلل CaCO3 (التفاعل 3).
الخاتمة
يؤثر اختيار الغلاف الجوي الأمثل تأثيرًا كبيرًا على جودة وكمية المعلومات التي يمكن الحصول عليها من خلال قياسات التحليل الحراري. ويرد مثال على هذه الظاهرة في التحليل الحراري المقدم لعينة من الدولوميت. في هذه الحالة، أدى الانتقال من جو الهواء التقليدي إلى اختيار ثاني أكسيد الكربون غير التقليدي إلى حد ما إلى تأثير ملحوظ على الخصائص الحرارية المقاسة للدولوميت الذي تم تحليله. ونتيجة لذلك، أصبح من الممكن الوصول إلى معلومات جديدة تمامًا مثل نسبة الكالسيوم إلى المغنيسيوم.