Introduzione
La dolomite è un minerale composto da carbonato di calcio e magnesio, chimicamente noto come CaMg(CO3)2. È una risorsa naturale essenziale con un'importanza tecnica significativa in diversi settori. Un'applicazione importante è quella nell'industria delle costruzioni, dove la dolomite viene utilizzata come materiale da costruzione e come aggregato nel calcestruzzo. La sua durezza e la sua durata la rendono un componente ideale per la base stradale, i blocchi di cemento e l'asfalto. La resistenza della dolomite agli agenti atmosferici e all'erosione ne aumenta ulteriormente il valore nei progetti infrastrutturali.
La comprensione del rapporto tra calcio e magnesio nella dolomite è fondamentale per ottimizzare le sue applicazioni. Rapporti diversi tra questi elementi possono avere un impatto significativo sulle proprietà fisiche e chimiche del minerale, come la solubilità, la velocità di reazione e la struttura cristallina. Conoscendo e controllando questo rapporto, i produttori possono personalizzare la dolomite per applicazioni specifiche, garantendo le caratteristiche e le prestazioni desiderate.
Risultati e discussione
Per studiare il rapporto Ca/Mg della dolomite, le misure sono state effettuate con lo strumento NETZSCH STA 449 F3 Jupiter® utilizzando diverse atmosfere gassose. La tabella 1 riporta un elenco dettagliato delle condizioni di misurazione.
Tabella 1: Parametri di misura
| Strumento | STA 449 F3 Jupiter® |
| Forno | Forno a carburo di silicio |
| Sensore | Tipi TG-DSC |
| Crogiolo | 85 μl Al2O3 con coperchio forato |
| Programma di temperatura | 40°C - 1200°C mit a K/min |
| Atmosfera | 70 ml/min di aria sintetica o anidride carbonica |
| Massa del campione | circa 40 mg |
Comportamento termico della dolomia sotto aria
Quando la dolomite viene riscaldata in presenza di ossigeno, subisce una Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. decomposizione termica. La Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. reazione di decomposizione può essere rappresentata come segue:
CaMg(CO3)2 → CaO + MgO + 2CO2 (1)
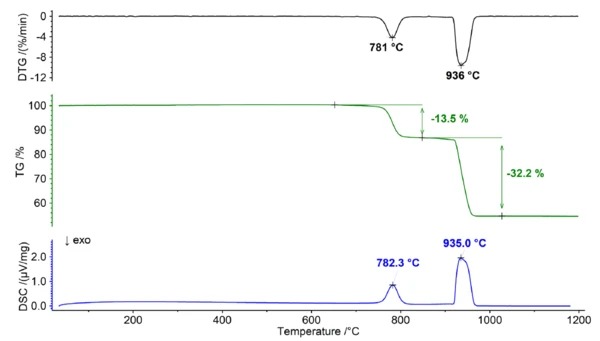
Durante questo processo di Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. decomposizione (vedi figura 1), la dolomite solida si scompone in ossido di calcio (CaO), ossido di magnesio (MgO) e anidride carbonica (CO2). Questa reazione avviene a temperature superiori a 700°C e dà luogo a un'ampia fase di perdita di massa che presenta più picchi nel segnale DTG e DSC. La caratteristica di sovrapposizione della perdita di massa ostacola significativamente la capacità di assegnare fasi distinte nella curva TGA, rendendo così impossibile determinare ulteriori informazioni sul rapporto Ca/Mg della dolomite.
Comportamento termico della dolomite in atmosfera di anidride carbonica
In presenza di un'atmosfera contenente biossido di carbonio, la dolomite presenta un comportamento diverso a causa della natura reversibile della Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. reazione di decomposizione e della diversa stabilità dei carbonati coinvolti. La Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. reazione di decomposizione (1) può anche essere rappresentata come due singole reazioni di equilibrio come segue:
MgCO3 → MgO +CO2 (2)
CaCO3 → CaO +CO2 (3)
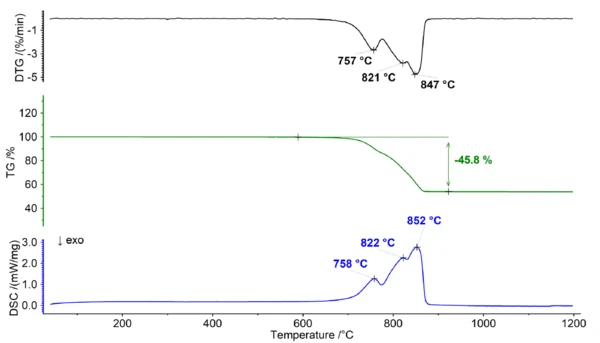
L'equilibrio tra i reagenti e i prodotti della reazione è influenzato da vari fattori, tra cui la temperatura e le concentrazioni diCO2. Quando l'anidride carbonica è presente in modo consistente, ha un impatto sull'equilibrio, causando uno spostamento verso la stabilizzazione dei carbonati e determinando una temperatura di Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. decomposizione più elevata. Questo effetto è più evidente per il carbonato di calcio che per il carbonato di magnesio, a causa della sua larger. energia di Gibbs di formazione. Di conseguenza, la Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. decomposizione del carbonato di calcio e del carbonato di magnesio può essere chiaramente distinta se misurata in un'atmosfera di anidride carbonica pura (vedi figura 2). Questa separazione offre l'opportunità di determinare con precisione il rapporto Ca/Mg della dolomite, poiché la fase iniziale può essere attribuita alla Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. decomposizione di MgCO3 (reazione 2), mentre la fase successiva corrisponde alla Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. decomposizione di CaCO3 (reazione 3).
Conclusione
Selectione dell'atmosfera ottimale influisce significativamente sulla qualità e sulla quantità di informazioni ottenibili attraverso le misure termoanalitiche. Un esempio di questo fenomeno è dato dall'analisi termica presentata di un campione di dolomite. In questo caso, il passaggio da un'atmosfera convenzionale di aria alla scelta leggermente più anticonvenzionale dell'anidride carbonica ha avuto un impatto notevole sulle proprietà termiche misurate della dolomite analizzata. Di conseguenza, sono diventate accessibili informazioni completamente nuove, come il rapporto Ca-Mg.