Introduzione
I siliconi, chiamati anche polisilossani, sono presenti ogni giorno senza che ce ne accorgiamo. Ad esempio, le gomme siliconiche proteggono l'elettronica delle automobili dall'umidità e dalla contaminazione, nelle lavatrici impediscono la formazione di schiuma, negli shampoo conferiscono ai capelli una lucentezza setosa e, sotto forma di pitture a base di resine siliconiche, mantengono la muratura idrorepellente e allo stesso tempo permeabile al vapore acqueo e all'anidride carbonica provenienti dall'interno. Ma i siliconi si trovano anche in altre applicazioni che richiedono un'elevata resistenza, come ad esempio nella tecnologia medica come materiale puro in tubi medici, tamponi per ferite o prodotti ortopedici, e nelle apparecchiature elettriche come materiali di tenuta e isolamento sicuri.
I siliconi sono molecole a catena lunga contenenti legami O-Si. A seconda della loro massa molecolare e del grado di indurimento, possono presentarsi come liquidi, gel o elastomeri [1, 2]. Questa ampia varietà di polisilossani è associata a proprietà molto diverse, per cui è importante caratterizzarli.
Parametri di misura DSC
La DSC è particolarmente adatta per analizzare il comportamento dei siliconi a basse temperature. Di seguito vengono determinate le proprietà termiche di un materiale siliconico. A tal fine, viene effettuata una misurazione DSC, come descritto nella tabella 1.
Tabella 1: Condizioni di misura
| Dispositivo | DSC 300 Caliris®, modulo P |
| Massa del campione | 8.75 mg |
| Crogiolo | Concavus® (alluminio) con coperchio forato |
| Intervallo di temperatura | -da 170°C a 100°C |
| Velocità di riscaldamento | 10 K/min |
| Atmosfera | Azoto (40 ml/min) |
Risultati della misurazione
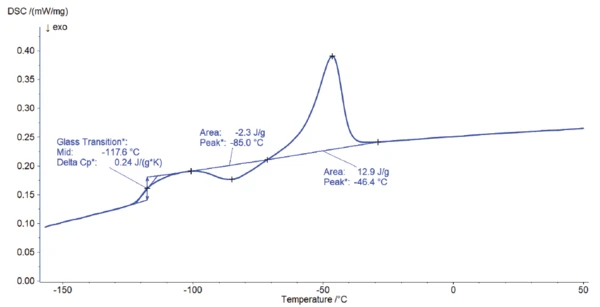
La Figura 1 mostra la curva DSC risultante. La fase endotermica rilevata a -117,6°C (punto centrale) è dovuta alla transizione vetrosa del materiale. È associato a una variazione dellaCapacità termica specifica (cp)La capacità termica è una grandezza fisica specifica del materiale, determinata dalla quantità di calore fornita al campione, divisa per l'aumento di temperatura risultante. La capacità termica specifica è correlata all'unità di massa del campione. capacità termica specifica di 0,24 J/(g-K). Tra -100°C e -30°C si verificano due effetti diversi. In primo luogo, il picco EsotermicoUna transizione campionaria o una reazione è esotermica se viene generato calore.esotermico si verifica a -85,0°C, che è un effetto post-CristallizzazioneLa cristallizzazione è il processo fisico di indurimento durante la formazione e la crescita dei cristalli. Durante questo processo viene rilasciato il calore di cristallizzazione.cristallizzazione. Questo si verifica al di sopra della temperatura di transizione vetrosa, quando le catene polimeriche sono in grado di muoversi liberamente e possono quindi cristallizzare. In secondo luogo, con l'aumento della temperatura, il picco EndotermicoUna transizione campionaria o una reazione è endotermica se per la conversione è necessario il calore.endotermico rilevato a -46,4°C rappresenta laTemperature di fusione ed entalpieL'entalpia di fusione di una sostanza, nota anche come calore latente, è una misura dell'apporto di energia, tipicamente calore, necessario per convertire una sostanza dallo stato solido a quello liquido. Il punto di fusione di una sostanza è la temperatura alla quale essa cambia stato da solido (cristallino) a liquido (fusione isotropa). fusione della fase cristallina.
Sintesi
Il silicone resiste bene alle alte temperature grazie alle sue proprietà materiali. Pertanto, può essere utilizzato per diverse applicazioni in un intervallo di temperature più ampio. Tuttavia, l'indagine DSC mostra che questi risultati sono fondamentali per il campo di applicazione di questo materiale a basse temperature: Il materiale si comporta in modo molto diverso a temperatura ambiente rispetto a una temperatura inferiore all'effetto diTemperature di fusione ed entalpieL'entalpia di fusione di una sostanza, nota anche come calore latente, è una misura dell'apporto di energia, tipicamente calore, necessario per convertire una sostanza dallo stato solido a quello liquido. Il punto di fusione di una sostanza è la temperatura alla quale essa cambia stato da solido (cristallino) a liquido (fusione isotropa). fusione o alla transizione vetrosa.