História de sucesso do cliente
Análise térmica no Instituto Max-Planck de Física Química de Sólidos em Dresden
A Case Study by Susann Scharsach and Dr. Marcus Schmidt about Thermal Analysis Systems Supporting the Synthesis and Crystal Growing at the Max Planck Institute.
arcA Max-Planck-Gesellschaft é o órgão responsável por um large número de instalações de pesquisa básica na Alemanha e no exterior. Com seus 84 institutos e instalações, é a organização de pesquisaarch mais bem-sucedida da Alemanha e o carro-chefe internacional da ciência alemã: Juntamente com cinco institutos no exterior, opera 20 Centros Max Planck com parceiros como a Universidade de Princeton, nos EUA, a Universidade Sciences Po, em Paris, na França, a University College London e a Universidade de Tóquio, no Japão.
arcOs Institutos Max-Planck conduzem pesquisas livres e independentes nos campos das ciências da vida, ciências naturais e humanas, muitas vezes em uma base interdisciplinar. Com 31 ganhadores do Prêmio Nobel, eles estão no mesmo nível das melhores e mais renomadas instituições de pesquisaarch do mundo.
Fonte: www.mpg.de

“NETZSCH os instrumentos de análise térmica dão suporte à síntese e ao crescimento de cristais no instituto. Em especial, o acoplamento Skimmer possibilita a identificação de gases facilmente condensáveis, como arsênico, telúrio ou vários vapores metálicos, mesmo em altas temperaturas.”
Instituto Max-Planck de Física Química de Sólidos em Dresden
arcO Instituto Max Planck de Física Química de Sólidos em Dresden(MPI CPfS) foi fundado em 1995 e inclui dois departamentos de pesquisa de orientação química e dois de orientação física, bem como vários grupos independentes de pesquisa Max Planckarch, com um total de 250 funcionários atualmente.

arcO instituto fornece descobertas por meio de pesquisas experimentais sobre fases intermetálicas e novas propriedades químicas, físicas e estruturais de substâncias com propriedades metálicas e semicondutoras. Por exemplo, são investigadas formas de magnetismo, supercondutividade ou transições metal-semicondutor. Com o desenvolvimento de métodos de síntese novos ou alternativos, os compostos são obtidos e posteriormente caracterizados em detalhes. As percepções sobre como a composição química e a estrutura cristalina estão relacionadas às propriedades físicas formam a base para a descoberta e a compreensão de novos fenômenos nos compostos sintetizados. Isso pode ser usado para desenvolver materiais e dispositivos.
MPI CPfS conta com soluções de NETZSCH
Um laboratório central de serviços para análise térmica está em funcionamento no instituto há mais de 20 anos. O conjunto de equipamentos inclui dois DSC 404 C Pegasus®, dois DSC 404 F1 Pegasus® , um STA 409, umacélulaDTA 404/7 e um STA 449 F3 Jupiter® . Um STA 449 CJupiter® é instalado em uma caixa de gás inerte da MBraun, enquanto um STA 409 CD, que é acoplado a um espectrômetro de massa QMG 422 por meio de um Skimmer, também é operado nessa caixa - uma solução desenvolvida para o instituto pelo NETZSCH em colaboração com a MBraun. Os dispositivos são equipados com fornos de platina, ródio, carbeto de silício ou grafite. Esses fornos abrangem uma faixa de temperatura que vai da temperatura ambiente até um máximo de 2.000°C. Ambas as atmosferas de gás inerte (argônio ou hélio) e os gases reativos - nitrogênio, oxigênio ou argônio/hidrogênio - estão disponíveis para medição. Amostras facilmente oxidáveis ou amostras em ampolas metálicas fechadas são geralmente medidas sob gás inerte. Portanto, ao instalar e operar os dispositivos, o foco está em uma baixa pressão parcial de oxigênio dentro do sistema de medição. Isso é obtido, entre outras formas, com o uso de um sistema OTS® em todos os dispositivos, com tubulações fixas (tubos de aço inoxidável) nos dispositivos e com a limpeza adicional dos gases inertes usados. As amostras que são particularmente sensíveis ao ar e/ou à umidade podem ser analisadas nos sistemas integrados em caixas de gás inerte.

Até 1.500 amostras por ano são analisadas em nosso laboratório de serviços. São analisados compostos de praticamente todos os elementos estáveis não radioativos, exceto gases nobres. O desafio específico na maioria dos casos é escolher o cadinho ou o material de ampola correto. Além dos diversos cadinhos oferecidos pelo site NETZSCH, muitas vezes são usadas ampolas de metal feitas de tântalo ou nióbio, que são fornecidas com incrustações de cerâmica feitas de Al2O3, Y2O3, ZrO2, AlN, BN ou carbono vítreo, entre outros. Essas ampolas foram desenvolvidas e fabricadas na oficina do instituto. As ampolas preenchidas com as substâncias a serem medidas são fechadas por solda em um forno elétrico arc.

Os sistemas de análise térmica dão suporte à síntese e ao crescimento de cristais no instituto, determinando as temperaturas de Temperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica). fusão e solidificação, as temperaturas de Transições de faseO termo transição de fase (ou mudança de fase) é mais comumente usado para descrever transições entre os estados sólido, líquido e gasoso.transição de fase e as temperaturas de reação, além de analisar o comportamento da Reação de decomposiçãoUma reação de decomposição é uma reação induzida termicamente de um composto químico que forma produtos sólidos e/ou gasosos. decomposição térmica. A Estabilidade térmicaUm material é termicamente estável se ele não se decompõe sob a influência da temperatura. Uma maneira de determinar a estabilidade térmica de uma substância é usar um TGA (analisador termogravimétrico). estabilidade térmica e a reatividade em diferentes atmosferas também são analisadas. O método analítico também é usado em colaboração com outros métodos para analisar diagramas de fase. Os dados termodinâmicos também podem ser determinados. Entender o comportamento térmico é fundamental para passar do composto ao material aplicável.
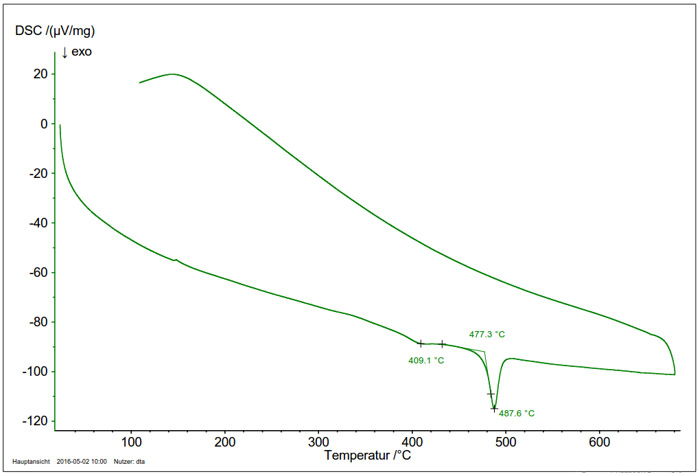
Figura 4: Medição DSC de uma fase de alta pressão Ca/Si (massa da amostra 1,5 mg). O sinal ExotérmicoUma transição de amostra ou uma reação é exotérmica se houver geração de calor.exotérmico na curva de aquecimento mostra a transformação da fase de alta pressão metaestável em sua forma termodinamicamente estável.

Combinação única de instrumentos
Skimmer Sistema de acoplamento com espectrômetro de massa quadrupolar e STA
O STA 409 CD, com seu fornoSKIMMER que permite o acoplamento direto ao espectrômetro de massa quadrupolo QMG 422, é um instrumento importante para analisar o comportamento da Reação de decomposiçãoUma reação de decomposição é uma reação induzida termicamente de um composto químico que forma produtos sólidos e/ou gasosos. decomposição térmica de compostos ou da fase gasosa que são liberados durante reações químicas. Ele pode ser usado para identificar espécies que são liberadas simultaneamente durante a Reação de decomposiçãoUma reação de decomposição é uma reação induzida termicamente de um composto químico que forma produtos sólidos e/ou gasosos. decomposição e não podem ser distinguidas usando o método "indireto" de termogravimetria, mas podem ser detectadas diretamente no espectrômetro de massa.
O sistema permite medições de até 1200°C e a detecção de espécies de gás de até 512 unidades de massa atômica. Em especial, o acoplamento Skimmer possibilita a identificação de gases facilmente condensáveis, como arsênico, telúrio ou vários vapores metálicos, mesmo em altas temperaturas.
Outra vantagem: Devido à sua alta sensibilidade, o espectrômetro de massa também pode detectar substâncias muito leves, como hidrogênio ou small quantidades de partículas de gás em VaporizaçãoA vaporização de um elemento ou composto é uma transição de fase do estado líquido para o vapor. Existem dois tipos de vaporização: evaporação e ebulição.vaporização, graças ao seu método de contagem física, que contrasta com o método de pesagem da termogravimetria.
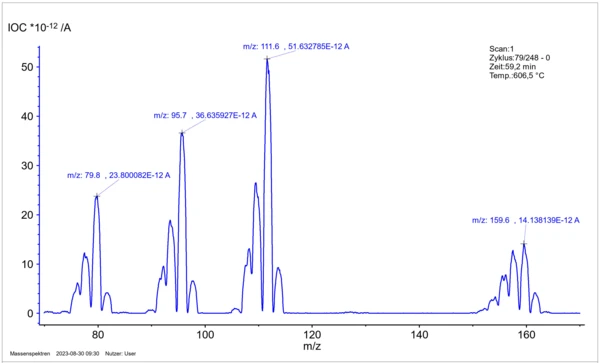
Figura 7: Espectro de massa da fase gasosa acima do Cu2OSeO3 a 606 °C para identificar as partículas de gás relevantes com base na massa e no padrão isotópico.
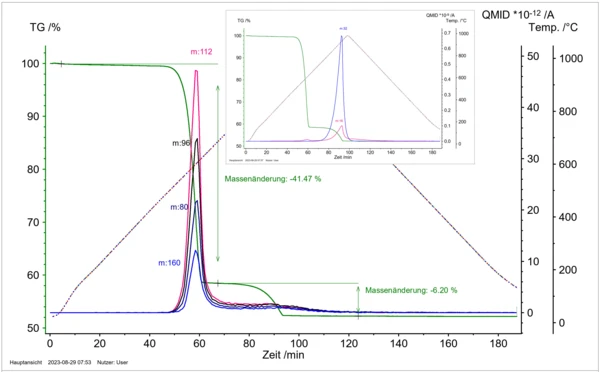
Figura 8: Perda de massa dependente da temperatura em correlação com as várias partículas de gás detectadas por espectrometria de massa: m/z 16 (O+), 32 (O2+), 80 (Se+), 96 (SeO+), 112 (SeO2+), 160 (Se2+) para a Reação de decomposiçãoUma reação de decomposição é uma reação induzida termicamente de um composto químico que forma produtos sólidos e/ou gasosos. decomposição térmica do Cu2OSeO3.
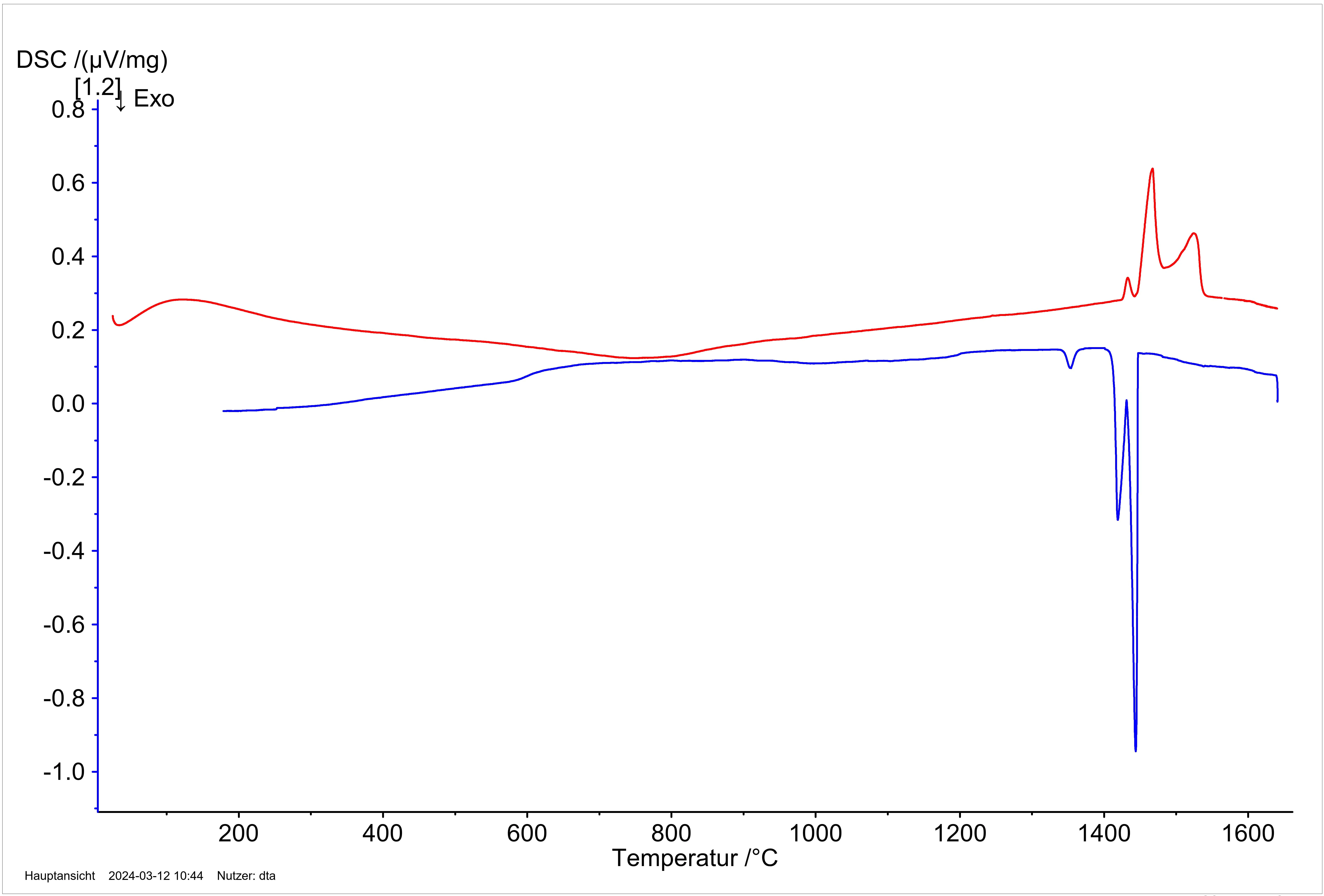
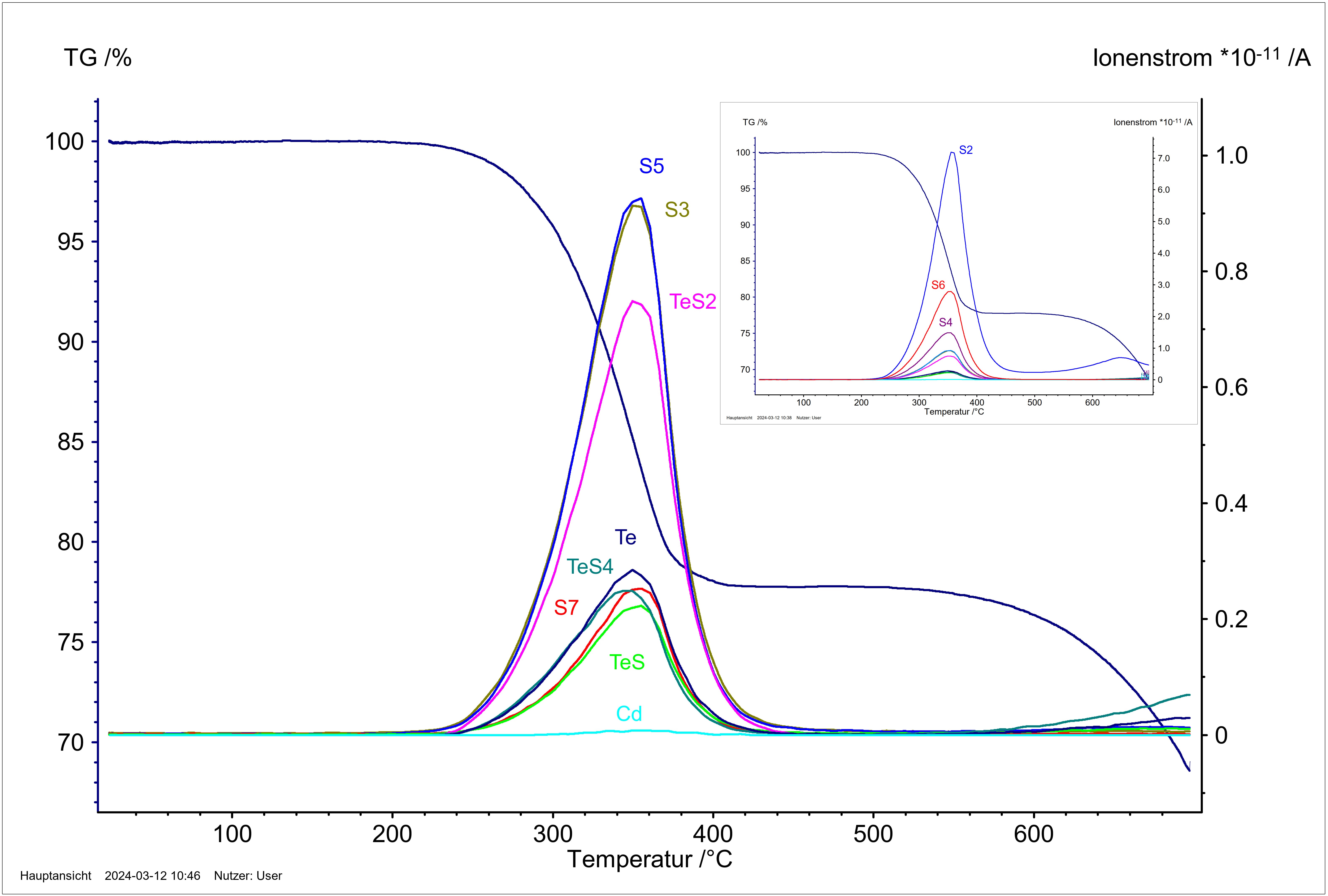
Figura 9: Perda de massa dependente da temperatura em correlação com as curvas de corrente iônica dos íons de fragmento S2+, S6+, S4+, S5+, S3+, TeS2+, Te+, S7+, TeS4+, TeS+ e Cd+. O CdTe sólido reage com o enxofre para formar o CdS sólido e liberar telúrio na fase gasosa, não sendo possível observar a evaporação do cádmio. O excesso de enxofre presente aumenta consideravelmente a volatilidade do telúrio por meio da formação de espécies de gás Te-S.
Trabalhamos com a NETZSCH há 25 anos. Durante esse tempo, temos nos beneficiado de um excelente atendimento ao cliente e de uma disposição constante para desenvolver soluções especiais para nosso instituto.
Susann Scharsach e Dr. Marcus Schmidt
arcMuito obrigado por compartilhar essas interessantes percepções sobre o seu trabalho. Estamos ansiosos para dar continuidade à nossa parceria.
Sobre os autores:
Marcus Schmidt, nascido em 1967, estudou química e concluiu seu doutorado na Universidade Técnica de Dresden sobre Investigações Termoquímicas de Haletos de Óxido de Bismuto.arcarcDesde 2000, ele é pesquisador associado do Max-Planck Institute for Chemical Physics of Solids em Dresden, onde seus tópicos de pesquisa incluem Reações sólido-gásAs reações sólido-gás são um tipo de reação heterogênea de estado sólido que ocorre quando um sólido reativo é exposto a um fluxo de gás reativo. Exemplos típicos de reações sólido-gás são a sorção e a corrosão de metais.reações sólido-gás, como a CristalizaçãoA cristalização é o processo físico de endurecimento durante a formação e o crescimento de cristais. Durante esse processo, o calor da cristalização é liberado.cristalização da fase gasosa e o comportamento termoquímico de materiais inorgânicos com foco na análise térmica. Ele é coautor da monografia "Chemische Transportreaktionen" (com M. Binnewies, R. Glaum, P. Schmidt).
Susann Scharsach, nascida em 1981, assistente técnica química qualificada, trabalha no Instituto Max-Planck de Física Química de Sólidos em Dresden desde 1999. Ela desempenhou um papel decisivo na configuração e no desenvolvimento do laboratório de análise térmica e contribuiu significativamente para a alta qualidade dos resultados da análise graças aos seus muitos anos de experiência.