Introdução
O diclofenaco é um medicamento anti-inflamatório com propriedades analgésicas e antipiréticas. Seu consumo pode causar problemas gastrointestinais, bem como dor de cabeça ou aumento da pressão arterial. Efeitos colaterais graves podem ocorrer se esse medicamento for tomado a longo prazo. Nos medicamentos, o diclofenaco está disponível na forma de, por exemplo, sal de sódio ou de potássio. [2] A degradação do diclofenaco de sódio foi investigada por meio de TGA acoplado a FT-IR e será discutida a seguir.
Resultados do teste
11.12 mg de diclofenaco de sódio foram preparados em um cadinho de óxido de alumínio e colocados no TG 209 F1 Libra® . A amostra foi aquecida a 600°C a uma taxa controlada de 10 K/min sob uma atmosfera dinâmica de nitrogênio (40 ml/min). Os gases que evoluíram durante o aquecimento foram injetados diretamente no espectrômetro FT-IR por meio do acoplamento PERSEUS®.
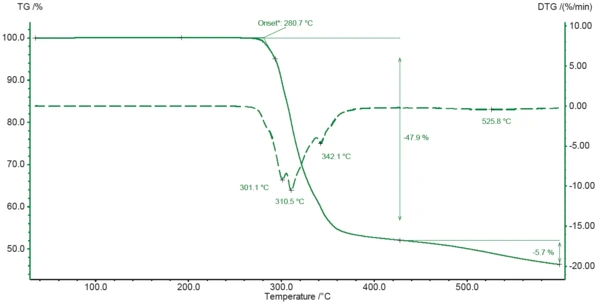
A curva de TGA do diclofenaco de sódio durante o aquecimento a 600°C é mostrada na Figura 2. A degradação da amostra começa a 281°C (início extrapolado da curva TGA) e leva a uma perda de massa inicial de 48% entre a temperatura ambiente e 425°C. Pode-se concluir, a partir dos mínimos na curva DTG, que o processo é executado em diferentes etapas sucessivas (301°C, 311°C e 342°C). A degradação continua até o final da medição com outra perda de massa de 6% entre 425°C e 600°C.
Para compreender melhor o mecanismo de degradação, os gases liberados durante o aquecimento foram analisados por FT-IR. O gráfico 3D da figura 3 mostra a perda de massa (curva vermelha), bem como os espectros FT-IR dos gases liberados durante o aquecimento (apresentação tridimensional).
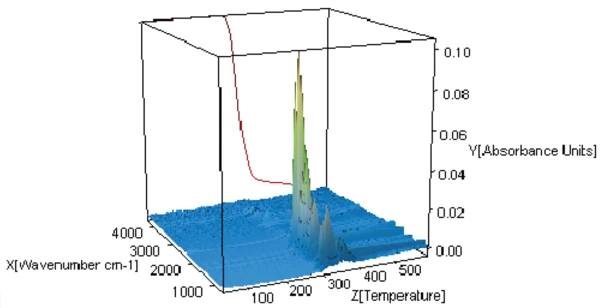
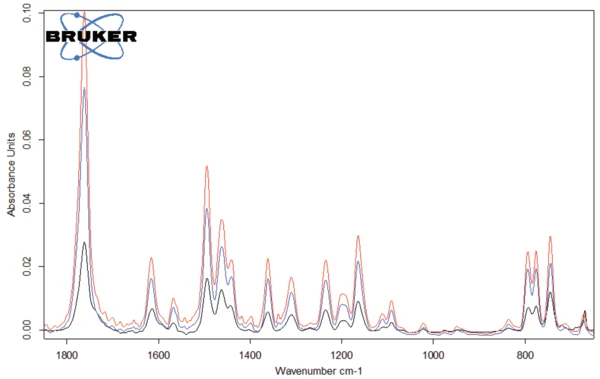
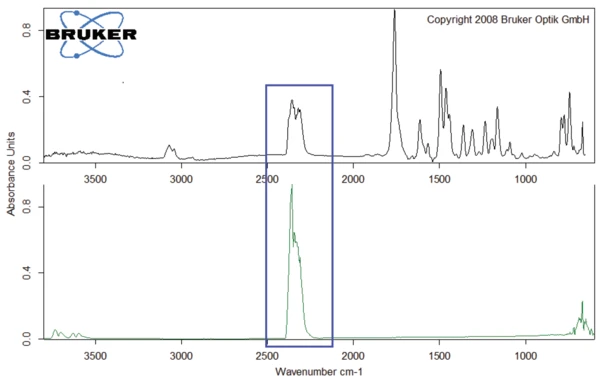
Os espectros dos gases liberados a 301°C, 311°C e 343°C estão representados nas figuras 4 e 5. Pode-se ver claramente que esses três espectros diferem apenas na intensidade das bandas, ou melhor, na concentração dos produtos liberados: Há um aumento contínuo no início da degradação (curvas azul e vermelha) antes de ocorrer uma diminuição (curva preta). A única exceção a isso são as bandas entre 2300 e 2400 cm-1, indicando a liberação deCO2 a 343°C (consulte a Figura 6).
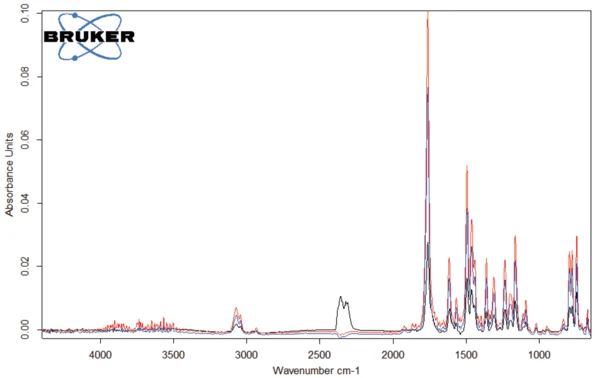
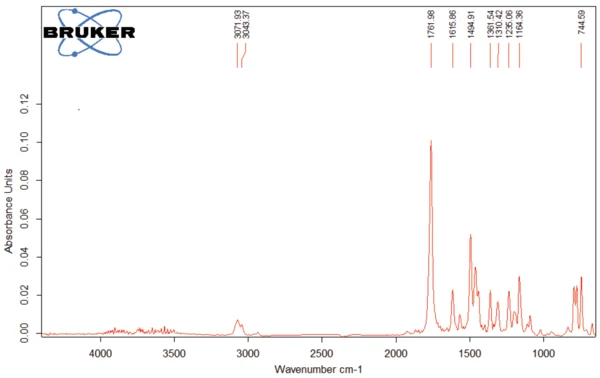
O espectro dos produtos liberados a 311°C (curvas vermelhas nas figuras 4 e 5) é apresentado na figura 7. As bandas acima de 3000 cm-1 resultam de vibrações de estiramento =C-H. A banda em 1761 cm-1 é típica de ligações C=O, enquanto a banda em 1462 cm-1 indica a presença de ligações -C-H nos gases liberados. As bandas em torno de 1500 cm-1 denotam a volatilização de grupos amina e amida. As outras bandas detectadas são causadas por grupos funcionais contendo grupos aromáticos e cloro.
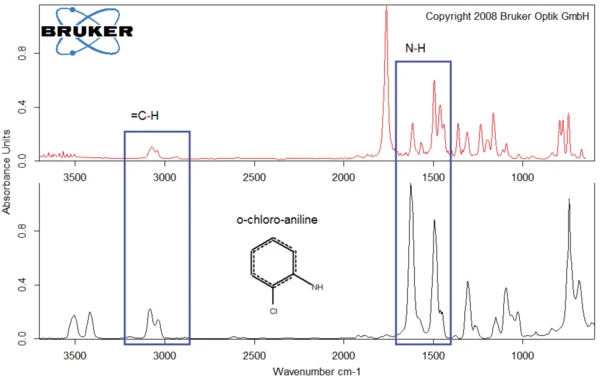
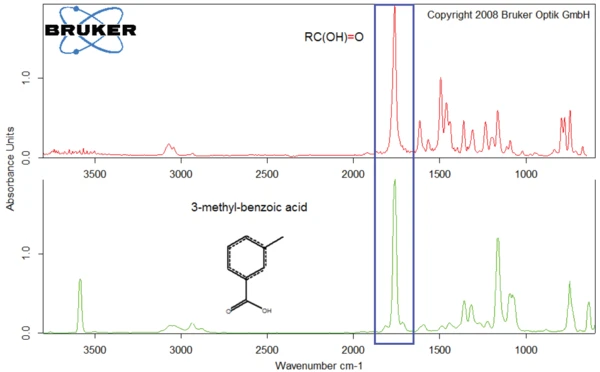
Como exemplo, as figuras 8 e 9 comparam os produtos liberados pelo diclofenaco de sódio a 311°C com os espectros da o-cloroanilina (figura 8) e do ácido 3-metil-benzoico (figura 9).
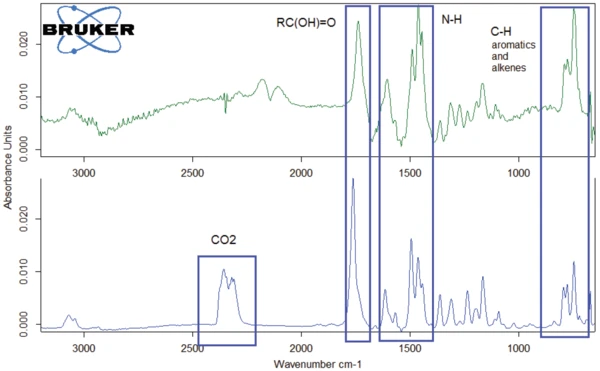
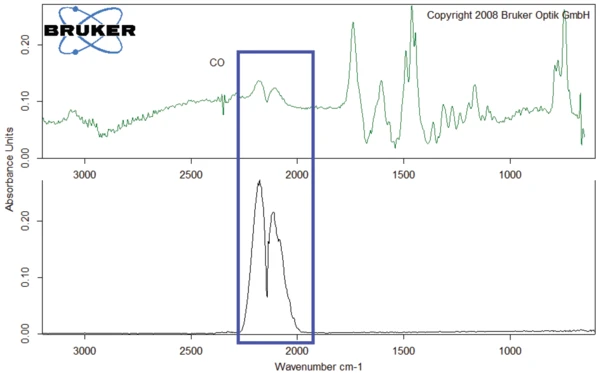
O espectro FT-IR dos gases liberados a 526°C é apresentado na figura 10 (curva verde escura), juntamente com o espectro dos gases liberados a 343°C (curva azul). As curvas apresentam semelhanças entre si. A principal diferença é o pico deCO2 que ocorre somente no espectro a 343°C. Em contraste, o monóxido de carbono foi detectado somente no espectro a 526°C (veja também a figura 11).
Conclusão
Apesar da facilidade com que as medições de TGA-FT-IR podem ser manipuladas, o método fornece muitas informações de uma só vez, como a forma como a degradação ocorre, a temperatura em que ela começa e os tipos de substâncias liberadas durante o processo. Isso torna o FT-IR uma tecnologia poderosa capaz de caracterizar a estabilidade e a composição de produtos farmacêuticos.