Introduzione
Il diclofenac è un farmaco antinfiammatorio con proprietà analgesiche e antipiretiche. Il suo consumo può provocare disturbi gastrointestinali, mal di testa o aumento della pressione sanguigna. Se il farmaco viene assunto a lungo termine, possono verificarsi pesanti effetti collaterali. Nei farmaci, il diclofenac è disponibile sotto forma, ad esempio, di sale di sodio o di potassio. [2] La degradazione del diclofenac sodico è stata studiata mediante TGA accoppiata a FT-IR e sarà discussa di seguito.
Risultati del test
11.12 mg di diclofenac sodico sono stati preparati in un crogiolo di ossido di alluminio e posti nel TG 209 F1 Libra® . Il campione è stato riscaldato a 600°C a una velocità controllata di 10 K/min in un'atmosfera dinamica di azoto (40 ml/min). I gas evoluti durante il riscaldamento sono stati iniettati direttamente nello spettrometro FT-IR tramite l'accoppiamento PERSEUS®.
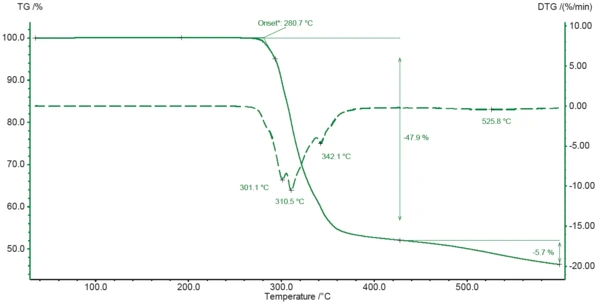
La curva TGA del diclofenac sodico durante il riscaldamento a 600°C è illustrata nella Figura 2. La degradazione del campione inizia a 600°C. La degradazione del campione inizia a 281°C (inizio estrapolato della curva TGA) e porta a una perdita iniziale di massa del 48% tra la temperatura ambiente e i 425°C. Dai minimi della curva DTG si può concludere che il processo si svolge in diverse fasi successive (301°C, 311°C e 342°C). La degradazione continua fino alla fine della misurazione con un'ulteriore perdita di massa del 6% tra 425°C e 600°C.
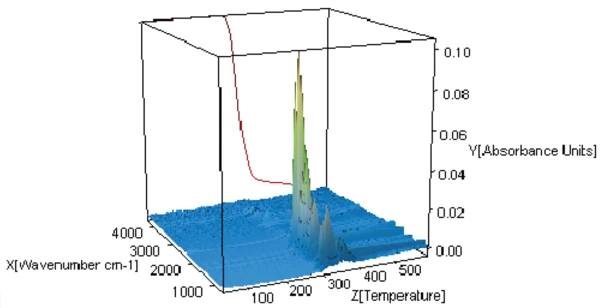
Per comprendere meglio il meccanismo di degradazione, i gas rilasciati durante il riscaldamento sono stati analizzati mediante FT-IR. Il grafico 3-D della figura 3 mostra la perdita di massa (curva rossa) e gli spettri FT-IR dei gas rilasciati durante il riscaldamento (presentazione tridimensionale).
Gli spettri dei gas rilasciati a 301°C, 311°C e 343°C sono rappresentati nelle figure 4 e 5. Si può chiaramente notare che questi tre spettri differiscono solo per l'intensità delle bande, o meglio per la concentrazione dei prodotti rilasciati: Si osserva un aumento continuo all'inizio della degradazione (curve blu e rosse) prima che si verifichi una diminuzione (curva nera). L'unica eccezione è rappresentata dalle bande tra 2300 e 2400 cm-1, che indicano il rilascio diCO2 a 343°C (vedi figura 6).
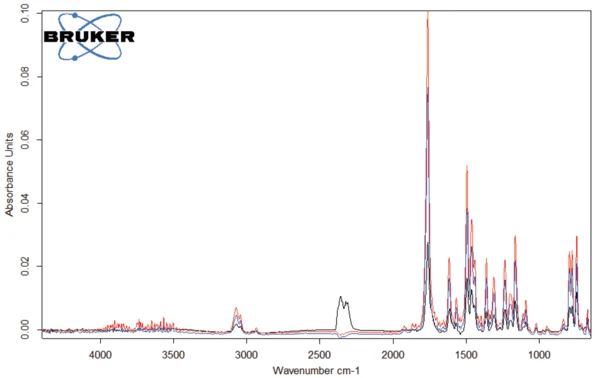
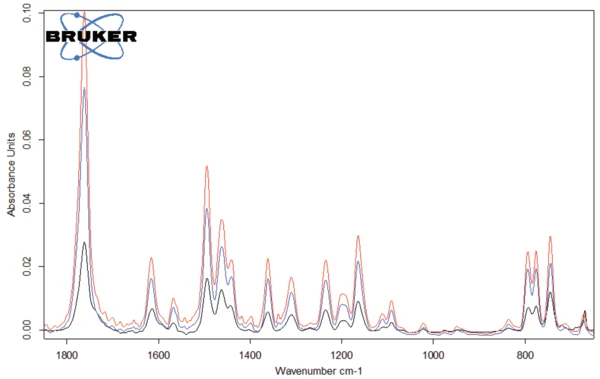
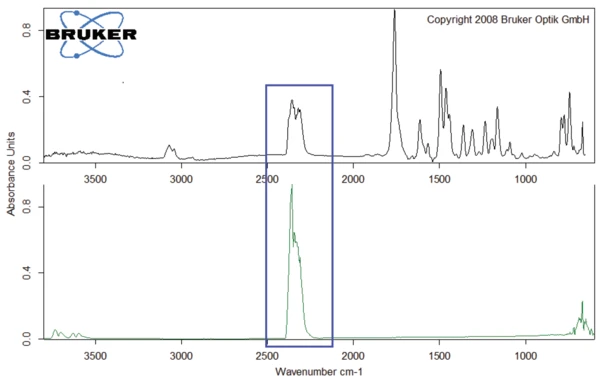
Lo spettro dei prodotti rilasciati a 311°C (curve rosse nelle figure 4 e 5) è riportato nella figura 7. Le bande oltre i 3000 cm-1 derivano da VibrazioniUn processo meccanico di oscillazione è chiamato vibrazione. La vibrazione è un fenomeno meccanico in cui si verificano oscillazioni intorno a un punto di equilibrio. In molti casi, le vibrazioni sono indesiderate, perché sprecano energia e creano suoni indesiderati. Ad esempio, i movimenti vibratori dei motori, dei motori elettrici o di qualsiasi dispositivo meccanico in funzione sono tipicamente indesiderati. Tali vibrazioni possono essere causate da squilibri nelle parti rotanti, da attriti non uniformi o dall'ingranamento dei denti degli ingranaggi. In genere, una progettazione accurata riduce al minimo le vibrazioni indesiderate.vibrazioni di stiramento =C-H. La banda a 1761 cm-1 è tipica dei legami C=O, mentre la banda a 1462 cm-1 indica la presenza di legami -C-H nei gas rilasciati. Le bande intorno ai 1500 cm-1 denotano la volatilizzazione di gruppi amminici e ammidici. Le altre bande rilevate sono dovute a gruppi funzionali contenenti gruppi aromatici e cloro.
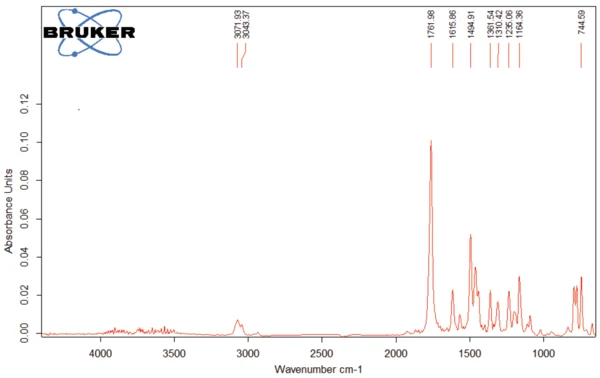
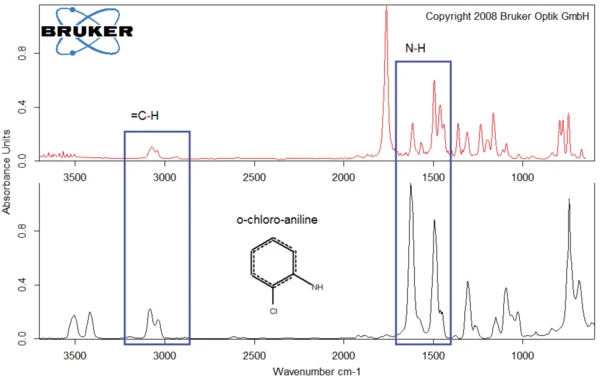
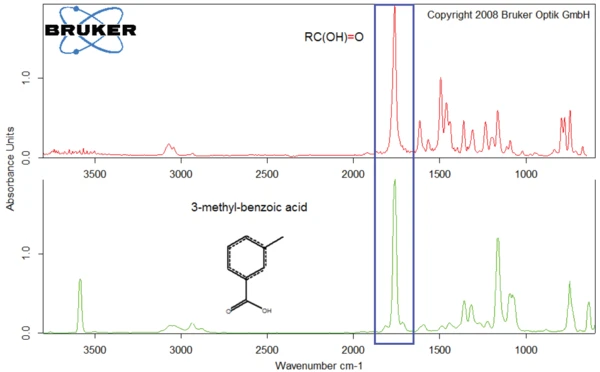
A titolo di esempio, le figure 8 e 9 confrontano i prodotti rilasciati dal diclofenac sodico a 311°C con gli spettri dell'o-cloroanilina (figura 8) e dell'acido 3-metil-benzoico (figura 9).
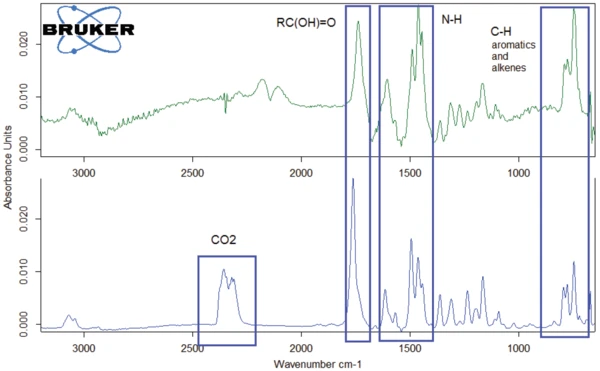
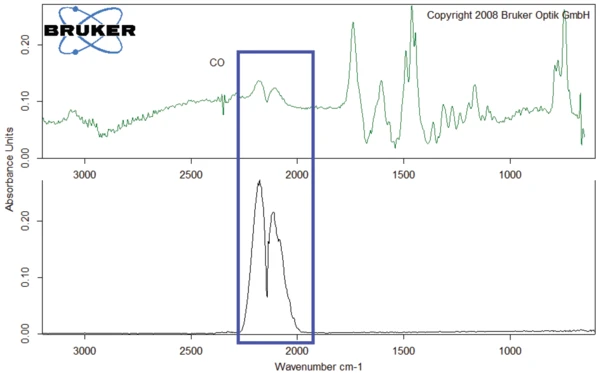
Lo spettro FT-IR dei gas rilasciati a 526°C è riportato nella figura 10 (curva verde scuro) insieme allo spettro dei gas rilasciati a 343°C (curva blu). Le curve sono simili tra loro. La differenza principale è il picco dellaCO2 che si presenta solo nello spettro a 343°C. Al contrario, il monossido di carbonio è stato rilevato solo nello spettro a 526°C (si veda anche la figura 11).
Conclusione
Nonostante la facilità con cui le misure TGA-FT-IR possono essere gestite, il metodo fornisce molte informazioni tutte insieme, come ad esempio il modo in cui avviene la degradazione, la temperatura a cui inizia e quali tipi di sostanze vengono rilasciate durante il processo. Ciò rende l'FT-IR una tecnologia potente in grado di caratterizzare la stabilità e la composizione dei prodotti farmaceutici.