Introduzione
In farmacia, non c'è quasi nessun principio attivo di cui si sia scritto di più dell'acido acetilsalicilico (o ASA in breve; nei paesi di lingua inglese e tedesca, il nome del marchio Aspirin™ è spesso usato come sinonimo). La sua storia di successo è iniziata alla fine del XIX secolo, quando il Dr. Felix Hoffmann sintetizzò per la prima volta la sostanza nei laboratori BAYER senza impurità. Oggi è ancora uno dei farmaci più popolari, utilizzato in un ampio spettro terapeutico. Appartiene al gruppo dei farmaci antinfiammatori non steroidei (FANS) ed è indicato per il trattamento del dolore, della febbre e delle infiammazioni. Inoltre, viene utilizzato per prevenire le recidive di infarto o ictus in pazienti ad alto rischio. Nel 1977, l'ASA è stato aggiunto come analgesico alla "lista dei farmaci essenziali" dell'OMS (Organizzazione Mondiale della Sanità). [1]
Questa è l'ultima di quattro note applicative che esaminano più dettagliatamente il comportamento termico dell'acido acetilsalicilico; le prime tre hanno affrontato la Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. decomposizione in diverse atmosfere gassose, la cinetica di Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. decomposizione e le specie gassose risultanti [2, 3, 4].
Sperimentale
Per studiare la Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. decomposizione termica dell'acido acetilsalicilico, sono state eseguite misure termogravimetriche (TGA) con il sistema NETZSCH TG 209 Libra® in atmosfera di elio. Per un'interpretazione di supporto, l'analizzatore termico è stato accoppiato con uno spettrometro di massa a quadrupolo 403 Aëolos®. Le condizioni esatte di misurazione sono riportate nella tabella 1.
Tabella 1: Parametri di misura
| Parametro | Acido acetilsalicilico |
|---|---|
| Analizzatore | TG 209 Libra® con QMS 403 Aëolos® |
| Portacampioni | TGA, tipo S |
| Crogiolo | Al2O3, 85 μl, aperto |
| Massa del campione | 8.35 mg |
| Programma di temperatura | Da RT a 500°C, velocità di riscaldamento: 10 K/min |
| Atmosfera | Elio* (100 ml/min) |
*In questo lavoro, un'atmosfera di elio era in linea con le misurazioni incluse nelle precedenti Note applicative 208, 209 e 210 (parte 1 a 3).
Risultati delle misure e discussione
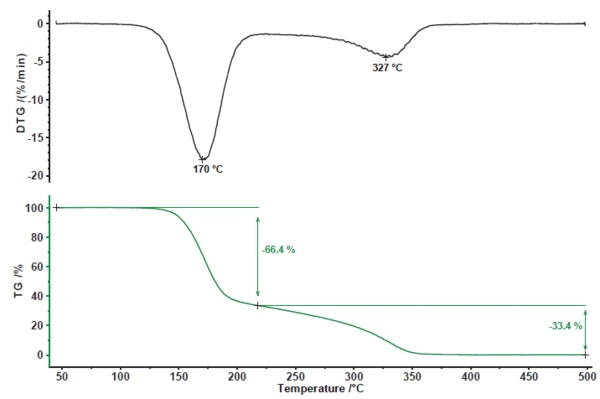
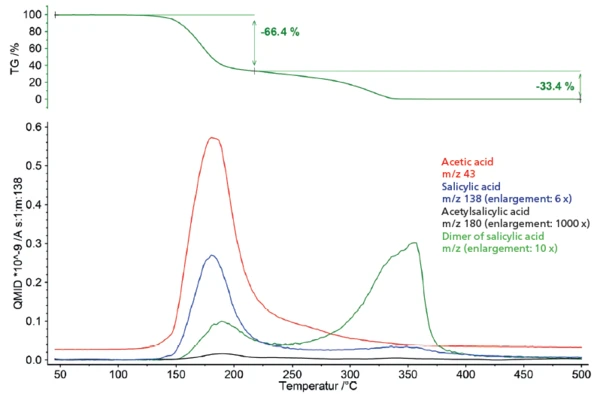
La PirolisiLa pirolisi è la decomposizione termica di composti organici in atmosfera inerte.pirolisi dell'acido acetilsalicilico presenta due fasi di perdita di massa (figura 1). La prima fase di perdita di massa, pari al 66,4%, è associata a un picco del tasso di perdita di massa (DTG) a 170°C. La seconda fase di perdita di massa ammonta al 33,4% con un picco nella curva DTG a 327°C.
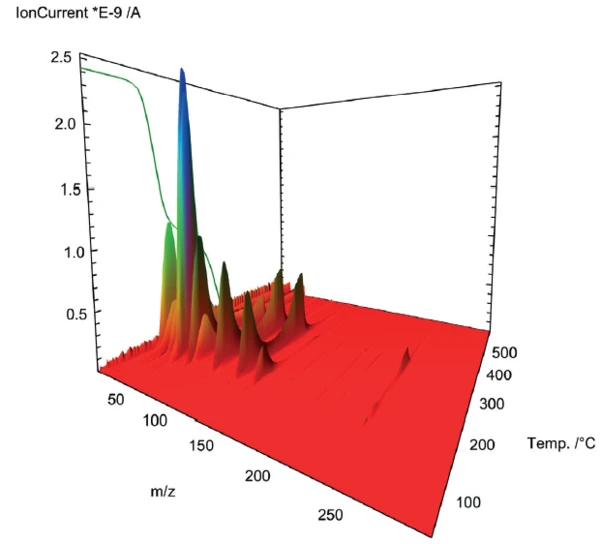
L'accoppiamento dello spettrometro di massa utilizzato per approfondire la PirolisiLa pirolisi è la decomposizione termica di composti organici in atmosfera inerte.pirolisi dell'acido acetilsalicilico mostra un profilo complesso per il degassamento nelle due fasi di perdita di massa (figura 2). Per un esame più approfondito, gli spettri di massa delle rispettive fasi sono stati estratti e sottoposti a un confronto con il database "NIST MS Library".
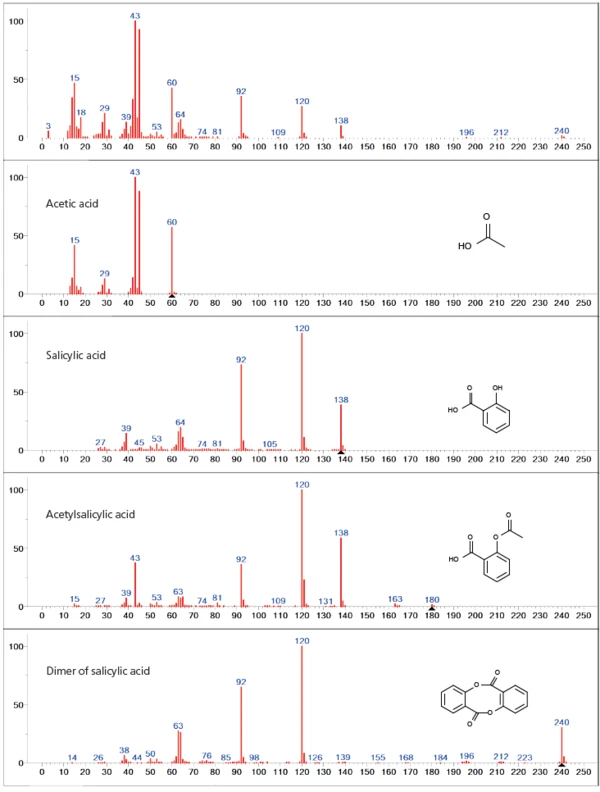
L'analisi del database della prima fase di perdita di massa mostra principalmente una sovrapposizione di rilascio di acido acetilico e acido salicilico, indicando la degradazione della funzionalità acetilica dell'acido acetilsalicilico (figura 3). Oltre ai due prodotti principali di degassamento, nello spettro sono rappresentati anche numeri di massa più elevati (> 138 u), che possono essere attribuiti al dimero dell'acido salicilico. Inoltre, non si può escludere l'evaporazione parziale dell'acido acetilsalicilico non decomposto durante la prima fase di perdita di massa, poiché tutte le masse principali dello spettro dell'acido acetilsalicilico (43, 60, 92, 120, 138 u) sono sovrapposte ai prodotti di Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. decomposizione precedentemente menzionati.
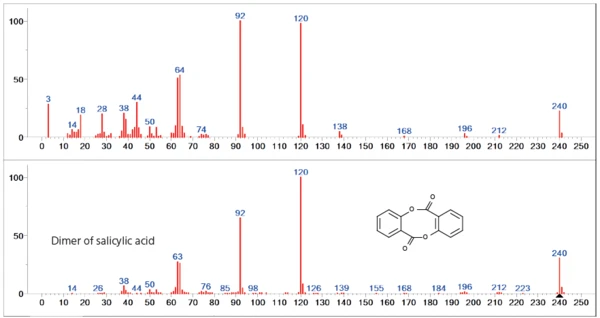
La seconda fase di perdita di massa è dominata principalmente dal rilascio del dimero dell'acido salicilico. Soprattutto nell'intervallo di massa inferiore (< 60u), tuttavia, si notano differenze rispetto allo spettro del database, che indicano il rilascio di specie gassose aggiuntive (figura 4).
Grazie ai prodotti di degassamento rilevati, è possibile ottenere una visione del comportamento del degassamento in funzione della temperatura. A tal fine, i numeri di massa specifici dei singoli prodotti di degassamento sono stati selecte tracciati rispetto alla curva di perdita di massa (figura 5). La corrispondente presentazione illustra la sovrapposizione della degradazione termica dell'acido acetilsalicilico e l'evaporazione dell'acido salicilico formatosi come prodotto di Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. decomposizione nella prima fase di perdita di massa. Risulta inoltre evidente che la formazione e l'evaporazione degli oligomeri dell'acido salicilico inizia già nello stesso intervallo di temperatura ed è il processo di degradazione dominante nel corso della temperatura successiva.
Sintesi
La combinazione di termogravimetria e spettrometria di massa è uno strumento potente per ottenere una visione approfondita dei processi di Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. decomposizione termica e dei gas rilasciati. L'accoppiamento con uno spettrometro di massa consente di ottenere una panoramica dei prodotti di degassamento dipendenti dalla temperatura, con una qualità simile a quella del metodo di combinazione della termogravimetria con la spettroscopia infrarossa. Tuttavia, grazie al carattere più specifico degli spettri di massa, l'accoppiamento con uno spettrometro di massa consente di trarre conclusioni più precise sulle specie gassose rilasciate.
In sintesi, la Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. decomposizione termica dell'acido acetilsalicilico in atmosfera di elio avviene in un processo a due fasi composto dalla separazione della funzionalità acetilica e dal rilascio associato di acido acetico, nonché dall'evaporazione dell'acido salicilico in forma oligomerica (ad esempio, dimero). Una visione gas-analitica delle rispettive fasi di perdita di massa ha evidenziato una parziale sovrapposizione dei due processi a causa del rilascio simultaneo di acido acetico e salicilico nella prima fase di perdita di massa.
L'analisi dettagliata degli spettri MS ottenuti suggerisce che non tutti i prodotti di degassamento sono accessibili mediante l'accoppiamento diretto della TGA a uno spettrometro di massa. Pertanto, soprattutto nella seconda fase di perdita, è stato possibile assegnare chiaramente solo una parte dei numeri di massa osservati. Tuttavia, la combinazione di gascromatografia e spettrometria di massa (GC-MS), come già mostrato nella parte 3 di questa serie di note applicative, presenta una metodologia di accoppiamento ancora più specializzata, sviluppata in particolare per questo tipo di attività [4].