
09.05.2022 by Aileen Sammler
Jak DSC pomaga w charakteryzowaniu aktywnych składników farmaceutycznych
W celu leczenia chorób, przemysł farmaceutyczny nieustannie dąży do badań nad nowymi składnikami farmaceutycznymi (API). Dr Carsten Schauerte z SOLID-CHEM GmbH pokaże, w jaki sposób DSC może pomóc w charakteryzowaniu aktywnych składników farmaceutycznych.
Dr Carsten Schauerte jest współzałożycielem i dyrektorem zarządzającym SOLID-CHEM GmbH w Centrum Biomedycznym w Bochum w Niemczech. Ukończył studia chemiczne na Uniwersytecie w Essen, uzyskał tytuł doktora w 2004 r. i pracował jako postdoc na Uniwersytecie Goethego we Frankfurcie nad Menem.
W firmie SOLID-CHEM GmbH, założonej w 2010 r., koncentruje się na analizie i opracowywaniu metod krystalizacji, polimorfów, soli i współkryształów, a także amorficznych "badań przesiewowych" oraz identyfikacji i charakteryzacji cząstek. SOLID-CHEM oferuje dodatkowo szeroki zakres metod analitycznych do analizy usieciowanego ciała stałego.

Dziś dr Carsten Schauerte wyjaśnia, w jaki sposób DSC wspomaga charakteryzację aktywnych składników farmaceutycznych:
W celu leczenia chorób, przemysł farmaceutyczny nieustannie poszukujearch nowych składników farmaceutycznych (API) o specyficznych, określonych właściwościach fizykochemicznych, takich jak zdolność do dokowania do białek receptorowych, a tym samym wywoływania pożądanych reakcji komórkowych. Po znalezieniu aktywnego farmaceutyku wyzwaniem jest sprawienie, by był on wchłaniany przez organizm. Kluczowym terminem jest tutaj rozpuszczalność. Ponadto, aktywny składnik musi być następnie wprowadzony do odpowiedniej postaci dawkowania, np. tabletki, kapsułki lub roztworu. Formuła leku zwykle zawiera również substancje pomocnicze, które pełnią takie funkcje, jak wywieranie pozytywnego wpływu na rozpuszczalność lub stabilność. Charakterystyka materiału odgrywa ważną rolę na tym etapie. Spośród szerokiej gamy struktur stałych (polimorfów, hydratów, solwatów i materiałów amorficznych) należy zidentyfikować te, które gwarantują biodostępność i bezpieczeństwo produktu.
Różne uzupełniające się metody analityczne są często wykorzystywane do charakterystyki odpowiedniej postaci ciała stałego. Właściwości termiczne składników aktywnych, substancji pomocniczych i preparatów można wykryć za pomocą DSC. Obejmuje to określenie temperatury topnienia i ogólnych przemian fazowych, np. poprzez sygnały endotermiczne w DSC.
Polimorfizm substancji krystalicznych - ważny dla skuteczności leków
Wiele substancji krystalicznych może tworzyć polimorfy. Polimorfy to związki o tym samym składzie chemicznym, charakteryzujące się innym rozmieszczeniem cząsteczek wewnątrz kryształów w stanie stałym. Różne formy polimorficzne mogą być generowane poprzez ustawienie różnych parametrów podczas procesu krystalizacji ze stopu lub roztworu. Mogą one również powstawać w wyniku przemian fazowych ciało stałe-ciało stałe. Może im sprzyjać wilgotność lub różne ciśnienia, ale w szczególności pewne temperatury lub gradienty temperatury. Różnice na poziomie molekularnym między polimorfami mogą również powodować różnice na poziomie makroskopowym. Polimorfy mogą zatem wykazywać różne właściwości fizyczne w swoich różnych formach krystalicznych. Obejmują one między innymi różną rozpuszczalność, a tym samym prawdopodobnie zmienioną biodostępność.
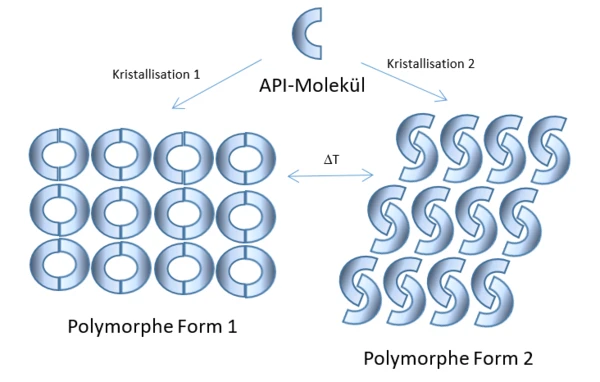
Znalezienie stabilnego polimorfu o pożądanej skuteczności jest jednak bardzo czasochłonne. Nawet jeśli uda się znaleźć obiecującą substancję, tylko jeden z wielu tysięcy aktywnych składników "przetrwa" fazę testów i stanie się lekiem dostępnym na rynku. Takie obiecujące składniki aktywne są zatem również patentowane przez firmy farmaceutyczne, aby zagwarantować wyłączność na rynku.
Analiza jako pomocne narzędzie do rozwiązywania problemów w produkcji leków
Dogłębne badania laboratoryjne dostarczają informacji na temat optymalnych parametrów przetwarzania dla każdej formy polimorficznej, takich jak rozpuszczalność, preferowany rozpuszczalnik krystalizacyjny, zoptymalizowane stężenia w mieszanych układach rozpuszczalników, warunki krystalizacji i inne. Jeśli jednak lek nie wykazuje pożądanej skuteczności w użyciu, konieczne jest wyjaśnienie, w którym momencie przetwarzania lub przygotowania występują problemy. Być może substancja czynna przeszła do innej formy polimorficznej w wyniku procesu produkcyjnego lub niepożądanej interakcji z substancjami pomocniczymi, a może problem jest spowodowany zanieczyszczeniem produktu? W takich przypadkach firmy farmaceutyczne często korzystają z pomocy wyspecjalizowanych laboratoriów kontraktowych, takich jak SOLID-CHEM GmbH w Bochum w Niemczech. W ich wewnętrznym laboratorium dostępne są wszechstronne metody analityczne, takie jak dyfrakcja rentgenowska i laserowa, spektroskopia wibracyjna i magnetycznego rezonansu jądrowego oraz mikroskopia, a także analiza termiczna z termograwimetrią i różnicową kalorymetrią skaningową za pomocą NETZSCH DSC 204 F1 Phoenix®.
Jak może pomóc analiza termiczna?
Analiza termiczna obejmuje szereg metod. Jedną z nich jest różnicowa kalorymetria skaningowa (DSC), stosowana do testowania, czy w materiale zachodzą przemiany fazowe lub reakcje chemiczne. W tym celu próbka jest poddawana określonemu programowi temperaturowemu, tj. temperatura próbki jest zwiększana lub zmniejszana w określonym tempie lub pozostawiana na stałym poziomie przez określony czas. Mierzone jest ciepło zaadsorbowane (egzotermiczne) lub zaabsorbowane (endotermiczne). Pozwala to na wyciągnięcie wniosków na temat procesów chemicznych i fizycznych, takich jak Temperatury i entalpie topnieniaEntalpia syntezy substancji, znana również jako ciepło utajone, jest miarą nakładu energii, zazwyczaj ciepła, która jest niezbędna do przekształcenia substancji ze stanu stałego w ciekły. Temperatura topnienia substancji to temperatura, w której zmienia ona stan ze stałego (krystalicznego) na ciekły (stopiony izotropowo). topnienie, KrystalizacjaKrystalizacja to fizyczny proces twardnienia podczas tworzenia i wzrostu kryształów. Podczas tego procesu uwalniane jest ciepło krystalizacji.krystalizacja lub przemiany polimorficzne.
Występowanie i rozpoznawanie form polimorficznych na przykładzie paracetamolu
Znane są trzy polimorfy aktywnego składnika paracetamolu, powszechnie stosowanego środka przeciwbólowego:
- Stabilna forma I (jednoskośna)
- Metastabilna forma II (ortorombowa) i
- Niestabilna forma III
Różne formy polimorficzne można dobrze rozróżnić za pomocą analizy DSC.
W poniższym przykładzie 2,4 mg paracetamolu ogrzewano dwukrotnie od -20°C do 200°C w atmosferze azotu w aluminiowych tyglach. Segment chłodzenia w międzyczasie również przeprowadzono z prędkością 10 K/min. Podczas pierwszego ogrzewania można zaobserwować efekt EndotermicznyPrzemiana próbki lub reakcja jest endotermiczna, jeśli do konwersji potrzebne jest ciepło.endotermiczny z ekstrapolowaną temperaturą początkową 169°C. Dobrze koreluje to z temperaturą topnienia formy I. Podczas kolejnego etapu kontrolowanego chłodzenia (nie pokazanego tutaj) nie zachodzi KrystalizacjaKrystalizacja to fizyczny proces twardnienia podczas tworzenia i wzrostu kryształów. Podczas tego procesu uwalniane jest ciepło krystalizacji.krystalizacja. Oznacza to, że paracetamol jest nadal amorficzny na początkudrugiego etapu ogrzewania. Podczasdrugiego etapu ogrzewania najpierw następuje Punkt przecięciaW teście reologicznym, takim jak przemiatanie częstotliwości lub przemiatanie czas/temperatura, punkt przecięcia jest wygodnym punktem odniesienia wskazującym punkt "przejścia" próbki. przejście szkliste (small krok w kierunku endotermicznym) jako cecha charakterystyczna stanu amorficznego, a następnie efekt EgzotermicznyPrzejście próbki lub reakcja jest egzotermiczna, jeśli generowane jest ciepło.egzotermiczny (z temperaturą szczytową 82°C) związany z procesem zimnej lub postkrystalizacji. Równoległe badania XRD wykazały, że powstaje tutaj forma III. Ta forma III przekształca się w formę II po dalszym ogrzewaniu (również potwierdzonym badaniami XRD), która ostatecznie topi się w temperaturze 157°C (ekstrapolowana temperatura początku). Efekt EgzotermicznyPrzejście próbki lub reakcja jest egzotermiczna, jeśli generowane jest ciepło.egzotermiczny w 133°C (temperatura szczytowa) wynika z transformacji strukturalnej w inną formę polimorficzną. Ekstrapolowana temperatura początkowa 157°C jest charakterystyczna dla formy II.
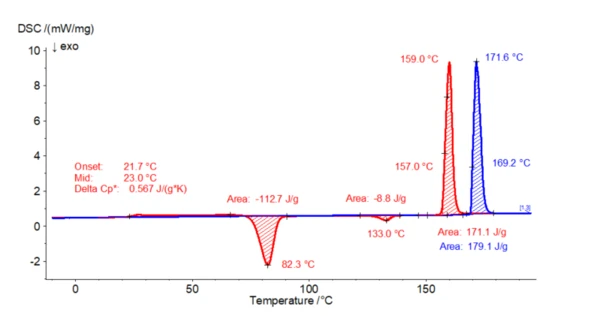
Zadaliśmy dr Schauerte jeszcze kilka pytań, aby uzupełnić jego artykuł:
NETZSCH: Dr Schauerte, ściśle współpracuje Pan z firmami farmaceutycznymi, zapewniając wsparcie w zakresie problemów napotykanych podczas opracowywania i przetwarzania aktywnych składników farmaceutycznych. Jakie pytania są najczęściej zadawane przez firmy farmaceutyczne i w jaki sposób metody analizy (termicznej) mogą pomóc w rozwiązaniu tych problemów?
Dr Carsten Schauerte: Jeśli chodzi o układy polimorficzne, najczęściej zadawane pytania to:
- Jakie formy stałe istnieją?
- Jakie są właściwości poszczególnych form?
Zwłaszcza w przypadku pierwszego pytania odpowiedź nie jest łatwa i należy zaplanować i przeprowadzić szeroko zakrojone eksperymenty z późniejszą analizą usieciowania, aby jak najdokładniej opisać krajobraz stanu stałego kandydata na lek. Zawsze zależy to od tego, ile czasu i energii (oraz środków finansowych) należy zainwestować. Metody analityczne są tu szczególnie przydatne do identyfikacji i charakterystyki nowych form polimorficznych. Analizy termiczne pokazują zachowanie termiczne różnych form (przejścia szkliste, Temperatury i entalpie topnieniaEntalpia syntezy substancji, znana również jako ciepło utajone, jest miarą nakładu energii, zazwyczaj ciepła, która jest niezbędna do przekształcenia substancji ze stanu stałego w ciekły. Temperatura topnienia substancji to temperatura, w której zmienia ona stan ze stałego (krystalicznego) na ciekły (stopiony izotropowo). topnienie i KrystalizacjaKrystalizacja to fizyczny proces twardnienia podczas tworzenia i wzrostu kryształów. Podczas tego procesu uwalniane jest ciepło krystalizacji.krystalizacja, a także odgazowywanie cieczy), ale także dostarczają informacji o potencjalnych właściwościach transformacji między dwiema lub więcej formami. Ponadto, DSC może być również wykorzystywana jako narzędzie przygotowawcze do generowania nowych form.
NETZSCH: Wysokie nakłady inwestycyjne ponoszone przez firmę farmaceutyczną do czasu znalezienia aktywnego składnika nadającego się do wprowadzenia na rynek oznaczają, że kwestie prawa patentowego są również częścią twojego zakresu. Czy mógłby Pan pokrótce wyjaśnić, na czym to głównie polega i w jaki sposób (termiczne) metody analityczne również przyczyniają się do rozwiązywania tych problemów?
Dr Carsten Schauerte: Wnioski patentowe dotyczące polimorficznej postaci stałej są zazwyczaj składane w następstwie wygaśnięcia patentu na substancję i często służą przedłużeniu ochrony patentowej substancji czynnej. Inne firmy mogą następnie zakwestionować ten nowy patent lub wprowadzić na rynek alternatywną, niechronioną formę, być może nawet mając ją chronioną. Analizy termiczne również przyczyniają się do scharakteryzowania i jasnego przypisania form. Ponadto, określając na przykład temperaturę topnienia, mogą one wyjaśnić decydującą przewagę nowej formy nad innymi formami, co może prowadzić do opatentowania.
NETZSCH: Ostatnie pytanie, dr Schauerte: Różnicowa kalorymetria skaningowa jest jedną z najczęściej stosowanych metod analizy termicznej. Gdzie widzi Pan siłę DSC w swoich zastosowaniach?
Dr Carsten Schauerte: Tak ważne i cenne jak metody dyfrakcji rentgenowskiej, mikroskopii i spektroskopii wibracyjnej, zwykle dostarczają one tylko migawkę, podczas gdy metody analizy termicznej przedstawiają dynamiczny obraz w określonym zakresie temperatur. Ma to dla nas ogromne znaczenie, ponieważ składniki aktywne są przetwarzane nie tylko w jednej bardzo określonej temperaturze, ale w wielu temperaturach na przestrzeni czasu: Istnieją procesy produkcji i formułowania, a także drogi przechowywania i transportu, podczas których dany składnik aktywny jest narażony na wyższe lub niższe temperatury, a selected w postaci stałej musi je wytrzymać. Aby to zagwarantować, musimy jak najdokładniej poznać i opisać zachowanie termiczne składnika aktywnego lub polimorfu, aby móc zapobiec niepożądanym przemianom fazowym.
NETZSCH: Dr Schauerte, bardzo dziękuję za ten ekscytujący wgląd w Pańską pracę!