
23.02.2023 by Prof. Dr. Michael Gasik (Aalto University Helsinki, Finland)
DMA sui biomateriali: Vedere l'invisibile!
Un articolo del Prof. Dr. Michael Gasik (Università Aalto di Helsinki, Finlandia)
Attualmente sono disponibili molti tipi di biomateriali da utilizzare in diversi impianti, soprattutto in ambito ortopedico e dentale. Vengono utilizzate leghe metalliche, ceramiche e compositi, con o senza cellule vive. Vi è un crescente campo di applicazione di diversi scaffold utilizzati nelle applicazioni di ingegneria tissutale per sostenere e promuovere la formazione di nuovi tessuti, e molti di questi sono realizzati con la (bio)stampa 3D. La rigenerazione dei tessuti biologici è nota per essere una delle sfide più impegnative, che richiede strutture biomateriali con proprietà biomeccaniche corrette [1] che imitino il comportamento in vivo [2]. I biomateriali corretti aiutano l'organismo a ricostruire il tessuto danneggiato e a ridurre al minimo il dolore e i tempi di guarigione associati [3].
Questo articolo del Prof. Dr. Michael Gasik (Aalto University Helsinki, Finlandia) mostra una nuova applicazione della tecnica di analisi dinamico-meccanica (DMA), chiamata BEST(Biomaterials Enhanced Simulation Testing), utilizzata per caratterizzare e migliorare i biomateriali e i dispositivi medici; questo metodo va oltre le note analisi classical viscoelastico.

Il Prof. Michael Gasik dell'Università di Aalto in Finlandia (Dipartimento di Ingegneria Chimica e Metallurgica) ha iniziato a lavorare alle applicazioni di analisi termica nel 1985 e collabora con NETZSCH-Gerätebau GmbH da quasi altrettanto tempo.
La sua attenzione si è concentrata sui materiali per applicazioni ad alta temperatura e per la tecnologia dell'idrogeno. Dal 2000 si occupa attivamente di biomateriali, dispositivi medici e applicazioni di medicina rigenerativa. Nel 2019 è stato nominato ambasciatore della European Orthopedic Research Society.
Il Prof. Michael Gasik è cofondatore di Seqvera Ltd. e inventore del metodo BEST - Biomaterials Enhanced Simulation Testing - che è stato implementato per la prima volta nell'apparecchiatura DMA di NETZSCH.
arcUn punto focale delle attività di ricerca del Prof. Michael Gasik è la determinazione delle proprietà meccaniche dei biomateriali. In questo contesto, utilizza i dati DMA generati con un NETZSCH DMA 242 Artemis come base per ulteriori calcoli per caratterizzare questi materiali. Per saperne di più sul suo approccio:
Sfide
Sono già stati condotti numerosi studi e sono stati raccolti dati clinici relativi alla forma, al design e allo stato superficiale dei biomateriali, nonché alla geometria degli impianti e alla loro idoneità alla qualità e alla posizione dei diversi tessuti. Sono state riportate differenze significative anche per materiali impiantati apparentemente identici ma provenienti da fonti diverse [4]. La caratterizzazione biomeccanica dell'osso e dei tessuti molli è più problematica rispetto a quella dei materiali metallici, ceramici e polimerici. Gli insiemi di dati pubblicati spesso non si basano su protocolli e condizioni di misurazione comparabili, con conseguente mancanza di coerenza. La generalizzazione di questi dati è molto difficile o quasi impossibile quando si tratta di fornire informazioni semplici, robuste e pertinenti.
Per la caratterizzazione biomeccanica, di solito si ricorre all'ipotesi che un materiale sia di tipo elastico o viscoelastico per approssimare le proprietà in singoli numeri, solitamente indicati come "Modulo elasticoIl modulo complesso (componente elastica), modulo di conservazione o G', è la parte "reale" del modulo complesso complessivo del campione. Questa componente elastica indica la risposta del campione in fase di misurazione. modulo elastico". Questo, tuttavia, si adatta solo ai materiali elastici lineari per deformazioni molto small e le linee guida NPL [5] elencano nove metodi per calcolare il Modulo elasticoIl modulo complesso (componente elastica), modulo di conservazione o G', è la parte "reale" del modulo complesso complessivo del campione. Questa componente elastica indica la risposta del campione in fase di misurazione. modulo elastico che possono portare a valori diversi. La stragrande maggioranza dei biomateriali e dei tessuti non sono chiaramente elastici, quindi è una semplificazione eccessiva cercare di ridurre artificialmente i dati ad alcuni numeri fissi: Quale sarebbe, ad esempio, il vantaggio di conoscere il "Modulo elasticoIl modulo complesso (componente elastica), modulo di conservazione o G', è la parte "reale" del modulo complesso complessivo del campione. Questa componente elastica indica la risposta del campione in fase di misurazione. modulo elastico della mucosa" che va da 0,1 a 680 MPa da fonti diverse?
Purtroppo, i problemi legati agli effetti di inerzia (alte frequenze) o ai limiti degli strumenti (basse frequenze) non sono sempre sufficientemente documentati nei protocolli di prova pubblicati. Anche se l'inerzia dello strumento viene eliminata, il campione stesso avrà sempre un'inerzia finita, che può produrre artefatti dovuti alla diffusione del momento, alle onde viscoelastiche e ai flussi secondari, tutti elementi che possono violare l'ipotesi di deformazione omogenea e lineare [6]. I modelli più sofisticati hanno un numero considerevole di parametri di adattamento artificiali e vi sono grandi difficoltà sperimentali nell'eseguire tali test nell'ambito degli standard, dei protocolli e dei metodi di prova ad hoc esistenti [7].
Per processi come il bioprinting 3D, ci sono diverse sfide da superare, come il controllo delle proprietà dei bioink, la gestione del flusso e del suo effetto sulla vitalità delle cellule e la garanzia di proprietà biofisiche ottimali dei costrutti dopo la stampa e l'impianto [8]. Sono necessarie una maggiore risoluzione e velocità di controllo nel microambiente 3D e una combinazione ottimale di proprietà meccaniche e di trasporto all'interno della scala spaziale e temporale, necessarie in particolare per la vascolarizzazione limitata alla diffusione. Le nuove normative sui dispositivi medici (2017/745) richiedono che venga effettuata una corretta valutazione meccanica, con conseguente adesione alle normative sulla valutazione delle tecnologie sanitarie (2021/2282).
Purtroppo, molti metodi diversi di test biofisici danno risultati piuttosto diversi e non è facile ottenere proprietà realistiche e veritiere. Le ragioni di queste differenze sono molteplici: contatto irregolare, stato di fase, effetti di inerzia e instabilità elastica, adattamento a modelli assunti in modo improprio, limiti nella definizione delle deformazioni, mancanza di un'adeguata valutazione della storia di carico, ecc. È quindi molto importante disporre di un approccio robusto in grado di quantificare sia il comportamento di un biomateriale che le sue prestazioni nel processo, piuttosto che limitarsi a generare alcuni numeri specifici.
Il concetto BEST
Per affrontare queste sfide, abbiamo sviluppato il metodo brevettato BEST(Biomaterials Enhanced Simulation Testing). Può essere applicato a molti biomateriali duri e morbidi, compresi gli idrogel, i costrutti stampati in 3D e la somministrazione controllata di farmaci. Le soluzioni BEST mirano a risolvere i problemi causati soprattutto da prove improprie e frammentarie, e si basano su un approccio integrato basato su un principio di causalità fondamentale: "Non c'è stata risposta da parte del campione prima dell'applicazione dello stimolo"
Il BEST viene eseguito in condizioni controllate con gli stimoli coerenti richiesti nell'ambiente DMA. Valuta i cambiamenti delle proprietà del campione nei domini del tempo, della fase e dello stimolo [9]. Nella post-elaborazione, BEST integra i dati, convolge la storia del campione ed estrae i valori sconosciuti, il tutto senza richiedere all'utente di select il modello del materiale (l'analisi dei dati è essenzialmente priva di modello). I parametri invarianti ottenuti con un algoritmo proprietario di regressione quantistica incorporano la storia del campione, mostrando la posizione e la direzione dello sviluppo di un biomateriale [10].
La caratteristica chiave di BEST è l'elaborazione invariante dei dati DMA, che di solito rimane inesplorata dall'utente. Questo nuovo metodo supera le limitazioni comuni alla linearità delle proprietà tissutali in molti modelli, in particolare una proprietà di scalatura (omogeneità) e una proprietà di sovrapposizione (additività), che in genere non sono presenti nella trasformazione di Fourier utilizzata nella viscoelasticità lineare.
BEST applica quindi un protocollo di prova corretto e utilizza metodi idempotenti per estrarre i parametri da un singolo campione/test, ottenendo dati di output elevati senza l'uso di matematica complessa (non c'è bisogno di moduli complessi) o l'assunzione di linearità, ed è in grado di rielaborare anche altri dati reologici in modo tale da non perdere il loro valore.
Esempio di applicazione del DMA
Nell'esempio qui riportato, il metodo sopra descritto è stato applicato sulla base di misurazioni eseguite con un DMA 242 Artemis® NETZSCH per caratterizzare le proprietà dell'idrogel acrilico per la bioprinting 3D senza utilizzare un modello presunto. Il gel è stato inserito in una siringa da 1 ml con un ago da 29 G e posizionato nel portacampioni DMA personalizzato, solitamente utilizzato per la piegatura; è stato testato in modalità stepwise creep a 25°C.
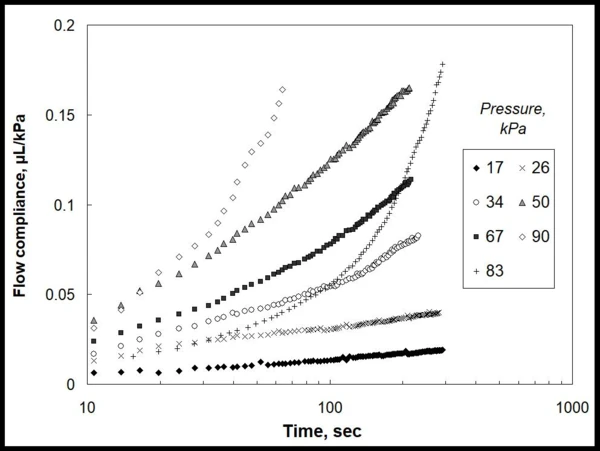
La Figura 1 mostra i dati sperimentali relativi alla quantità di gel estruso (µL) attraverso un ugello definito, normalizzato per la pressione locale applicata (kPa). Questi dati rivelano chiaramente la non linearità della cinetica di flusso con il tempo e la pressione applicata, e non esiste un modo diretto per select qualsiasi modello di materiale per descrivere queste dipendenze.
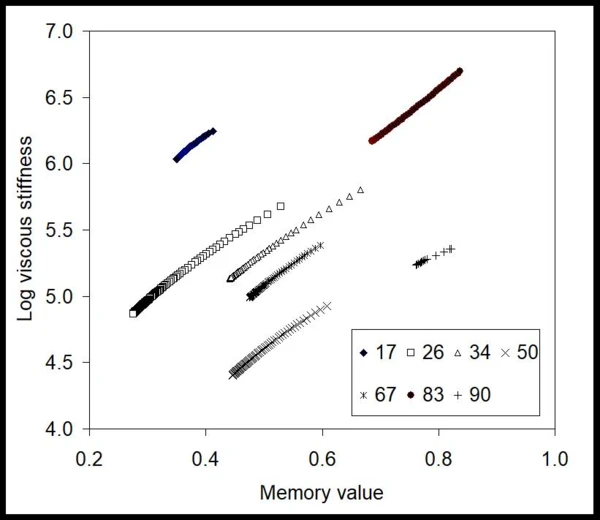
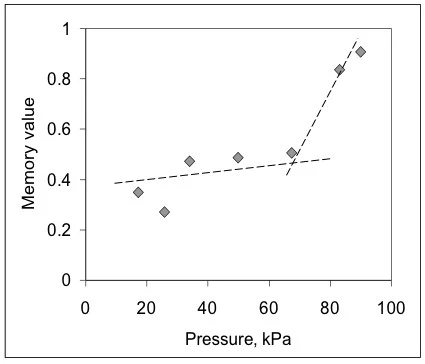
Da questi dati, il metodo BEST ha estratto valori variabili nel tempo per la rigidità viscosa del gel in queste condizioni di iniezione e il suo valore di memoria [9,10] (fig. 2). In questo caso, le curve sono quasi lineari e le pendenze delle linee sono quasi costanti per tutte le pressioni applicate (numeri in kPa). Ciò significa che il gel, pur presentando un comportamento Non newtonianoUn fluido non newtoniano è un fluido che presenta una viscosità che varia in funzione della velocità di taglio o dello sforzo di taglio applicato.non newtoniano, è lineare in termini di valori invarianti senza modello. Si può anche notare che i valori numerici cambiano con la pressione applicata in modo non monotono, rivelando che potrebbero esserci diversi fenomeni limitanti che influenzano il flusso. Per vedere l'effetto dello sviluppo del flusso, la fig. 3 mostra il grafico dei valori di memoria in funzione della pressione applicata. Questa mappa mostra che il gel nella siringa subisce attriti, resistenze al flusso ed eventualmente effetti di non scivolamento a basse pressioni, quando i valori di memoria sono molto inferiori all'unità. Dopo circa 65 kPa - l'inizio - questi valori aumentano, segnalando che il gel raggiunge un flusso più sviluppato.
Il metodo presentato è in grado di determinare valori invarianti e di utilizzarli nella previsione senza modelli dei processi di bioprinting 3D, in funzione dell'ugello, della geometria, della pressione, del tempo e di altre condizioni di processo, senza la necessità di determinare separatamente i parametri reologici dell'inchiostro. Il metodo BEST genera dati "di prima mano" per un'ulteriore modellazione predittiva del processo di stampa 3D e applica la stessa filosofia per la caratterizzazione dei tessuti e dei costrutti stampati in 3D.
SINTESI
L'approccio sviluppato dimostra la capacità di "vedere le caratteristiche invisibili" dei materiali e le loro interazioni con gli stimoli e l'ambiente. In questo modo, l'analisi dinamico-meccanica (DMA) può fornire molte più informazioni dei moduli elastici e della tangente di perdita. Utilizzando l'elaborazione BEST, si possono ottenere molte letture per vari scopi (in alcuni casi, anche da un singolo provino o test). Ad esempio, è possibile ottenere il modulo aggregato; il tempo caratteristico di Deborah; la cedevolezza per scorrimento; la diffusività e la permeabilità/permittività effettive del fluido; la dimensione equivalente del canale per il flusso del fluido nella dinamica; il valore di memoria del materiale; la pressione di rigonfiamento e altro ancora in un singolo esperimento. E questo va oltre i soli biomateriali, poiché l'applicazione BEST è priva di modelli e non richiede parametri di adattamento; inoltre, può essere applicata anche a dati di prova già creati.
Letteratura:
[1] Hubbell J.A. Nature Biotechnol. 13 (1995) 565-576.
[2] Gasik M. Sci. Techn. Adv. Mater. 18 (2017) 550-562.
[3] Chung C., Burdick J.A. Adv. Drug Delivery Rev. 60 (2008) 243-262.
[4] Gasik M., Lambert F., Bacevic M., Materiali 14 (2021) 2845.
[5] Lord J.D., Morrell R. Guida alle buone pratiche di misurazione n. 98nPL Teddington, Regno Unito (2006)
[6] Ewoldt R.H., Johnston M.T., Caretta L.M. In: Fluidi complessi nei sistemi biologicispringer, Germania (2015).
[7] Vrana N.E., Knopf-Marques H., Barthes J. (Eds.) Biomateriali per la rigenerazione di organi e tessutiwoodhead Publ. UK (2020).
[8] Jammalamadaka U., Tappa K. J. Funct. Biomater. 9 (2018) 22
[9] Gasik M., Bilotsky Y. Patent US 10379106 B2 (2019).
[10] Gasik M.Brevetto US 10809171 B2 (2020).
Contatto:
Prof. Dr. Michael Gasik, Dr. Sci.
Terkko Health Hub, Building 14
Helsinki University Central Hospital Area
Haartmaninkatu 4, FIN-00290 Helsinki
www.seqvera.com
Si ringrazia il Prof. Dr. Michael Gasik per questo articolo e per gli approfondimenti sul suoarclavoro di ricerca.







