Principio di funzionamento di un DSC a flusso termico
Una cella di misura DSC è costituita da un forno e da un sensore integrato con posizioni designate per le vaschette del campione e di riferimento.
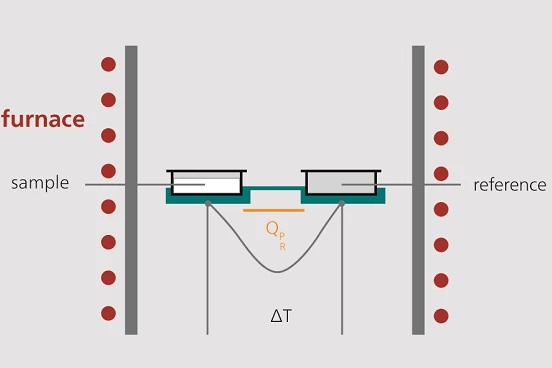
Le aree del sensore sono collegate alle termocoppie o possono anche essere parte della termocoppia. Ciò consente di registrare sia la differenza di temperatura tra il campione e il lato di riferimento (segnale DSC) sia la temperatura assoluta del campione o del lato di riferimento.
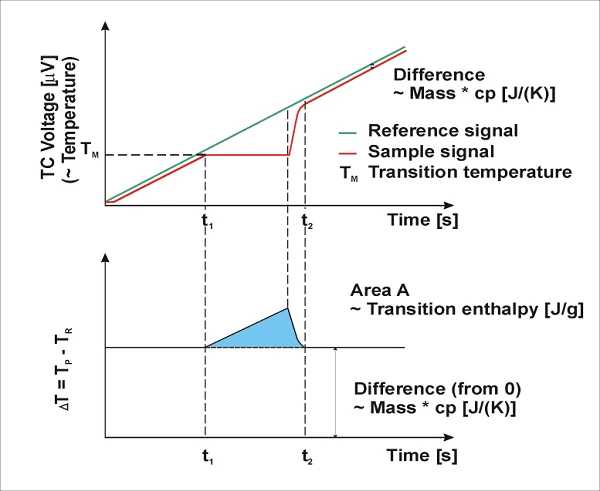
A causa della capacità termica (Capacità termica specifica (cp)La capacità termica è una grandezza fisica specifica del materiale, determinata dalla quantità di calore fornita al campione, divisa per l'aumento di temperatura risultante. La capacità termica specifica è correlata all'unità di massa del campione.cp) del campione, il lato di riferimento (di solito una pentola vuota) si riscalda generalmente più velocemente del lato campione durante il riscaldamento della cella di misura DSC; in altre parole, la temperatura di riferimento (TR, verde) aumenta un po' più velocemente della temperatura del campione (TP, rosso). Le due curve hanno un comportamento parallelo durante il riscaldamento a velocità costante, fino a quando non si verifica una reazione del campione. Nel caso qui illustrato, il campione inizia a fondere a t1. La temperatura del campione non cambia durante laTemperature di fusione ed entalpieL'entalpia di fusione di una sostanza, nota anche come calore latente, è una misura dell'apporto di energia, tipicamente calore, necessario per convertire una sostanza dallo stato solido a quello liquido. Il punto di fusione di una sostanza è la temperatura alla quale essa cambia stato da solido (cristallino) a liquido (fusione isotropa). fusione; la temperatura del lato di riferimento, invece, rimane inalterata e continua a mostrare un aumento lineare. Al termine dellaTemperature di fusione ed entalpieL'entalpia di fusione di una sostanza, nota anche come calore latente, è una misura dell'apporto di energia, tipicamente calore, necessario per convertire una sostanza dallo stato solido a quello liquido. Il punto di fusione di una sostanza è la temperatura alla quale essa cambia stato da solido (cristallino) a liquido (fusione isotropa). fusione, anche la temperatura del campione ricomincia ad aumentare e, a partire dal momento t2, presenta nuovamente un aumento lineare.
Il segnale differenziale (ΔT) delle due curve di temperatura è presentato nella parte inferiore dell'immagine. Nella parte centrale della curva, il calcolo delle differenze genera un picco (blu) che rappresenta il processo EndotermicoUna transizione campionaria o una reazione è endotermica se per la conversione è necessario il calore.endotermico diTemperature di fusione ed entalpieL'entalpia di fusione di una sostanza, nota anche come calore latente, è una misura dell'apporto di energia, tipicamente calore, necessario per convertire una sostanza dallo stato solido a quello liquido. Il punto di fusione di una sostanza è la temperatura alla quale essa cambia stato da solido (cristallino) a liquido (fusione isotropa). fusione. A seconda che durante il calcolo la temperatura di riferimento sia stata sottratta dalla temperatura del campione o viceversa, il picco generato può puntare verso l'alto o verso il basso nei grafici. L'area del picco è correlata al contenuto di calore della transizione (entalpia in J/g).
Le norme DIN 51007 e ISO 11357-1 raccomandano di rappresentare i processi endotermici con un'ampiezza dell'ordinata verso l'alto. Nelle norme ASTM E793 ed E794, ad esempio, si suggerisce di applicare la direzione endotermica verso il basso. Per questo motivo il software NETZSCH Proteus® consente di selectla direzione di applicazione dei processi endotermici ed esotermici.






