Introdução
Muitos sólidos farmacêuticos apresentam PolimorfismoPolimorfismo é a capacidade de um material sólido de formar diferentes estruturas cristalinas (sinônimos: formas, modificações).polimorfismo, ou seja, a capacidade de uma substância existir em diferentes formas cristalinas; portanto, eles têm diferentes arranjos moleculares na estrutura cristalina. Devido às suas diferenças estruturais, os polimorfos podem ter propriedades sólidas diferentes, como DensidadeA densidade de massa é definida como a relação entre massa e volume. densidade, cor, Temperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica).ponto de fusão, solubilidade, propriedades mecânicas etc. Consequentemente, a forma polimórfica pode ter uma influência significativa no processamento farmacêutico e pode, por exemplo, afetar a moagem, a granulação e a capacidade de ser apresentado em comprimidos [1].
O paracetamol, que é usado para o tratamento de dor e febre, também é um polimorfo, ou seja, existe em diferentes formas cristalinas. Cada uma dessas modificações se comporta de forma diferente, especialmente com relação à estabilidade termodinâmica e à capacidade de compressão. Essa última propriedade influencia a capacidade de compressão do paracetamol, ou seja, sua capacidade de ser transformado em um comprimido sob o efeito da pressão. Foi comprovado que o paracetamol ortorrômbico (também chamado de forma II) pode ser usado para compressão direta. Sua melhor capacidade de formar comprimidos do que a forma monoclínica do paracetamol (forma I) se deve à presença de planos de deslizamento paralelos na estrutura cristalina ortorrômbica. [5, 6]
No entanto, a forma monoclínica é a mais usada comercialmente [4], provavelmente por causa de sua melhor estabilidade termodinâmica. Como a modificação do paracetamol está intimamente associada às suas propriedades, é essencial saber em que forma ele está presente antes do processamento, especialmente para a produção de comprimidos que exigem compactação. A seguir, a modificação do paracetamol é determinada por meio da calorimetria de varredura diferencial.
Condições de medição
1.69 mg de paracetamol foram medidos em um cadinho de alumínio vedado com uma tampa perfurada. Essa amostra foi aquecida duas vezes a 200°C em uma taxa de aquecimento de 10 K/min. Entre as duas execuções de aquecimento, ela foi resfriada a uma taxa controlada de 10 K/min.
Resultados do teste
A Figura 2 exibe as curvas de medição para as duas execuções de aquecimento. O pico detectado a 169 °C (temperatura de início) durante o primeiro aquecimento (curva verde) está em ótima concordância com o valor do Temperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica).ponto de fusão da modificação cristalina I (consulte a tabela 1).
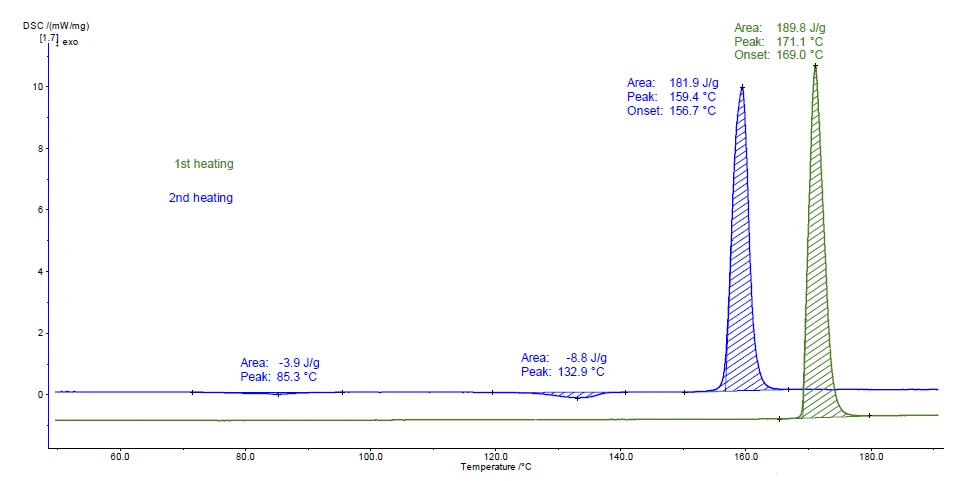
Tabela 1: Temperatura deTemperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica). fusão das diferentes modificações do paracetamol [2, 3]
Os picos exotérmicos a 85°C e 133°C (temperatura de pico) que ocorrem no segundo aquecimento indicam CristalizaçãoA cristalização é o processo físico de endurecimento durante a formação e o crescimento de cristais. Durante esse processo, o calor da cristalização é liberado.cristalização. A modificação formada derrete posteriormente a 156,7°C (temperatura inicial); isso é típico da forma cristalina II.
Conclusão
A caracterização do estado sólido é de importância fundamental para o setor farmacêutico, uma vez que os medicamentos são predominantemente produzidos como sólidos. Selectíon da forma sólida ideal é um aspecto crítico no desenvolvimento de medicamentos, pois eles podem existir em mais de uma forma de estrutura cristalina. Esse PolimorfismoPolimorfismo é a capacidade de um material sólido de formar diferentes estruturas cristalinas (sinônimos: formas, modificações).polimorfismo mostra diferentes propriedades físicas que influenciam não apenas as propriedades biofarmacêuticas, mas também a capacidade de ser combatido.
Uma única execução de aquecimento DSC até aTemperaturas e entalpias de fusãoA entalpia de fusão de uma substância, também conhecida como calor latente, é uma medida da entrada de energia, normalmente calor, necessária para converter uma substância do estado sólido para o líquido. O ponto de fusão de uma substância é a temperatura na qual ela muda de estado, passando do sólido (cristalino) para o líquido (fusão isotrópica). temperatura de fusão permite a identificação da modificação do paracetamol que está sendo investigada, possibilitando a estimativa de seu comportamento durante a compressão.