Введение
Термическая обработка различных материалов может привести к выделению аммиака, который имеет агрессивный запах и может поражать бронхиальную систему. Выделение аммиака может быть вызвано множеством различных процессов. Это и термическое разложение солей, и дым от сжигания табака, и пиролиз полимеров, например полиамидов (ПА), и производство пластиковых пен, требующих пенообразователей. Широко известным продуктом последней категории являются коврики для йоги. Выделение аммиака может привести к образованию мелкодисперсной пыли в результате реакции с серной и азотной кислотой при образовании солей. В окружающей среде выделение аммиака может привести к закислению почвы. Одним из основных источников аммиака в окружающей среде является сельское хозяйство, особенно удобрение навозом и азотсодержащими минеральными удобрениями.
По этой причине количественное определение высвобождающегося аммиака имеет важное значение для многих приложений. Выделение аммиака в зависимости от температуры может быть легко обнаружено с помощью ТГА-ФТ-ИК-связи.libraДля количественного определения выделившейся части аммиака необходимо построить кривую с известной концентрацией аммиака. Подходящим соединением для этого является бикарбонат аммония, поскольку он выделяет аммиак в стехиометрическом соотношении в дополнение к выделению воды и углекислого газа; см. уравнение (1). При этом образуются только газообразные соединения:
(1) NH4HCO3->NH3 + H2O+ CO2
Как сгенерировать кривую Calibration
Для проведения данного исследования использовался NETZSCH PERSEUS® TG 209 F1 Libra® . Нагревание бикарбоната аммония приводило к полному разложению к 200°C, с пиком скорости потери массы при 127°C (согласно условиям измерений, приведенным в таблице 1).
Таблица 1: Условия измерения для построения кривой каlibraтирования
| Параметр | NH4HCO3 | |||
| Температурная программа | RT - 200°C, 5 К/мин | |||
| Скорость потока | 40 мл/мин | |||
| Держатель образца | Держатель стандартного образца | |||
| Газовая атмосфера | Азот | |||
| Крюшон | Al2O3 (85 мкл) открытый | |||
| Масса образца | 5.31 мг | 10.16 мг | 15.01 мг | 20.50 мг |
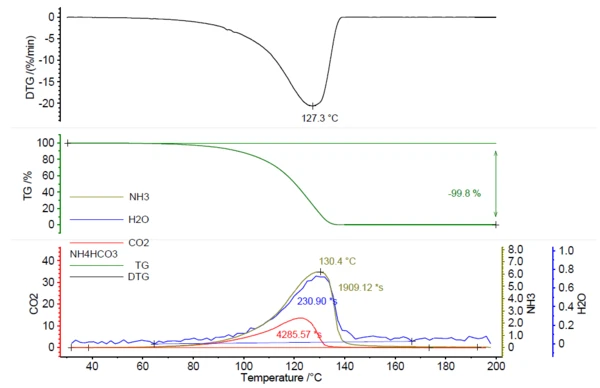
В соответствии с потерей массы было обнаружено выделение ИК-активных газов; см. рис. 1.
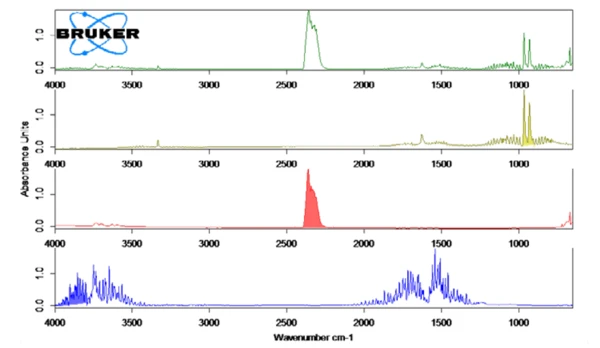
На рис. 2 показан измеренный ИК-Фурье спектр при 130°C (зеленый) в корреляции со спектрами library аммиака (оливковый), воды (синий) и углекислого газа (красный). Зависимое от температуры выделение этих соединений было представлено в виде трасс на рисунке 1. Эти следы были получены путем интегрирования окрашенных областей (см. рис. 2) ИК-Фурье спектров для каждого соединения во всем диапазоне температур. Эти области ИК-Фурье спектров были отдельными для NH3 (898 см-1 - 981 см-1),CO2 (2200 см-1 - 2450 см-1) и H2O(3793 см-1 - 4001 см-1) и не пересекались с областями других соединений.
В таблице 2 приведены стехиометрически рассчитанные количества выделяющихся газов по отношению к массе образца бикарбоната аммония.
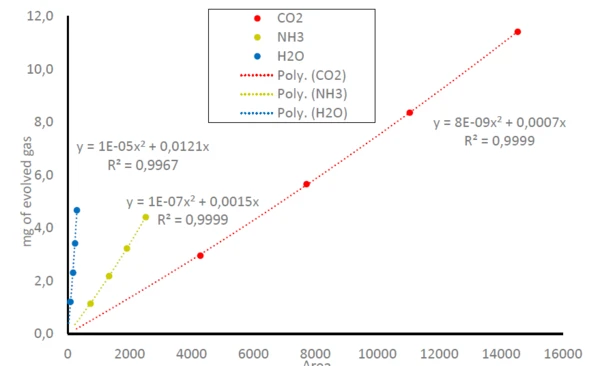
Следовательно, площади под следами NH3,CO2 и H2Oна рисунке 1 могут быть связаны с количеством выделившихся газов; сравните уравнение (1).libraЭто приводит к построению кривых для NH3,CO2 и H2O, где обнаруженная площадь под следами связана с количеством выделившегося газа; см. рисунок 3. Поскольку ИК-Фурье-спектрометр имеет только линейный диапазон small, это приводит к полиномиальным уравнениям для всех трех газообразных молекул с коэффициентами детерминации (R2), очень близкими к 1. В данном исследовании масса каждого образца измерялась только один раз. Повторные измерения или большее количество точек данных привело бы к еще большей точности линии тренда.
Таблица 2: Масса образца и полученные стехиометрические количества выделившегося газа
| m (NH4HCO3) [мг] | m (CO2) [мг] | m (NH3) [мг] | m (H2O) [мг] |
| 5.31 | 2.96 | 1.14 | 1.21 |
| 10.16 | 5.66 | 2.19 | 2.31 |
| 15.01 | 8.36 | 3.23 | 3.42 |
| 20.50 | 11.42 | 4.41 | 4.67 |
Как проверить точность кривой Calibra
Точность кривой каlibraтирования была проверена с помощью другого измерения NH4HCO3 с определенной массой образца 15,22 мг. Теоретические количества NH3,CO2 и H2Oсравнивались с рассчитанными значениями NH3,CO2 и H2Oс помощью кривой каlibraтирования. В результате погрешность составила от 0,8 % для NH3 до 4,9 % для H2O; см. таблицу 3.
Исследование пенообразователя - воплощение теории в практику
На следующем этапе полученные и проверенные кривые каlibraтификации могут быть использованы для количественного определения выделения неизвестных количеств каlibraтифицированных газов.
Азодикарбонамид используется в качестве пенообразователя для получения полимерных пен (структуру см. на рис. 4). Он используется при производстве ПВХ-пены и ЭВА-ПЭ-пены, где при разложении при температуре обработки образуются пузырьки с выделением N2, CO,CO2 и NH3. Виниловая пена легко сжимается и демонстрирует высокую и быструю восстанавливаемость, поэтому ее часто называют "пружинистой". Он также прилипает к гладким поверхностям. По этой причине он используется для изготовления подкладок под ковры, напольных ковриков и ковриков для йоги.
Полимеры, для которых использовался этот пенообразователь, не должны контактировать с водой. NH3 и вода могут образовывать NH4OHи вызывать коррозию окружающей среды. По этой причине количественное определение аммиака из этого пенообразователя представляет большой интерес.
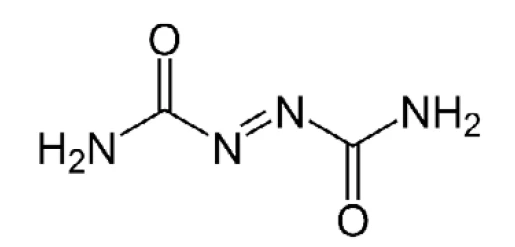
Таблица 3: Определение погрешности, сравнение теоретических и расчетных величин
Теоретическое (мг) | Расчетное (мг) | Ошибка (%) | |
| m (NH4HCO3) | 15.22 | ||
| m (NH3) | 3.28 | 3.30 | 0.801 |
| м (CO2) | 8.48 | 8.76 | 3.28 |
| м (H2O) | 3.47 | 3.31 | 4.86 |
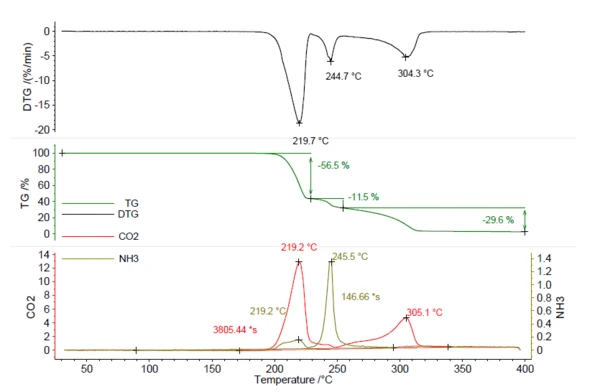
Образец 5,25 мг азодикарбонамида нагревали до 400°C со скоростью 5 К/мин в атмосфере азота. Полученная термограмма представлена на рисунке 5. В общей сложности наблюдались три ступени потери массы 56,5 %, 11,5 % и 29,6 % с пиками на кривой ДТГ при 219 °С, 245 °С и 304 °С. СледыCO2 и NH3 были созданы так же, как и для NH4HCO3 на рисунке 1, и изображены красным и оливковым цветами. Это показывает, чтоCO2 и NH3 высвобождаются во время различных этапов потери массы и не могут быть количественно определены только по результатам ТГА. Для количественного определения этого соединения необходимы данные анализа уходящих газов. При расчете количества выделившегося аммиака с использованием кривой выделения calibraбыло получено 0,22 мг NH3 (4%). Аналогичным образом можно рассчитать количество выделившегосяCO2, которое составило 2,78 мг (53 %). Эти знания ценны для производственного процесса, чтобы убедиться, что все количество пенообразователя высвобождается во время вспенивания. Если в продукте остаются следы small, то для дальнейшего высвобождения необходима температура более 219°C.
Заключение
Комбинация термогравиметрии и инфракрасной спектроскопии является подходящим методом для обнаружения выделения постоянных газов, например, воды, углекислого газа и аммиака. При этом интерес представляет не только идентификация, но и количественное определение.libraДля этого необходимо построить кривую выделения с использованием известного материала. В данном примере бикарбонат аммония идеально отвечает этим требованиям. Кривые Calibration могут быть построены одновременно для H2O,CO2 и NH3 путем разложения трех различных порций NH4HCO3. Отклонения, подлежащие исследованию, определялись пятым измерением. С помощью этого препарата можно было идентифицировать и количественно определить неизвестные количества NH3 иCO2 из пенообразователя азодикарбонамида, используемого для производства полимерных пен.