Введение
Клавуланат калия (рис. 1) представляет собой соль клавулановой кислоты, которая является основным ß-лактамным антибиотиком, вырабатываемым организмом Streptomyces clavuligerus [1]. Сам по себе он обладает лишь слабой антибактериальной активностью в отношении большинства организмов, но в сочетании с антибиотиком амоксициллином эффективен против ß-лактамаз-продуцирующих стафилококков, устойчивых к амоксициллину [2, 3]. Именно поэтому он является признанным препаратом в фармацевтической промышленности.
Амоксициллин и клавуланат калия имеют схожие пути разложения. Однако стабильность комбинации амоксициллин-клавуланат в основном зависит от клавуланата, который является более разлагаемым из двух компонентов [4, 5].
Разложение клавуланата калия изучалось во многих работах [3, 4, 7, 12]. Как правило, вещество изучали в растворах с различными уровнями pH и в присутствии амоксициллина. Было замечено, что на стабильность примеси амоксициллин/клавулановая кислота влияет повышение температуры с 25 до 40 °C [3]. С другой стороны, срок годности примеси значительно увеличивается, если pH раствора подкисляется [4]. Также было замечено, что в растворах разложение клавулановой кислоты катализируется продуктами гидролиза [12]. Как показано с помощью метода ВЭЖХ на образцах, хранившихся при разных температурах и в разных атмосферных условиях, разложение клавуланата калия в твердом состоянии происходит по другому механизму: Продукты разложения, образующиеся в твердой фазе, не обладают каталитическим действием [8].
Термическая стабильность также может быть исследована с помощью термогравиметрии, которая определяет, в частности, температуру, при которой материал начинает разлагаться или реагировать [9]. Термическое разложение твердого клавуланата калия было охарактеризовано с помощью термовесов, соединенных с ИК-Фурье спектрометром в работе [13]. Далее термогравиметрические измерения используются для проведения кинетических исследований реакции разложения.
Это позволяет прогнозировать разложение клавуланата калия для конкретных температурных и временных условий. Знание термической стабильности и понимание процесса разложения клавуланата калия в твердом состоянии позволяет оптимизировать условия его хранения.
Экспериментальный
Измерения ТГА проводились на термобаллоне NETZSCH TG 209 F1 Libra® с автоматической сменой образцов. Из измерений ТГА-ФТ-ИК, описанных в [13], мы узнали, что образец выделяет поверхностную воду, как только начинается измерение. По этой причине следующие измерения проводились с использованием закрытых алюминиевых тиглей. Непосредственно перед измерением крышка тигля автоматически прокалывалась устройством для прокалывания ASC. Это предотвращает выделение образцом поверхностной воды еще до начала измерения, что привело бы к фальсификации значения начальной массы.
Масса образцов составляла от 4,33 до 5,04 мг. Образцы нагревались от комнатной температуры до 600°C при четырех скоростях нагрева от 1 К/мин до 10 К/мин. Измерения проводились в динамической атмосфере азота (40 мл/мин).
Полученные кривые ТГА являются основой для кинетической оценки реакции разложения.
Для этого использовалось программное обеспечение Kinetics Neo ( NETZSCH-Gerätebau GmbH). Она позволяет моделировать кинетику одно- и многостадийных реакций.
Каждый отдельный этап может быть отнесен к различным типам реакций с собственными кинетическими параметрами, такими как энергия активации, порядок реакции и предэкспоненциальный коэффициент. На основе полученных результатов Kinetics Neo может моделировать реакцию(и) для заданных пользователем температурных программ.
Результаты и обсуждение
Измерения ТГА
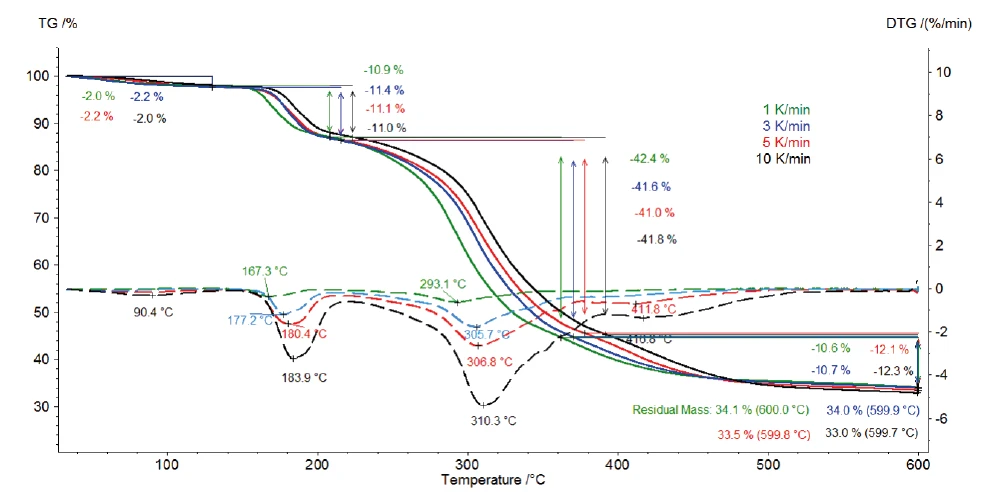
На рис. 2 представлены кривые ТГА и ДТГ (первая производная) измерений клавуланата калия при скоростях нагрева 1, 3, 5 и 10 К/мин. Первая ступень потери массы, обнаруженная между комнатной температурой и 120°C, обусловлена испарением поверхностной воды [13]. Далее, три ступени потери массы, обнаруженные между 120 и 600 °C, обусловлены разложением клавуланата калия. Они смещаются к более высоким температурам с увеличением скорости нагрева (кинетическое влияние). Например, при скорости нагрева 1 К/мин первый этап разложения происходит при 167°C (пик ДТГ), а при скорости нагрева 10 К/мин - при 184°C (пик ДТГ). Последняя ступень разложения становится более выраженной с увеличением скорости нагрева: При скорости нагрева 5 К/мин пик ДТГ наблюдается при 412°C (красная пунктирная кривая), а при 10 К/мин - при 417°C (черная пунктирная кривая).
Кинетический анализ термического разложения
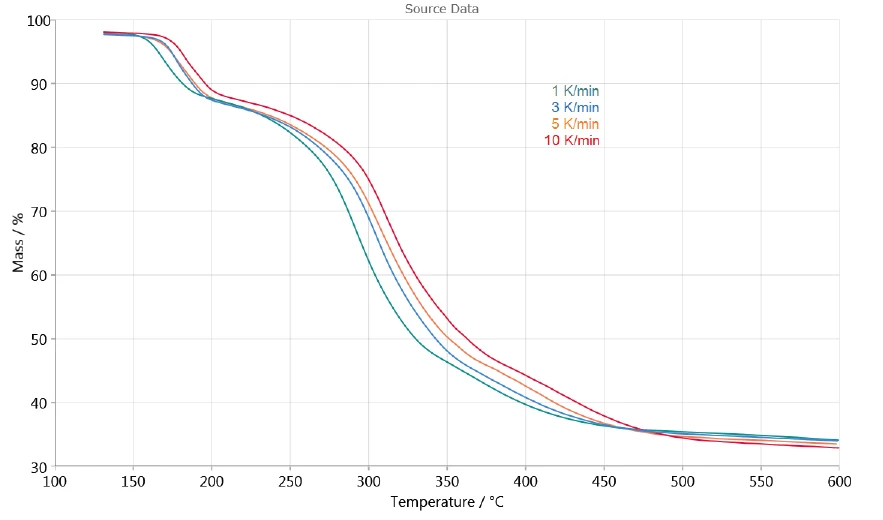
Зависимость разложения от скорости нагрева позволяет оценить процесс с помощью программы NETZSCH Kinetics Neo. На рисунке 3 представлены кривые ТГА измерений в интервале от 130°C до 600°C, использованные для кинетической оценки. Выделение поверхностной воды при температурах ниже 130°C не учитывается.
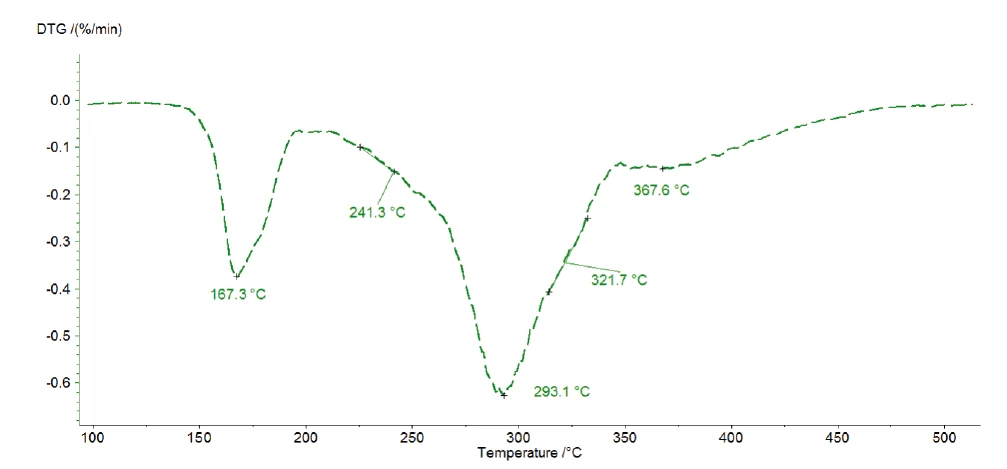
Обнаруженные три последовательные потери массы указывают как минимум на три стадии разложения. Кривая ДТГ при измерении со скоростью 1 К/мин, представленная на рисунке 4, показывает три пика при 167°C, 293°C и 368°C, а также два плеча с температурами начала разложения при 241°C и 322°C. Именно поэтому Kinetics Neo предлагает кинетическую модель с пятью последовательными шагами n-го порядка.
Скорость реакции каждого шага j описывается функцией: Reaction Ratej = Aj - f(ej,pj) - exp[-Ej/RT]
Aj: предэкспоненциальный коэффициент
Ej: энергия активации [Дж.моль-1]
T: температура [K]
R: газовая постоянная (8,314 Дж.K-1.моль-1)
f(ej,pj): функция, зависящая от концентрации
исходного реагента ej и концентрации продукта pj
На рисунке 5 приведено сравнение измеренных кривых ТГА (пунктирные линии) с расчетными кривыми (сплошные линии) выбранной 5-ступенчатой модели. Между измеренными и рассчитанными данными достигнут высокий коэффициент корреляции >0,999.
В таблице 1 приведены результаты кинетической оценки для каждого этапа. Теоретическая потеря массы рассчитывается путем умножения вклада этапа реакции в разложение на общую потерю массы, происходящую в процессе разложения.
Первый шаг разложения, A→B, связан с расчетной потерей массы 11,9 % и соответствует экспериментальным значениям 11 %. Потеря массы на последнем этапе, E→F, составляет 13,9 %. Это несколько выше экспериментального значения 11 - 12 %. Это означает, что последняя ступень потери массы начинается раньше (< 360°C). Общая потеря массы для ступеней B→C, C→D и D→E составляет 36,9% и соответствует сложному процессу разложения около 300°C (пик DTG) на рисунке 2.
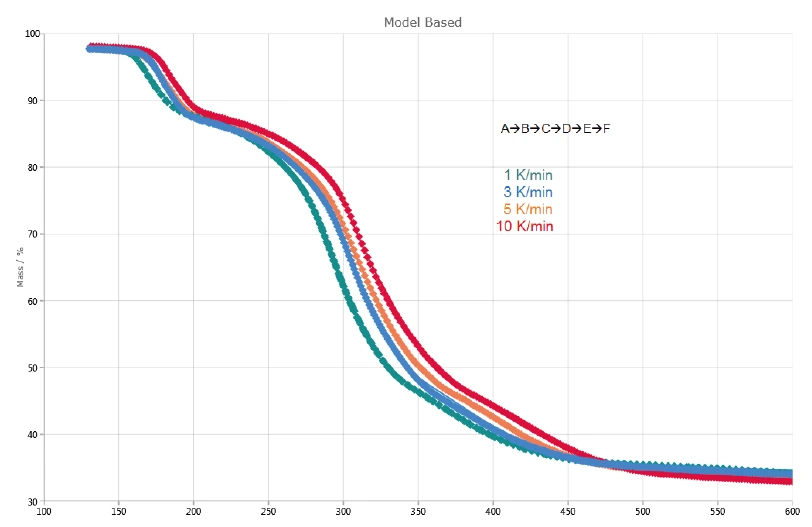
Таблица 1: Кинетические параметры термической деструкции клавуланата калия
| Шаг реакции | A → B | B → C | C → D | D → E | E → F |
|---|---|---|---|---|---|
| Энергия активации [кДж/моль] | 265.1 | 240.8 | 260.5 | 179.8 | 166.5 |
| Предэкспоненциальный коэффициент | 28.6 | 21.6 | 21.7 | 13.3 | 10.5 |
| Порядок реакции | 3.6 | 2.1 | 1.8 | 1.6 | 3.4 |
| Взнос | 0.190 | 0.099 | 0.244 | 0.246 | 0.222 |
| Теоретическая потеря массы | 11.9% | 6.2% | 15.3% | 15.4% | 13.9% |
Хорошая корреляция измерений с реакциями n-го порядка подтверждает выводы, сделанные в [8], о том, что в отличие от поведения клавуланата калия при разложении в растворах, его разложение в твердом состоянии не является автокатализируемым.
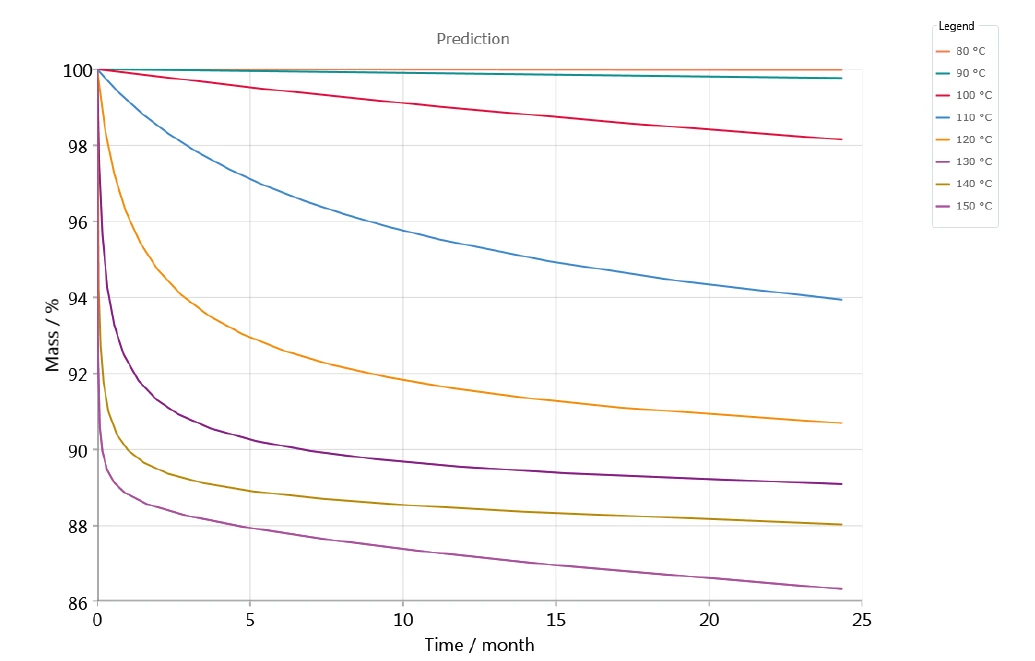
Кинетическая оценка была проведена с высоким коэффициентом корреляции и, таким образом, с высоким уровнем согласия между измеренными и смоделированными кривыми ТГА, что позволяет делать прогнозы относительно долгосрочного поведения при различных температурах хранения. В качестве примера на рисунке 6 показано изменение массы в зависимости от времени на основе 5-ступенчатой модели с последовательными шагами; оно представляет собой прогноз разложения клавуланата калия для различных температур от 80°C до 150°C в атмосфере азота. С повышением температуры разложение увеличивается. Этот эффект можно наблюдать уже при температуре хранения 90°C (зеленая кривая в верхней части графика - рисунок 6).
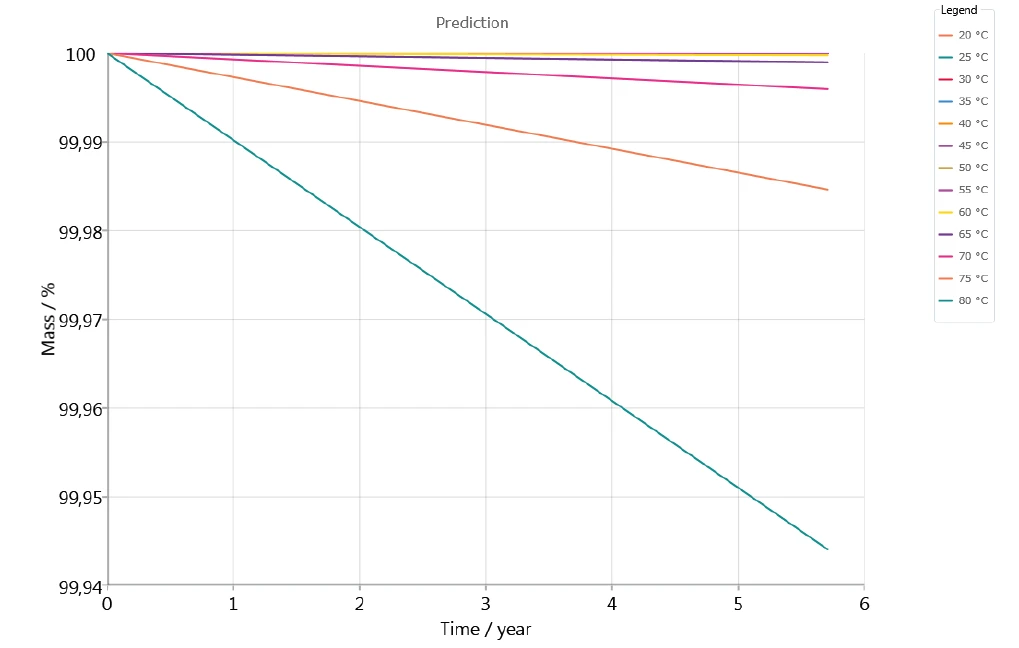
На рисунке 7 показана стабильность препарата в инертной атмосфере в течение 5 лет при температуре от 20°C до 80°C. Похоже, что при прогнозе температуры до 60°C не происходит значительной потери массы.
Следует напомнить, что кинетика разложения была проведена на сухом образце. Однако вода оказывает большое влияние на разложение клавуланата калия: Хранение во влажной атмосфере сдвигает его разложение к более низким температурам [10]. J. Cieleka-Piontek показывает, что образцы клавуланата калия разлагаются быстрее при повышенной влажности воздуха, чем при воздействии сухого воздуха, и предполагает, что атака молекулы воды на карбонильную группу ß-лактамного кольца вызывает термолиз [8].
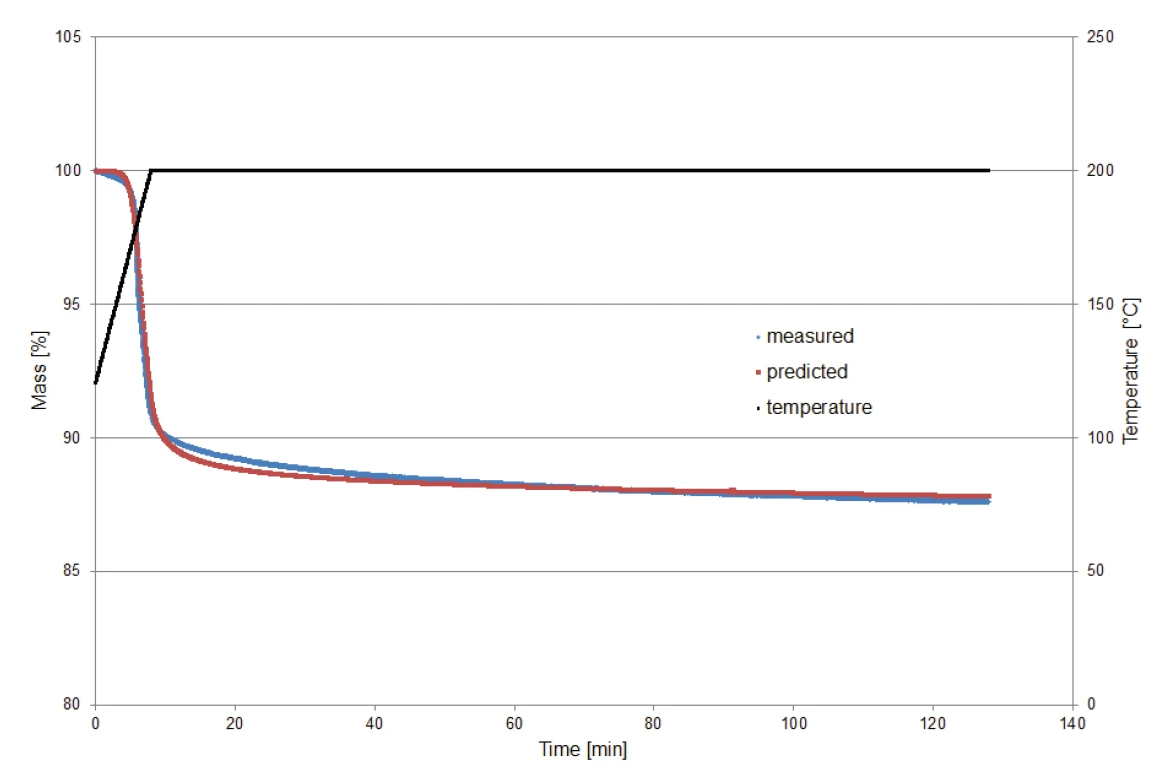
Для проверки кинетической модели, рассчитанной в Kinetics Neo для предсказания поведения разложения в изотермических условиях, образец клавуланата калия массой 9,23 мг нагрели до 200°C и затем выдерживали в изотермических условиях в течение двух часов. Мониторинг измерений начался при 120°C, чтобы исключить эффект потери массы при выделении поверхностной воды.
На рис. 8 сравниваются потери массы, определенные по результатам измерений, с потерями, определенными по результатам прогнозирования (Kinetics Neo). Сравнение показывает хорошее согласие между двумя кривыми и, следовательно, надежность расчета.
Заключение
Кинетика термического разложения клавуланата калия в твердом состоянии под азотом исследована с помощью термогравиметрии и Kinetics Neo. Высокий уровень корреляции между измеренными и смоделированными данными был получен при использовании последовательной пятиступенчатой кинетической модели, где каждая ступень имеет n-й порядок. Это позволяет прогнозировать поведение при хранении при различных температурах, температурных профилях и периодах.
Результаты подтверждаются путем сравнения измерений ТГА при заданном температурном профиле, включая изотермический участок, с прогнозами, рассчитанными с помощью Kinetics Neo.