
23.02.2023 by Prof. Dr. Michael Gasik (Aalto University Helsinki, Finland)
DMA o biomateriálech: Vidět neviditelné!
Článek prof. dr. Michaela Gasika (Aalto University Helsinki, Finsko)
V současné době je k dispozici mnoho typů biomateriálů pro použití v různých implantátech, zejména v ortopedických a stomatologických případech. Používají se kovové slitiny, keramika a kompozity, ať už s živými buňkami nebo bez nich. Rozšiřuje se oblast použití různých scaffoldů používaných v aplikacích tkáňového inženýrství k podpoře a podpoře tvorby nových tkání a mnohé z nich se vyrábějí pomocí 3D (bio)tisku. Je známo, že regenerace biologických tkání je jednou z nejnáročnějších výzev, která vyžaduje biomateriálové struktury se správnými biomechanickými vlastnostmi [1], jež napodobují chování in vivo [2]. Správné biomateriály pomáhají tělu při obnově poškozené tkáně a minimalizují související bolest a dobu hojení [3].
Tento článek Prof. Dr. Michaela Gasika (Aalto University Helsinki, Finsko) ukazuje novou aplikaci techniky dynamicko-mechanické analýzy (DMA) nazvané BEST(Biomaterials Enhanced Simulation Testing), která se používá pro charakterizaci a zlepšování biomateriálů a zdravotnických prostředků; tato metoda jde nad rámec známých klasických viskoelastických analýz.

Prof. Michael Gasik z Aalto University ve Finsku (katedra chemického a metalurgického inženýrství) se začal zabývat aplikacemi termické analýzy v roce 1985 a téměř stejně dlouho spolupracuje s NETZSCH-Gerätebau GmbH.
Zaměřil se na materiály pro vysokoteplotní aplikace a pro vodíkové technologie. Od roku 2000 se aktivně zabývá biomateriály, lékařskými přístroji a aplikacemi v regenerativní medicíně. V roce 2019 byl jmenován velvyslancem Evropské ortopedické výzkumné společnosti.
Prof. Michael Gasik je spoluzakladatelem společnosti Seqvera Ltd. a vynálezcem metody BEST - Biomaterials Enhanced Simulation Testing - která byla poprvé implementována do zařízení NETZSCH DMA.
Jedním z těžišť výzkumných aktivit Prof. Michaela Gasika je stanovení mechanických vlastností biomateriálů. V této souvislosti využívá data DMA získaná pomocí zařízení NETZSCH DMA 242 Artemis jako základ pro další výpočty k charakterizaci těchto materiálů. Přečtěte si více o jeho přístupu:
Výzvy
Byla již provedena řada studií a shromážděna klinická data týkající se tvaru, designu a stavu povrchu biomateriálů, stejně jako geometrie implantátů a jejich vhodnosti pro různé kvality a umístění tkání. Významné rozdíly byly zaznamenány i u implantovaných materiálů, které byly zdánlivě identické, ale pocházely z různých zdrojů [4]. Biomechanická charakterizace kostí a měkkých tkání je problematičtější než u kovových, keramických a polymerních materiálů. Publikované soubory dat často nejsou založeny na srovnatelných protokolech a podmínkách měření, což vede k nedostatečné konzistenci. Zobecnění těchto údajů je velmi obtížné nebo téměř nemožné, pokud jde o poskytnutí jednoduchých, robustních a relevantních informací.
Pro biomechanickou charakterizaci se obvykle vracíme k předpokladu, že materiál je typem elastické nebo viskoelastické hmoty, abychom mohli vlastnosti aproximovat na jednotlivá čísla, obvykle označovaná jako "Modul pružnostiKomplexní modul pružnosti (pružná složka), modul skladování nebo G' je "reálná" část vzorků celkového komplexního modulu pružnosti. Tato pružná složka udává pevnou nebo fázovou odezvu měřeného vzorku. modul pružnosti". To však vyhovuje pouze u lineárně pružných materiálů pro velmi small deformace a pokyny NPL [5] uvádějí devět metod výpočtu modulu pružnosti, které mohou vést k různým hodnotám. Naprostá většina biomateriálů a tkání zjevně není elastická, takže snaha uměle redukovat údaje na nějaká pevná čísla je značným zjednodušením: Jaký by byl například přínos znalosti "modulu pružnosti sliznice" v rozpětí od 0,1 do 680 MPa podle různých zdrojů?
Bohužel otázky související s účinky setrvačnosti (vysoké frekvence) nebo limity přístrojů (nízké frekvence) nejsou vždy dostatečně zdokumentovány v publikovaných zkušebních protokolech. I když se eliminuje setrvačnost přístroje, samotný vzorek bude mít vždy konečnou setrvačnost, což může způsobit artefakty způsobené difuzí hybnosti, viskoelastickými vlnami a sekundárními toky - to vše může porušit předpoklad homogenní a lineární deformace [6]. Složitější modely mají značný počet umělých parametrů přizpůsobení a provádění takových zkoušek v rámci stávajících norem, protokolů a ad hoc zkušebních metod je velmi obtížné z experimentálního hlediska [7].
U procesů, jako je 3D bioprinting, je třeba překonat několik výzev, jako je kontrola vlastností bioinků, řízení toku a jeho vlivu na životaschopnost buněk a zajištění optimálních biofyzikálních vlastností konstruktů po tisku a při implantaci [8]. Je zapotřebí vyšší rozlišení a rychlost s kontrolou v 3D mikroprostředí a je třeba dosáhnout optimální kombinace mechanických a transportních vlastností v rámci prostorového a časového měřítka; ty jsou potřebné zejména pro difuzně omezenou vaskularizaci. Nová nařízení o zdravotnických prostředcích (2017/745) vyžadují, aby bylo provedeno řádné mechanické hodnocení, což vede k dodržování nařízení o hodnocení zdravotnických technologií (2021/2282).
Bohužel mnoho různých metod biofyzikálního testování poskytuje poměrně odlišné výsledky a není snadné získat realistické, skutečné vlastnosti. Příčin rozdílů je mnoho - nerovnoměrný kontakt, fázový stav, vliv setrvačnosti a pružné nestability, přizpůsobení pomocí nesprávně předpokládaných modelů, omezení v definici deformace, nedostatečné posouzení historie zatížení atd. Proto je velmi důležité mít robustní přístup, který dokáže kvantifikovat chování biomateriálu i jeho vlastnosti v procesu, a ne pouze generovat nějaká konkrétní čísla.
Koncepce BEST
Pro řešení těchto problémů jsme vyvinuli patentovanou metodu BEST(Biomaterials Enhanced Simulation Testing). Lze ji použít pro mnoho tvrdých i měkkých biomateriálů, včetně hydrogelů, 3D tištěných konstrukcí a řízeného podávání léčiv. Řešení BEST se zaměřuje na problémy způsobené zejména nesprávným a roztříštěným testováním a je založeno na integrovaném přístupu založeném na základním principu kauzality: "Před aplikací podnětu nedošlo k žádné odezvě vzorku."Metoda BESTje založena na principu kauzality
BEST se provádí za kontrolovaných podmínek s požadovanými koherentními podněty v prostředí DMA. Posuzuje změny vlastností vzorku v časové, fázové a stimulační oblasti [9]. Při následném zpracování BEST integruje data, konvolutuje historii vzorku a extrahuje neznámé hodnoty, a to vše bez toho, aby uživatel musel select model materiálu (analýza dat je v podstatě bezmodelová). Invariantní parametry získané pomocí vlastního algoritmu kvantové regrese zahrnují historii vzorku a ukazují polohu a směr vývoje biomateriálu [10].
Klíčovou vlastností BEST je invariantní zpracování dat DMA, které obvykle zůstává uživateli neprozkoumáno. Tato nová metoda překonává běžná omezení linearity vlastností tkání v mnoha modelech, konkrétně vlastnost škálování (homogenita) a vlastnost superpozice (aditivita), které obecně neplatí pro Fourierovu transformaci používanou v lineární viskoelasticitě.
Proto BEST používá správný zkušební protokol a používá idempotentní metody k extrakci parametrů z jednoho vzorku/testu, což vede k vysokým výstupním datům bez použití složité matematiky (není třeba v komplexních modulech) nebo předpokladu linearity a je schopen přepracovat i jiná reologická data tak, aby neztratila svou hodnotu.
Příklad aplikace DMA
V uvedeném příkladu byla výše popsaná metoda nasazena na základě měření provedených pomocí přístroje NETZSCH DMA 242 Artemis® k charakterizaci vlastností akrylátového hydrogelu pro 3D bioprint bez použití předpokládaného modelu. Gel byl umístěn do stříkačky o objemu 1 ml s jehlou 29G a nastaven do přizpůsobeného držáku vzorků DMA, který se obvykle používá pro ohýbání; byl testován v režimu postupného tečení při teplotě 25 °C.
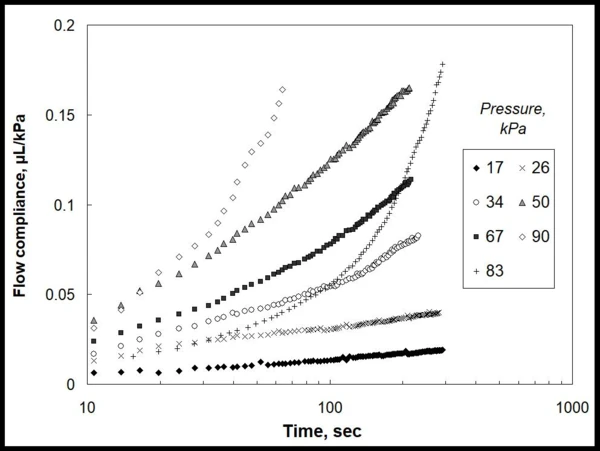
Obrázek 1 ukazuje experimentální údaje pro množství vytlačeného gelu (µl) definovanou jehlovou tryskou, normalizované na použitý lokální tlak (kPa). Tato data jasně odhalují nelinearitu kinetiky toku v závislosti na čase a aplikovaném tlaku a neexistuje žádný přímočarý způsob, jak select jakýkoliv materiálový model tyto závislosti popsat.
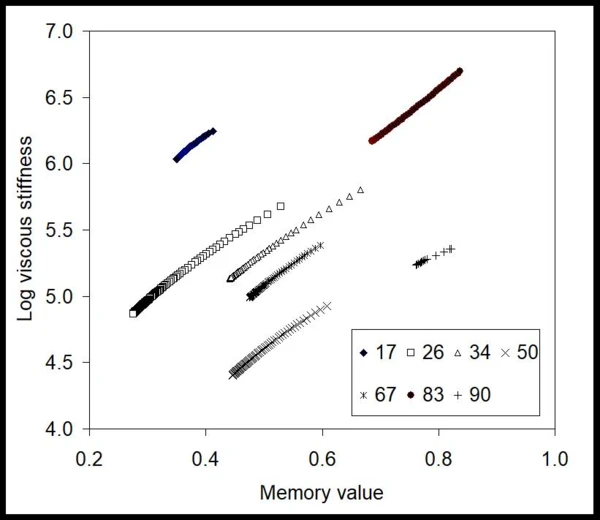
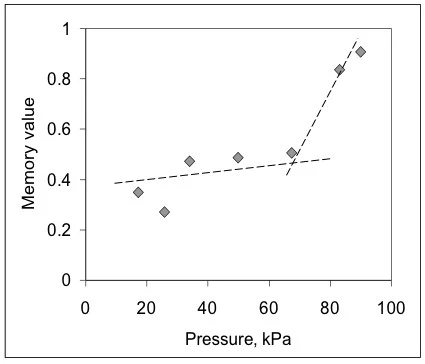
Z těchto údajů byly metodou BEST získány časově proměnné hodnoty viskózní tuhosti gelu za těchto podmínek vstřikování a také její paměťová hodnota [9,10] (obr. 2). Zde jsou křivky téměř lineární a sklony přímek jsou téměř konstantní pro všechny použité tlaky (čísla v kPa). To znamená, že gel, přestože vykazuje nenewtonovské chování, je lineární z hlediska bezmodelových invariantních hodnot. Je také vidět, že číselné hodnoty se mění s aplikovaným tlakem nemonotónně, což prozrazuje, že mohou existovat různé omezující jevy ovlivňující tok. Aby byl patrný vliv vývoje proudění, je na obr. 3 znázorněn graf závislosti hodnot paměti na aplikovaném tlaku. Tato mapa ukazuje, že gel v injekční stříkačce čelí tření, odporu proudění a případně i bezproudovému efektu při nízkých tlacích, kdy jsou hodnoty paměti mnohem nižší než jednotka. Po přibližně 65 kPa - počátek - tyto hodnoty vyskočí nahoru, což signalizuje, že gel dosahuje vyvinutějšího toku.
Představená metoda dokáže určit invariantní hodnoty a použít je při bezmodelové predikci procesů 3D biotisku v závislosti na trysce, geometrii, tlaku, čase a dalších podmínkách procesu, aniž by bylo nutné zvlášť určovat reologické parametry inkoustu. Metoda BEST generuje data "z první ruky" pro další prediktivní modelování procesu 3D tisku a stejnou filozofii uplatňuje i při charakterizaci 3D tištěných tkání a konstruktů.
SHRNUTÍ
Vyvinutý přístup prokazuje schopnost "vidět neviditelné" vlastnosti materiálů a jejich interakce s podněty a prostředím. Dynamicko-mechanická analýza (DMA) tak může poskytnout mnohem více informací než moduly pružnosti a ztrátový tangens. Pomocí zpracování BEST lze získat mnoho údajů pro různé účely (v některých případech dokonce z jediného vzorku nebo zkoušky). V rámci jediného experimentu je například možné získat modul agregátu; charakteristickou dobu Debory; poddajnost při plazení; efektivní difuzivitu a propustnost/permitivitu kapaliny; ekvivalentní velikost kanálu pro proudění kapaliny v dynamice; hodnotu materiálové paměti; tlak při bobtnání a další údaje. A to nejen u biomateriálů, protože aplikace BEST je bezmodelová a nevyžaduje žádné fitovací parametry; navíc ji lze použít i na již vytvořená zkušební data.
Literatura:
[Hubbell J.A. Nature Biotechnol. 13 (1995) 565-576.
[2] Gasik M. Sci. Techn. Adv. Mater. 18 (2017) 550-562.
[3] Chung C., Burdick J.A. Adv. Drug Delivery Rev. 60 (2008) 243-262.
[4] Gasik M., Lambert F., Bacevic M., Materiály 14 (2021) 2845.
[5] Lord J.D., Morrell R. Příručka správné praxe měření č. 98; NPL Teddington, Velká Británie (2006)
[6] Ewoldt R.H., Johnston M.T., Caretta L.M. In: Měřicí technika a měření: Komplexní tekutiny v biologických systémech; Springer, Německo (2015).
[7] Vrana N.E., Knopf-Marques H., Barthes J. (Eds.) Biomateriály pro regeneraci orgánů a tkání; Woodhead Publ. UK (2020).
[8] Jammalamadaka U., Tappa K. J. Funct. Biomater. 9 (2018) 22
[9] Gasik M., Bilotsky Y. Patent US 10379106 B2 (2019).
[10] Gasik M.Patent US 10809171 B2 (2020).
Kontakt:
Prof. Dr. Michael Gasik, Dr. Sci.
Terkko Health Hub, Building 14
Helsinki University Central Hospital Area
Haartmaninkatu 4, FIN-00290 Helsinki
www.seqvera.com
Děkujeme Prof. Dr. Michaelu Gasikovi za tento článek a nahlédnutí do jeho výzkumné práce.







