Introduzione
L'acido clavulanico viene utilizzato in combinazione con gli antibiotici del gruppo delle penicilline perché supera la resistenza agli antibiotici nei batteri che secernono ß-lattamasi, che altrimenti inattivano la maggior parte delle penicilline. Viene comunemente utilizzato sotto forma di sale di potassio, il clavulanato di potassio [1].
La conoscenza della degradazione del potassio clavulanato è fondamentale per migliorare la sua stabilità e quindi la sua durata di conservazione, che si riferisce all'intervallo di tempo in cui un prodotto farmaceutico può essere conservato senza diventare inadatto all'uso, al consumo o alla vendita [3].
Di seguito viene descritta un'indagine sul comportamento termico del clavulanato di potassio mediante DSC e TGA.
Condizioni di misura
Per la misurazione con NETZSCH DSC 204 F1 Phoenix® , il campione (2,67 mg) è stato riscaldato in una pentola di alluminio sigillata con coperchio forato a una velocità di riscaldamento di 10 K/min in un'atmosfera di azoto (40 ml/min) nell'intervallo di temperatura compreso tra -80°C e 250°C. La misurazione TGA è stata eseguita nelle stesse condizioni utilizzando il sistema NETZSCH TG 209 F1 Libra® tra la temperatura ambiente e i 600°C. La massa del campione è stata di 5,34 mg.
Risultati del test
La figura 2 illustra la misurazione DSC nell'intervallo di temperatura compreso tra la temperatura ambiente e 220°C. Il primo picco DSC a 77°C è associato a una perdita di massa dell'1,8% osservata nella misurazione TGA (figura 3). La forma di questo effetto ampio, il suo intervallo di temperatura e il fatto che si tratti di una reazione endotermica indicano il rilascio di acqua superficiale.
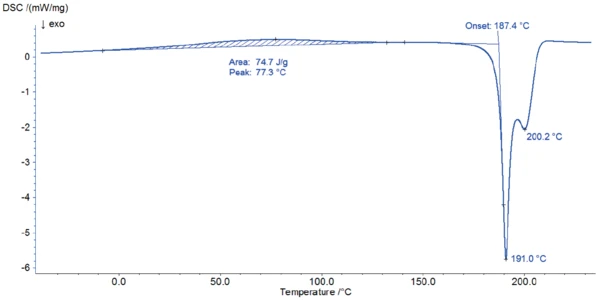
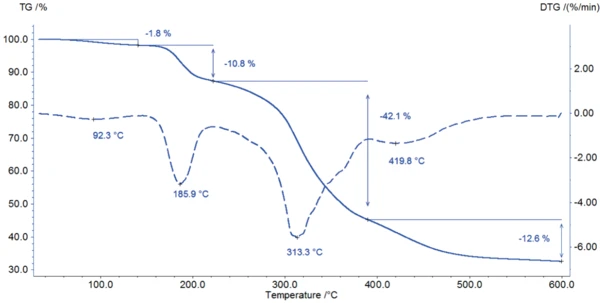
L'inizio della degradazione del clavulanato di potassio può essere rilevato con entrambi i metodi: Nella curva DSC, un forte effetto EsotermicoUna transizione campionaria o una reazione è esotermica se viene generato calore.esotermico inizia a 187°C (temperatura di inizio); a questa temperatura, la misurazione TGA registra una perdita di massa dell'11%.
La degradazione continua con una perdita di massa del 42% tra 200°C e 400°C (figura 3). Tra 400°C e 600°C, si raggiunge un'altra perdita di massa del 13%, con un tasso di Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. decomposizione massimo a 420°C.
Conclusione
Il riscaldamento del clavulanato di potassio a 600°C inizia con l'evaporazione dell'acqua adsorbita. Successivamente, la sostanza si degrada in tre fasi con tassi di Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. decomposizione massimi a 187°C, 313°C e 420°C. DSC e TGA sono metodi complementari. Una perdita di massa nella curva TGA associata a un effetto EndotermicoUna transizione campionaria o una reazione è endotermica se per la conversione è necessario il calore.endotermico nella curva DSC indica un rilascio di volatili. D'altra parte, la combinazione di una perdita di massa con un picco netto ed EsotermicoUna transizione campionaria o una reazione è esotermica se viene generato calore.esotermico nella curva DSC è piuttosto dovuta alla degradazione. Queste informazioni possono essere confermate dalle misure effettuate con la TGA accoppiata a un analizzatore di gas evoluti come il sistema FT-IR (si veda l'analisi TGA-FT-IR sul clavulanato di potassio in NETZSCH Application Note 118).