Bezpieczna kontrola procesu
Reakcje muszą pozostawać pod kontrolą przez cały czas, nie tylko w skali laboratoryjnej, zwykle mniejszej niż jeden litr, ale także - a nawet zwłaszcza - w reaktorach large, które produkują w skali ton. Nawet jeśli wystąpią nieplanowane zdarzenia, takie jak awaria pompy w cyklu chłodzenia reaktora, środki ostrożności muszą zostać podjęte już na etapie planowania zakładu produkcyjnego, aby zapobiec wymknięciu się reaktorów spod kontroli. Takie perspektywiczne planowanie, które uwzględnia również nieprzewidziane zdarzenia, umożliwia bezpieczną eksploatację zakładów produkcyjnych przez cały czas [1].
Najgorszy scenariusz
Już przed planowaniem zakładów produkcyjnych niezbędna jest ocena stosowanych chemikaliów i planowanych reakcji pod kątem ich potencjału zagrożenia. Aby uniknąć nieprzyjemnych niespodzianek związanych z rozmiarem i wydajnością instalacji, skalowaniem w górę, a nawet kolejnością dodawania reagentów, często przeprowadza się w tym celu badania opisujące Najgorszy scenariuszW odniesieniu do reaktora chemicznego, najgorszym scenariuszem jest sytuacja, w której wytwarzanie temperatury i/lub ciśnienia spowodowane reakcją wymyka się spod kontroli.najgorszy scenariusz. Znajomość najgorszego przypadku ułatwia kontrolowanie wszystkich rzeczywistych warunków produkcji. Najgorszym przypadkiem w odniesieniu do kontroli temperatury reaktora jest przekroczenie planowanej temperatury procesu z powodu, na przykład, awarii pompy w cyklu chłodzenia. Jeśli system chłodzenia ulegnie awarii, a ciepło reakcji nie może być zrównoważone, temperatura w reaktorze wzrasta powyżej planowanej temperatury reakcji. Może to prowadzić do niepożądanych reakcji ubocznych lub wtórnych. W najgorszym przypadku wzrost temperatury i/lub ciśnienia może spowodować rozerwanie reaktora. Aby zbadać, co się dzieje, gdy temperatura w reaktorze wzrasta w sposób niekontrolowany, jak szybko rośnie temperatura i jak duże ciśnienie narasta w reaktorze, takie reakcje są symulowane w skali small w laboratorium. Instrumentem zaprojektowanym do badania tego najgorszego przypadku jest NETZSCH ARC® 254.
NETZSCH ARC® 254
Kalorymetr NETZSCH ARC® 254 (rysunek 1) to kalorymetr przyspieszeniowy umożliwiający przeprowadzanie tzw. testów ucieczki termicznej. Celem tej technologii pomiarowej jest określenie niebezpiecznego potencjału w odniesieniu do temperatury próbki lub mieszaniny reakcyjnej w warunkach adiabatycznych. Adiabatyczność oznacza w szczególności brak wymiany ciepła. Jeśli całe ciepło reakcji pozostaje wewnątrz naczynia reakcyjnego i nie jest w stanie rozproszyć się do otoczenia, temperatura wzrośnie, a tym samym spowoduje wzrost prędkości reakcji. Spowoduje to samoprzyspieszający się mechanizm reakcji. Analizując takie scenariusze, można obliczyć i sklasyfikować wszelkie rzeczywiste warunki - które z reguły nie są w pełni adiabatyczne, ponieważ część ciepła jest zawsze tracona do otoczenia.

W jaki sposób wykrywana jest egzotermiczna reakcja samorozkładu?
Aby wykryć ucieczkę termiczną, temperatura badanej substancji lub mieszaniny reakcyjnej jest stopniowo zwiększana. Przy każdym kroku temperatury odczekuje się odpowiednią ilość czasu w celu odpuszczenia próbki do tej temperatury. Następnie wykrywa się, czy temperatura próbki pozostaje stała w tej temperaturze, czy też powoli rośnie, tj. czy występuje samonagrzewanie próbki, czy też nie. Jeśli nie zostanie wykryte samonagrzewanie, sekwencja stopniowego wzrostu temperatury (Heat-Wait-Search (HWS)Heat-Wait-Search to tryb pomiaru stosowany w urządzeniach kalorymetrycznych zgodnie z kalorymetrią przyspieszoną (ARC).Heat-Wait-Search) będzie kontynuowana. Po przekroczeniu szybkości samonagrzewania wynoszącej 0,02 K/min, urządzenie przechodzi w tzw. tryb AdiabatycznyTryb adiabatyczny opisuje system lub tryb pomiaru bez wymiany ciepła z otoczeniem. Tryb ten można zrealizować za pomocą urządzenia kalorymetrycznego zgodnie z metodą kalorymetrii przyspieszonej (ARC®). Głównym celem takiego urządzenia jest badanie scenariuszy i reakcji termicznych. Krótki opis trybu adiabatycznego to "brak ciepła na wejściu - brak ciepła na wyjściu".adiabatyczny. Ten tryb pomiaru zapobiega utracie ciepła do otoczenia próbki, ponieważ wszystkie grzałki otaczające komorę próbki podążają teraz za temperaturą próbki. Jeśli wszystkie grzałki mają taką samą temperaturę jak próbka, tj. nie ma gradientu temperatury, ciepło nie może być tracone do otoczenia. W ten sposób ARC® zapewnia adiabatyczne środowisko próbki w największym możliwym stopniu. To z kolei jest ważnym warunkiem wstępnym do zbadania najgorszego scenariusza, takiego jak Rozbieg termicznyUcieczka termiczna to sytuacja, w której reaktor chemiczny wymyka się spod kontroli w odniesieniu do wytwarzania temperatury i/lub ciśnienia spowodowanego samą reakcją chemiczną. Symulacja ucieczki termicznej jest zwykle przeprowadzana przy użyciu urządzenia kalorymetrycznego zgodnie z kalorymetrią przyspieszoną (ARC®).ucieczka termiczna.
Jak mierzy się reakcję ucieczki termicznej?
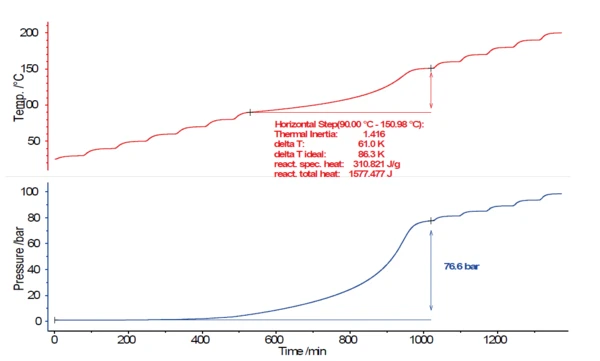
Jeśli podczas reakcji zaczyna występować Rozbieg termicznyUcieczka termiczna to sytuacja, w której reaktor chemiczny wymyka się spod kontroli w odniesieniu do wytwarzania temperatury i/lub ciśnienia spowodowanego samą reakcją chemiczną. Symulacja ucieczki termicznej jest zwykle przeprowadzana przy użyciu urządzenia kalorymetrycznego zgodnie z kalorymetrią przyspieszoną (ARC®).ucieczka termiczna, pożądane jest jak najwcześniejsze określenie tego krytycznego punktu w czasie lub temperaturze. Przeprowadzana sekwencyjnie, temperatura próbki będzie początkowo wzrastać bardzo powoli na początku samonagrzewania. 0.02 K/min to bardzo niskie tempo samonagrzewania, odpowiadające zaledwie 1,2 K na godzinę. Reakcja rozkładuReakcja rozkładu to wywołana termicznie reakcja związku chemicznego tworząca produkty stałe i/lub gazowe. Reakcja rozkładu rozpoczyna się powoli, ale stale zwiększa prędkość wraz ze wzrostem temperatury, aż do osiągnięcia maksymalnej szybkości samonagrzewania i wreszcie maksymalnej temperatury. Rysunek 3 przedstawia wyniki dla temperatury (czerwony) i ciśnienia (niebieski) dla testu Heat-Wait-Search (HWS)Heat-Wait-Search to tryb pomiaru stosowany w urządzeniach kalorymetrycznych zgodnie z kalorymetrią przyspieszoną (ARC®).HWS na 17,5% roztworze nadtlenku wodoru (H2O2). W tym celu objętość 5,0757 g roztworu nadtlenku wodoru umieszczono w kulistym pojemniku titanium (8,7 ml).
Jak wspomniano wcześniej, kryterium rozpoznania egzotermicznej reakcji rozkładu jest Szybkość samonagrzewaniaSpecjalny rodzaj kalorymetru jest wykorzystywany do wykrywania szybkości samonagrzewania się substancji. Metoda ta nazywana jest kalorymetrią przyspieszoną (ARC®). szybkość samonagrzewania > 0,02 K/min. Ta wartość progowa została przekroczona przy 90°C (początek), a następnie temperatura próbki wzrosła do 151°C w warunkach adiabatycznych. Podczas reakcji rozkładu ciśnienie wewnątrz naczynia z próbką wzrosło do 76,6 bara.
Czy istnieje sposób na powstrzymanie ucieczki termicznej?
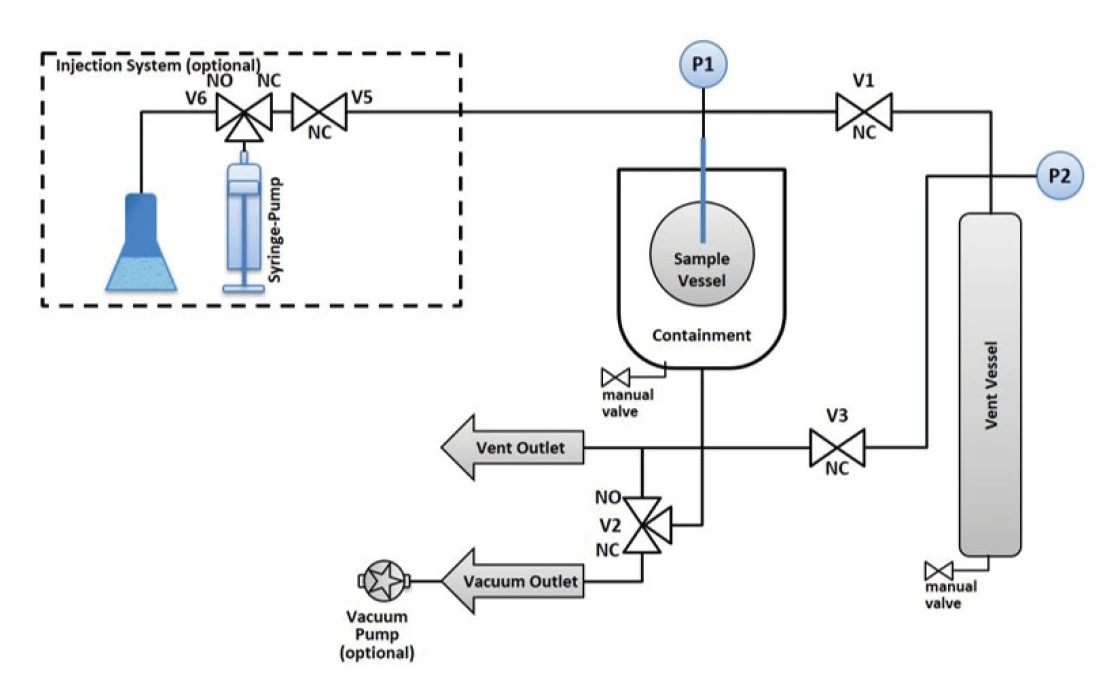
Pytanie, czy ucieczkę termiczną można zatrzymać, czy nie, jest oczywiście silnie związane z szybkością samonagrzewania. Konieczne jest wykrycie temperatury krytycznej lub początku ucieczki termicznej, ale być może nie zawsze jest pożądane, aby pozwolić reakcji rozkładu w pełni przebiegać. Znacznie ważniejsze byłoby poznanie temperatury lub ciśnienia, do którego reakcja, która już zaczęła ulegać niekontrolowanemu rozpadowi, może zostać ponownie zatrzymana i opanowana. Możliwość wykrycia początku termicznej ucieczki reakcji, a następnie zapobieżenia dalszemu samonagrzewaniu poprzez odcięcie środowiska adiabatycznego, a tym samym uniknięcie reakcji rozkładu, została już opisana w innym miejscu [2]. W tym miejscu należy podjąć próbę pokazania innego sposobu zatrzymania reakcji rozkładu, która właśnie się rozpoczęła, stosując inną strategię. Naczynie reakcyjne jest połączone przewodem ciśnieniowym i zaworem z innym naczyniem, tak zwanym naczyniem odpowietrzającym (rysunek 3). Po osiągnięciu dowolnie selectmożliwego ciśnienia próbki, oprogramowanie pomiarowe otworzy zawór do naczynia odpowietrzającego. Poprzez odpowietrzenie do tego naczynia, ciśnienie w naczyniu reakcyjnym powinno również spaść. Może to być wystarczające do zatrzymania samonagrzewania, a tym samym niekontrolowanych reakcji następczych i ubocznych.
Wentylacja
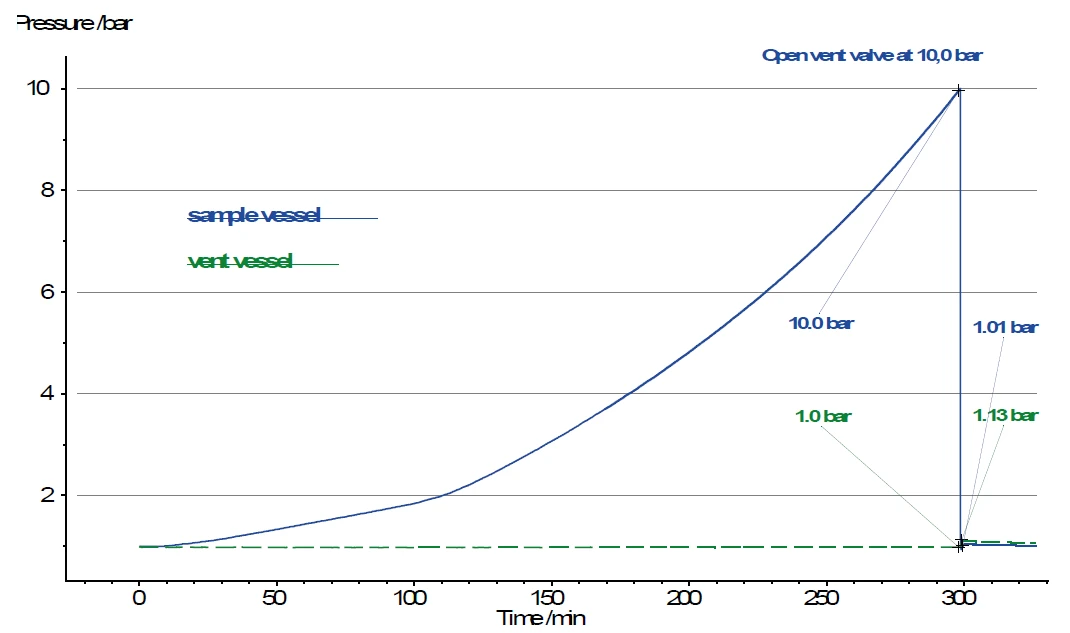
Zarówno zbiornik reakcyjny, jak i zbiornik odpowietrzający są wyposażone w indywidualny manometr. W ten sposób można śledzić wzrost ciśnienia po otwarciu zaworu (patrz V1 na rysunku 3). Objętość naczynia odpowietrzającego wynosząca 250 ml jest jednak wielokrotnie larger większa niż objętość naczynia z próbką, w którym zwykle około 5 ml gazu pozostaje nad próbką. Z tego powodu ciśnienie w naczyniu odpowietrzającym wzrasta tylko z 1,0 bar do 1,13 bar po otwarciu zaworu, podczas gdy ciśnienie w naczyniu z próbką spada z 10,0 bar do 1,0 bar w tym samym czasie (rysunek 4).
Rysunek 5 przedstawia wyniki pomiaru Heat-Wait-Search (HWS)Heat-Wait-Search to tryb pomiaru stosowany w urządzeniach kalorymetrycznych zgodnie z kalorymetrią przyspieszoną (ARC®).HWS z wodą jako substancją próbki, w którym sygnał ciśnienia wzrasta analogicznie do sygnału temperatury i zgodnie ze stopniami temperatury programu Heat-Wait-Search (HWS)Heat-Wait-Search to tryb pomiaru stosowany w urządzeniach kalorymetrycznych zgodnie z kalorymetrią przyspieszoną (ARC®).HWS. W tym przykładzie otwarcie zaworu odpowietrzającego zostało zaprogramowane przez oprogramowanie pomiarowe na 2,0 bar. Można łatwo zauważyć, że po otwarciu naczynia odpowietrzającego ciśnienie w naczyniu z próbką nie tylko spada z 2,0 bar do 1,0 bar, ale także znacznie spada temperatura w naczyniu z próbką. W okresie 60 minut, w którym zawór odpowietrzający pozostaje otwarty, grzałki otaczające kalorymetr również podążają za temperaturą próbki. Spada ona z 108,4°C do 96,8°C i - mimo że tryb pomiaru adiabatycznego pozostaje aktywowany w tym czasie, tj. otaczające grzejniki podążają za temperaturą próbki - nie można określić dalszego wzrostu temperatury próbki.
Teraz, badając wodę jako substancję próbki, można oczekiwać, że nie będzie reakcji egzotermicznej. Zamiast tego potwierdzono, że gdy próbka nie reaguje egzotermicznie, temperatura próbki spada po otwarciu zaworu odpowietrzającego, a następnie pozostaje stała ze względu na adiabatyczne otoczenie. Potwierdza to również Szybkość samonagrzewaniaSpecjalny rodzaj kalorymetru jest wykorzystywany do wykrywania szybkości samonagrzewania się substancji. Metoda ta nazywana jest kalorymetrią przyspieszoną (ARC®). szybkość samonagrzewania się próbki w dolnej części rysunku.
Badanie jednoprocentowego roztworu nadtlenku wodoru również nie wykazało dalszego wzrostu temperatury po otwarciu zaworu odpowietrzającego przy ciśnieniu 3 barów w zbiorniku próbki. W przypadku dwuprocentowego roztworu nadtlenku wodoru można już zauważyć, że egzotermiczna Reakcja rozkładuReakcja rozkładu to wywołana termicznie reakcja związku chemicznego tworząca produkty stałe i/lub gazowe. reakcja rozkładu spowodowana otwarciem zaworu odpowietrzającego i obniżeniem ciśnienia w układzie do ciśnienia atmosferycznego nie jest wystarczająca do całkowitego powstrzymania dalszego rozkładu. Skutkuje to szybkością samonagrzewania wynoszącą 0,02 K/min. W przypadku czteroprocentowego roztworu nadtlenku wodoru (rysunek 6) po otwarciu zaworu odpowietrzającego nadal wykrywana jest Szybkość samonagrzewaniaSpecjalny rodzaj kalorymetru jest wykorzystywany do wykrywania szybkości samonagrzewania się substancji. Metoda ta nazywana jest kalorymetrią przyspieszoną (ARC®). szybkość samonagrzewania wynosząca 0,04 K/min. Temperatury i szybkości samonagrzewania dla omawianych roztworów nadtlenku wodoru podsumowano w tabeli 1.
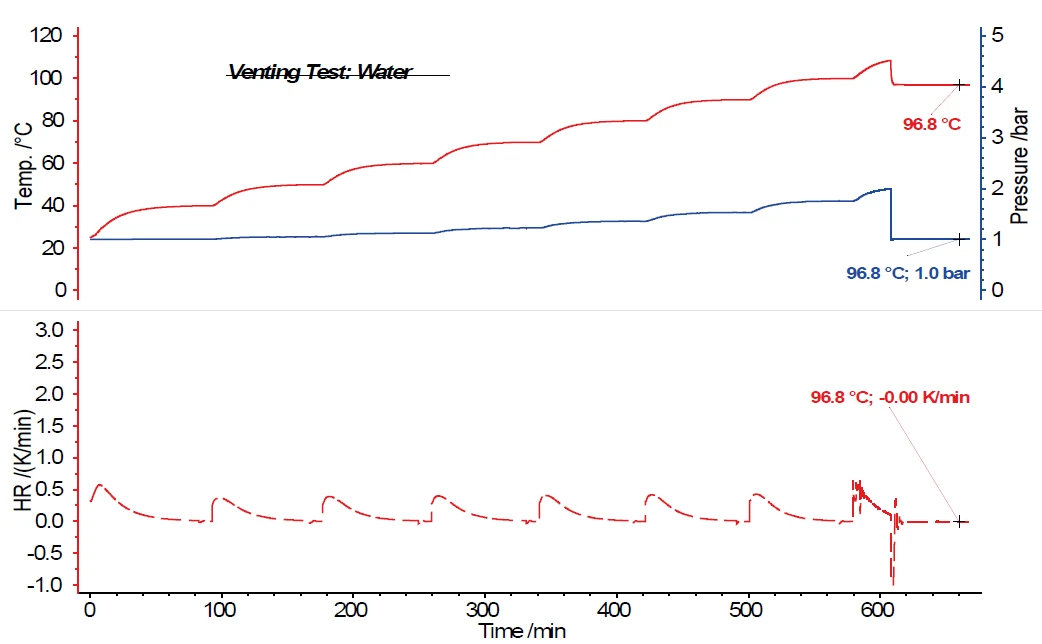
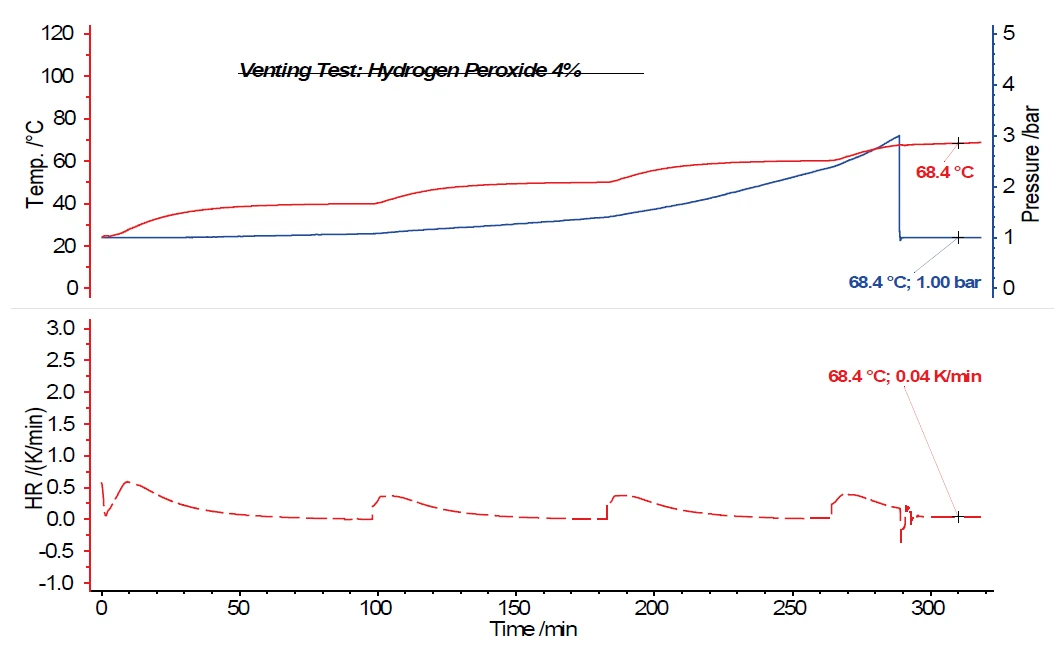
Tabela 1: Podsumowanie temperatury i szybkości samonagrzewania dla różnych roztworów nadtlenku wodoru
| Próbka | Temperatura podczas odpowietrzania | Szybkość samonagrzewaniaSpecjalny rodzaj kalorymetru jest wykorzystywany do wykrywania szybkości samonagrzewania się substancji. Metoda ta nazywana jest kalorymetrią przyspieszoną (ARC®). Szybkość samonagrzewania po odpowietrzeniu |
| H2O | 108.4°C (2 bar) | 0.00 K/min |
| H2O2 (1%) | 81.8°C (3 bar) | 0.00 K/min |
| H2O2 (2%) | 70.8°C (3 bar) | 0.02 K/min |
| H2O2 (4%) | 67.6°C (3 bar) | 0.04 K/min |
Podsumowanie
System NETZSCH ARC® 254 oferuje dwie możliwości odzyskania kontroli, jeśli to konieczne, nad reakcjami, w których rozpoczął się już niekontrolowany wzrost temperatury. Jedną z możliwości jest ta, w której otaczające grzejniki są wyłączane, gdy próbka osiągnie określoną Szybkość samonagrzewaniaSpecjalny rodzaj kalorymetru jest wykorzystywany do wykrywania szybkości samonagrzewania się substancji. Metoda ta nazywana jest kalorymetrią przyspieszoną (ARC®). szybkość samonagrzewania, eliminując w ten sposób adiabatyczne środowisko próbki i umożliwiając ponowne straty ciepła; dalsza ucieczka reakcji jest następnie powstrzymywana przez te straty ciepła [2]. Druga możliwość, w której ciśnienie może zostać usunięte z naczynia z próbką do innego naczynia z próbką (naczynia odpowietrzającego) poprzez otwarcie zaworu nadmiarowego ciśnieniowego (zaworu odpowietrzającego), została przedstawiona w niniejszej nocie aplikacyjnej. Poprzez niezależny pomiar ciśnienia można monitorować wzrost ciśnienia w naczyniu odpowietrzającym. Wykazano, że dalszy postęp słabo egzotermicznych reakcji rozkładu może zostać zatrzymany, podczas gdy silniej egzotermiczne reakcje nadal wykazują wykrywalne samonagrzewanie nawet po zwolnieniu ciśnienia.