Inhärent sichere Prozessführung
Nicht nur im Labormaßstab von üblicherweise weniger als einem Liter müssen Reaktionen jederzeit kontrollierbar bleiben, sondern gerade auch in großen Reaktoren, die im Tonnenmaßstab produzieren. Selbst für das Eintreten von ungeplanten Ereignissen, wie dem Defekt einer Pumpe im Kühlkreislauf eines Reaktors, müssen bereits bei der Planung der Produktionsanlage Vorkehrungen getroffen werden, um zu verhindern, dass Reaktoren außer Kontrolle geraten können. Diese vorausschauende Planung, die auch außerplanmäßige Ereignisse berücksichtigt, ermöglicht den jederzeit sicheren, den inhärent sicheren Betrieb von Produktionsanlagen [1].
Worst-Case-Szenario
Schon vor der Planung von Produktionsanlagen ist es unerlässlich, die verwendeten Chemikalien und die geplanten Reaktionen hinsichtlich ihres Gefährdungspotentials zu bewerten. Um bei der Größe und der Auslastung der Anlagen, beim Up-scaling oder auch bei der Reihenfolge der Zugabe der Reaktionspartner keine unangenehmen Überraschungen zu erleben, werden dazu häufig Untersuchungen durchgeführt, die den schlimmsten anzunehmenden Fall, den Worst Case, beschreiben. Wenn man den schlimmsten Fall kennt, kann man alle realen Produktionsbedingungen besser beherrschen. Der Worst Case im Hinblick auf die Temperaturführung eines Reaktors ist das Überschreiten der geplanten Prozesstemperatur, etwa durch das Ausfallen einer Pumpe im Kühlkreislauf. Wenn die Kühlung ausfällt und die Reaktionswärme nicht mehr abgeführt werden kann, dann steigt die Temperatur im Reaktor über die geplante Reaktionstemperatur und ReaktionsenthalpieReaktionstemperatur und Reaktionsenthalpie können mit z.B. mit Hilfe der dynamischen Differenz Thermoanalyse (DSC) bestimmt werden. Das Verfahren dazu ist z.B. in der DIN EN ISO 11357-5 beschrieben.Reaktionstemperatur an. Dies kann zu unerwünschten Nebenreaktionen oder Folgereaktionen führen. Im schlimmsten Fall können Temperatur- und/ oder Druckanstieg zum Bersten des Reaktors führen. Um zu untersuchen, was passiert, wenn die Temperatur im Reaktor unkontrolliert ansteigt, wie schnell die Temperatur ansteigt und wie viel Druck sich dabei im Reaktor aufbaut, werden solche Reaktionen im kleinen Maßstab im Labor nachgestellt. Eine Apparatur, die so konzipiert ist, dass sie diesen Worst Case untersuchen kann, ist das NETZSCH Accelerating Rate Calorimetry (ARC)Die Methode, die isotherme und adiabatische Testverfahren beschreibt, wird zur Detektion thermisch induzierter Zersetzungsreaktionen eingesetzt. Das Standardverfahren ist Heat-Wait-Search (HWS.ARC® 254.
Das NETZSCH ARC® 254
Das NETZSCH ARC® 254 (Abbildung 1) ist ein Accelerating Rate Kalorimeter, mit dem das sogenannte thermische Durchgehen untersuchen werden kann. Ziel dieser Messtechnologie ist es, das Gefährdungspotenzial im Hinblick auf die Temperatur einer Probe oder einer Reaktionsmischung unter adiabatischen Bedingungen zu untersuchen. Insbesondere bedeutet Adiabatizität, dass kein Wärmeaustausch stattfindet. Bleibt die Reaktionswärme im Reaktionsbehälter und kann keine Wärme an die Umgebung abgeben werden, steigt die Temperatur und somit die Reaktionsgeschwindigkeit. Dies führt zu einem selbstbeschleunigenden Reaktionsmechanismus. Wird dieses Szenario untersucht oder ist dieses bekannt, können alle realen Bedingungen, die in der Regel nicht völlig AdiabatischAdiabatisch beschreibt ein System oder einen Messmodus ohne Wärmeaustausch mit der Umgebung.adiabatisch sind, da sie immer gewisse Wärmeverluste an die Umgebung aufweisen, berechnet und klassifiziert werden.

Wie kann man den Beginn einer exothermen Selbstzersetzungsreaktionerkennen?
Um das thermische Durchgehen zu erkennen, wird die Temperatur der zu untersuchenden Substanz oder der Reaktionsmischung schrittweise erhöht. Bei jeder Temperaturstufe wird ausreichend lange gewartet, um die Probe auf diese Temperatur zu temperieren. Anschließend wird detektiert, ob die Probentemperatur bei dieser Temperatur konstant bleibt, oder ob sie langsam ansteigt, ob also eine Selbsterwärmung der Probe auftritt oder nicht. Wird keine Selbsterwärmung festgestellt, wird diese Sequenz der schrittwiesen Temperaturerhöhung (Heat-Wait-Search (HWS)HWS ist die Bezeichnung für eine Sequenz, die die Probe auf eine bestimmte Temperatur aufheizt (Heat), eine thermische Stabilisierung des Systems ermöglicht (Wait) und schließlich erkennt (Search), ob ein Anstieg der Probentemperatur festgestellt wird, der durch eine exotherme Zersetzungsreaktion der Probe verursacht wird.Heat-Wait-Search) fortgesetzt. Bei einer Überschreitung der SelbsterwärmungsrateUm die Selbsterwärmungsrate einer Substanz zu detektieren wird eine spezielle Art Kalorimeter verwendet. Die damit verbundene Methode wird Accelerating Rate Calorimetry (ARC) genannt.Selbsterwärmungsrate von 0,02 K/ min wechselt die Apparatur in den sogenannten adiabatischen Modus. Dieser Messmodus verhindert Wärmeverluste an die Probenumgebung, da alle Heizer, die den Probenraum umgeben, nun der Probentemperatur folgen. Haben alle Heizer die gleiche Temperatur wie die Probe, gibt es also keinen Temperaturgradienten, kann somit keine Wärme an die Umgebung abgegeben werden. Auf diese Weise stellt die ARC®-Apparatur eine weitestgehend adiabatische Probenumgebung sicher. Diese wiederum ist eine wichtige Voraussetzung für die Untersuchung eines Worst-Case-Szenarios wie das thermische Durchgehen.
Wie untersucht man eine Reaktion des thermisches Durchgehens?
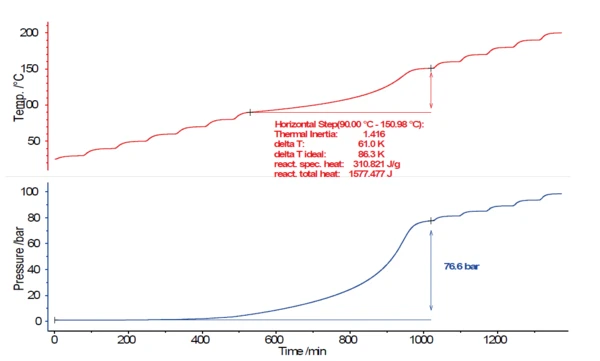
Setzt bei einer Reaktion das thermische Durchgehen ein, so möchte man diesen kritischen Zeitpunkt bzw. diese Temperatur möglichst rechtzeitig bestimmen. Folgerichtig steigt die Probentemperatur bei Beginn der Selbsterwärmung zunächst nur sehr langsam an. 0.02 K/min ist eine sehr geringe Selbsterwärmungsrate, sie entspricht nur 1,2 K pro Stunde. Die ZersetzungsreaktionEine Zersetzungsreaktion ist eine thermisch induzierte Reaktion einer chemischen Substanz, die fest und/oder gasförmige Zersetzungsprodukte bildet.Zersetzungsreaktion beginnt langsam, nimmt jedoch mit steigender Temperatur kontinuierlich an Geschwindigkeit zu, bis sie ihre maximale Eigenerwärmungsrate und schließlich die maximale Temperatur erreicht. Abbildung 2 zeigt die Ergebnisse für die Temperatur (rot) und den Druck (blau) für einen Heat-Wait-Search (HWS)HWS ist die Bezeichnung für eine Sequenz, die die Probe auf eine bestimmte Temperatur aufheizt (Heat), eine thermische Stabilisierung des Systems ermöglicht (Wait) und schließlich erkennt (Search), ob ein Anstieg der Probentemperatur festgestellt wird, der durch eine exotherme Zersetzungsreaktion der Probe verursacht wird.HWS-Test an einer 17,5 %-igen Wasserstoffperoxidlösung (H2O2). Dazu wurden 5,0757 g der Wasserstoffperoxidlösung in einen kugelförmigen Titanbehälter (8,7 ml) eingebracht.
Wie bereits vorher erwähnt, ist das Kriterium zur Erkennung einer exothermen Zersetzungsreaktion eine Selbsterwärmungsrate >0,02 K/min. Dieser Schwellenwert wurde bei 90 °C überschritten (Onset) und anschließend steigt die Probentemperatur unter adiabatischen Bedingungen bis auf 151 °C an. Während der Zersetzungsreaktion erhöhte sich der Druck innerhalb des Probenbehälters auf 76,6 bar.
Lässt sich das thermische Durchgehen stoppen?
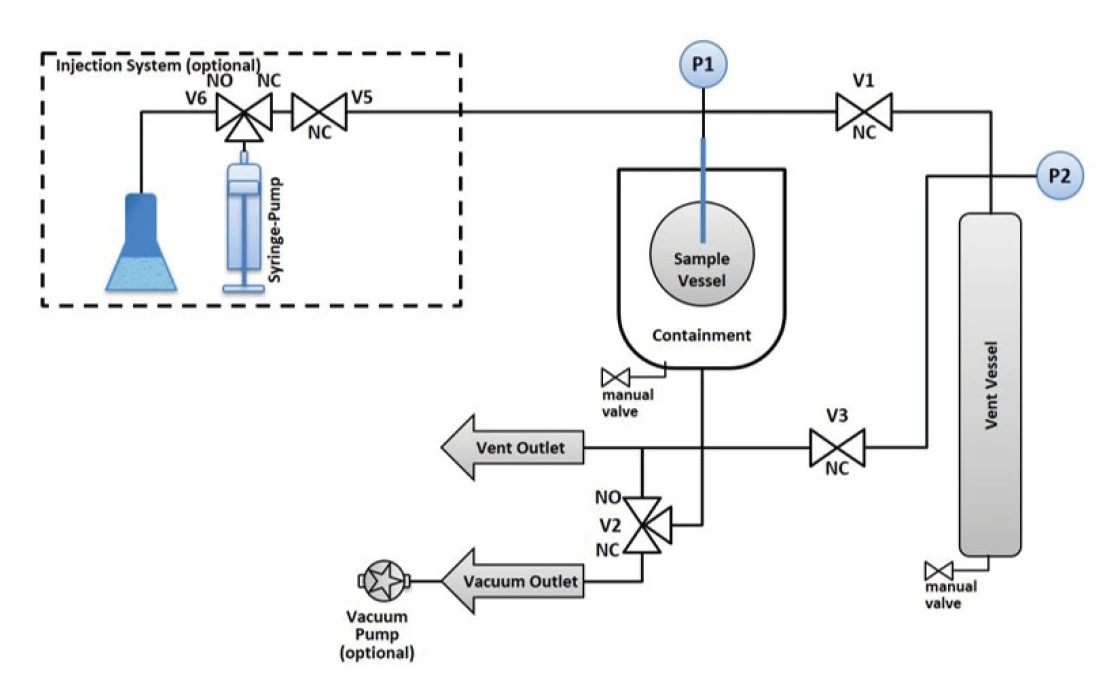
Die Frage, ob ein thermisches Durchgehen gestoppt werden kann oder nicht, ist natürlich eng verbunden mit der Selbsterwärmungsrate. Es ist zwar notwendig, die kritische Temperatur oder den Beginn des thermischen Durchgehens zu detektieren, es ist jedoch vielleicht nicht immer wünschenswert, die Zersetzungsreaktion dann auch vollständig stattfinden zu lassen. Viel wichtiger wäre zu wissen, bis zum Erreichen welcher Temperatur oder welches Drucks sich eine bereits durchgehende Reaktion wieder stoppen und unter Kontrolle bringen lässt. Über die Möglichkeit, das Durchgehen eines Reaktionsansatzes zu erkennen und anschließend durch Abschalten der adiabatischen Umgebung die weitere Selbsterwärmung zu verhindern und so die Zersetzungsreaktion zu vermeiden, wurde bereits an anderer Stelle berichtet [2]. Hier soll versucht werden, durch Verfolgen einer anderen Strategie einen weiteren Weg aufzuzeigen, eine gerade beginnende Zersetzungsreaktion wieder zu stoppen. Der Reaktionsbehälter ist über eine Druckleitung und ein Ventil mit einem weiteren Behälter, dem sogenannten Venting-Behälter, verbunden (Abbildung 3). Bei Erreichen eines frei wählbaren Probendrucks wird von der Messsoftware das Ventil zum Venting-Behälter geöffnet. Durch das Entspannen in diesen Behälter sollte der Druck im Reaktionsbehälter ebenfalls sinken. Dies könnte ausreichen, um die Selbsterwärmung und damit die unkontrollierten Folge- und Nebenreaktionen zu unterbinden.
Venting
Neben dem Reaktionsgefäß ist auch der Venting-Behälter mit einer unabhängigen Druckmessröhre ausgestattet. So kann dort der Druckanstieg nach dem Öffnen des Ventils (siehe V1 in Abbildung 3) verfolgt werden. Allerdings ist das Volumen des Venting-Behälters mit 250 ml um eine Vielfaches größer als das Volumen des Probenbehälters, bei dem typischerweise über der Probe etwa 5 ml Gasvolumen verbleiben. Aus diesem Grund steigt nach dem Öffnen des Ventils der Druck im Venting-Behälter lediglich von 1,0 bar auf 1,13 bar, während der Druck im Probenbehälter gleichzeitig von 10,0 bar auf 1,0 bar abfällt (Abbildung 4).
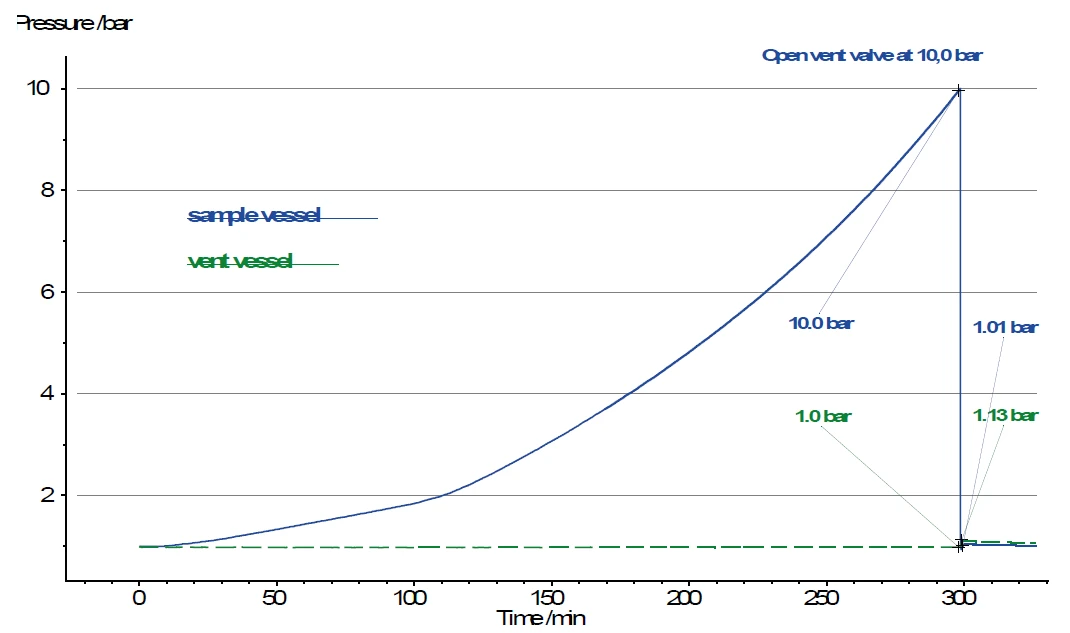
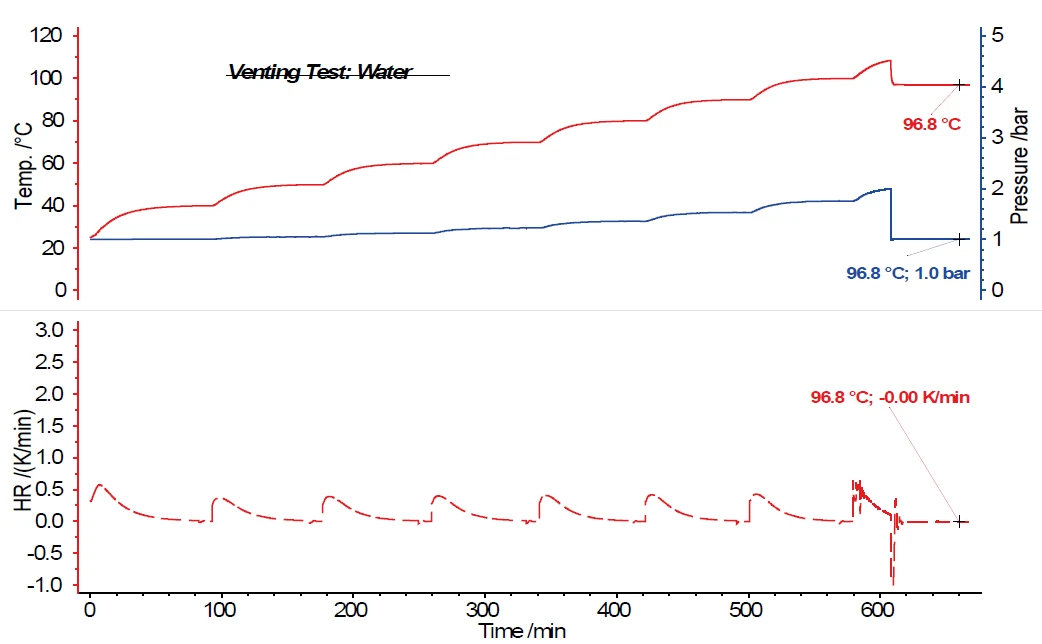
Abbildung 5 zeigt die Ergebnisse einer HWS-Messung mit Wasser als Probensubstanz, bei der das Drucksig-nal analog zum Temperatursignal und entsprechend der Temperaturstufen des HWS-Programms ansteigt. In diesem Beispiel wurde das Öffnen des Venting-Ventils über die Messsoftware bei 2,0 bar programmiert. Es ist leicht zu erkennen, dass mit dem Öffnen des Ven-ting-Ventils nicht nur der Druck im Probenbehälter von 2,0 bar auf 1,0 bar abfällt, sondern dass damit auch die Temperatur im Probenbehälter stark abnimmt. Über einen Zeitraum von 60 min, in dem das Venting-Ventil geöffnet bleibt, folgen auch die Umgebungsheizer des Kalorime-ters der Probentemperatur. Diese fällt von 108,4 °C auf 96,8 °C ab und, obwohl der adiabatische Messmodus während dieser Zeit aktiviert bleibt, was bedeutet, dass die Umgebungsheizer der Probentemperatur fol-gen, ist kein erneuter Anstieg der Probentemperatur festzustellen.
Nun kann man bei der Untersuchung von Wasser als Test-substanz auch keine exotherme Reaktion erwarten. Es ist hier vielmehr die Bestätigung gelungen, dass ohne eine exotherme Reaktion der Probe die Probentemperatur nach Öffnen des Venting-Ventils absinkt und anschlie-ßend aufgrund der adiabatischen Umgebung konstant bleibt. Dies wird auch durch die Selbsterwärmungsrate der Probe im unteren Teil der Abbildung bestätigt.
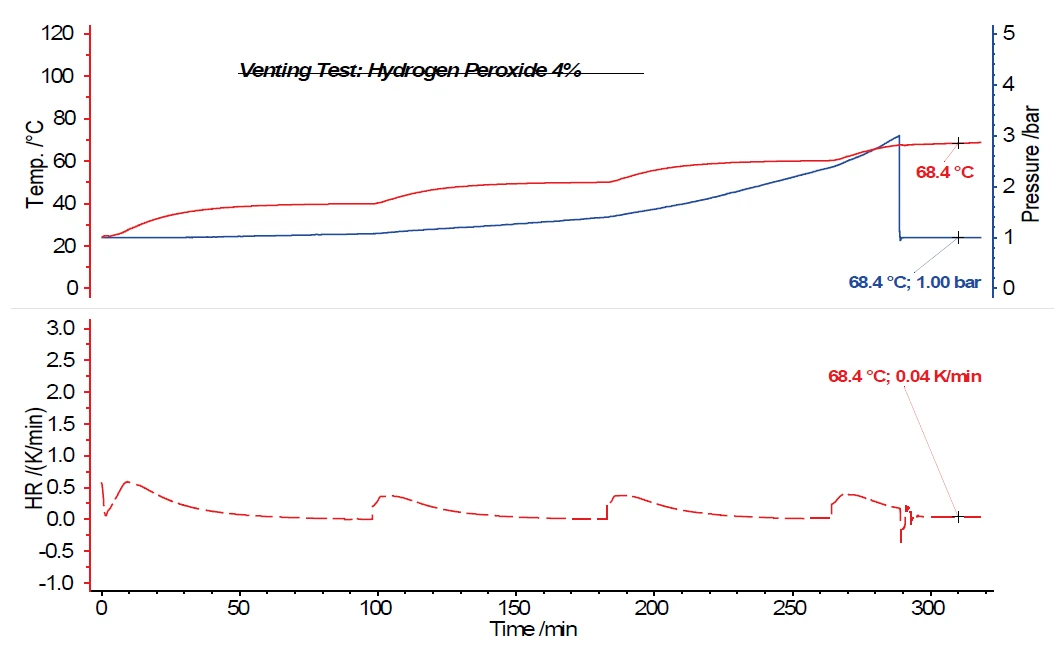
Die Untersuchung einer einprozentigen Wasserstoff-peroxidlösung zeigt ebenfalls keinen weiteren Tempe-raturanstieg nach Öffnen des Venting-Ventils bei 3 bar Druck im Probenbehälter. Bei einer zweiprozentigen Wasserstoffperoxidlösung ist bereits erkennbar, dass die exotherme Zersetzungsreaktion durch das Öffnen des Venting-Ventils und das Entspannen des Systems auf Atmosphärendruck nicht ausreicht, um die weitere Zersetzung vollständig zu unterbinden. Es resultiert eine Selbsterwärmungsrate von 0,02 K/min. Bei einer vierprozentigen Wasserstoffperoxidlösung (Abbildung 6) wird nach dem Öffnen des Venting- Ventils noch eine Selbsterwärmungsrate von 0,04 K/min. detektiert. Die Temperaturen und die Selbster- wärmungsraten für die diskutierten Wasserstoffperoxid-lösungen sind in Tabelle 1 zusammengefasst.
Tab.1 Zusammenfassung von Temperatur und Selbsterwärmungsrate für verschiedene Wasserstoffperoxidlösungen
| Probe | Temperatur beim Venting | Selbsterwärmungsrate nach dem Venting |
| H2O | 108,4 °C (2 bar) | 0.00 K/min |
| H2O2 (1%) | 81,8 °C (3 bar) | 0.00 K/min |
| H2O2 (2%) | 70,8 °C (3 bar) | 0.02 K/min |
| H2O2 (4%) | 67,6 °C (3 bar) | 0.04 K/min |
Zusammenfassung
Das NETZSCH ARC® 254 bietet zwei Möglichkeiten, um gegebenenfalls Reaktionen wieder unter Kontrolle zu bringen, bei denen ein Thermisches Durchgehen / Thermal runawayEin thermisches Durchgehen ist eine Situation, in der ein chemischer Reaktor bezüglich der durch die chemische Reaktion verursachten Temperatur- und/oder Druckerzeugung außer Kontrolle geraten ist. Die Simulation eines thermischen Durchgehens wird in der Regel mit einem Kalorimeter gemäß der Accelerated Rate Calorimetry (ARC) durchgeführt.Thermisches Durchgehen, also ein Thermal Runaway bereits begonnen hat. Die eine Möglichkeit, bei der bei einer bestimmten Selbsterwär-mungsrate der Probe die Umgebungsheizer abgeschal-tet werden, die adiabatische Umgebung der Probe also weggenommen wird und damit Wärmeverluste wieder möglich werden, kann, über eben diese Wärmeverluste, das weitere Durchgehen der Reaktion abfangen [2]. Die andere Möglichkeit, bei der über das Öffnen eines Über-druckventils (Venting-Ventil) Druck aus dem Proben-behälter in einen anderen Behälter (Venting-Behälter) abgeführt werden kann, wurde in dieser Arbeit vorge-stellt. Durch eine unabhängige Druckmessung lässt sich der Druckanstiegt im Venting-Behälter verfolgen. Es hat sich gezeigt, dass der weitere Verlauf von schwach exo-therme Zersetzungsreaktionen dadurch zu unterbin-den ist, während stärker exotherme Reaktionen auch nach der Druckentlastung weiterhin eine detektierbare Selbsterwärmung zeigen.