Der patentierte VariPhi-Heizer zur Variation des Ф-Faktors während der Untersuchung eines „Thermal Runaway“
Accelerating Rate Calorimetry (Accelerating Rate Calorimetry (ARC)Die Methode, die isotherme und adiabatische Testverfahren beschreibt, wird zur Detektion thermisch induzierter Zersetzungsreaktionen eingesetzt. Das Standardverfahren ist Heat-Wait-Search (HWS.ARC®) ist eine Methode zur Untersuchung von Worst-Case-SzenarienIm Zusammenhang mit einem chemischen Reaktor ist ein Worst-Case-Szenario die Situation, in der die durch die Reaktion verursachte Temperatur und/oder Druckerzeugung außer Kontrolle gerät.Worst-Case-Szenarien und des thermischen Durchgehens (thermal runaway). Im Gegensatz zu anderen kalorischen Techniken wie Reaktionskalorimetrie, Verbrennungskalorimetrie oder dynamische Differenz-Kalorimetrie (engl. Differential Scanning Calorimetry, DSC) erlauben Geräte vom Typ Accelerating Rate Calorimetry (ARC)Die Methode, die isotherme und adiabatische Testverfahren beschreibt, wird zur Detektion thermisch induzierter Zersetzungsreaktionen eingesetzt. Das Standardverfahren ist Heat-Wait-Search (HWS.ARC® eine weitgehend adiabatische Probenumgebung. Adiabatizität ist unerlässlich, um schlimmst mögliche Reaktionsverläufe beobachten zu können. Zersetzungsreaktionen, die in diesem Zusammenhang von besonderem Interesse sind, erzeugen Wärme und Druck, da die Reaktionen typischerweise stark ExothermEin Phasenübergang oder eine Reaktion ist exotherm, wenn von der Probe Wärme freigesetzt wirdexotherm sind und Zersetzungsgase bilden. Die adiabatische Probenumgebung innerhalb eines Kalorimeters vom Typ ARC® wird über eine Anordnung von Heizern, die den Probenraum umgeben, und eine intelligente Temperaturführung realisiert. Ein Ziel ist die Bestimmung der Temperatur, bei der die Eigenzersetzung einer Probe oder eines Probengemisches einsetzt. Ein weiteres Ziel ist es, einen Wärmeaustausch zwischen Probe und Umgebung zu vermeiden, sobald die exotherme ZersetzungsreaktionEine Zersetzungsreaktion ist eine thermisch induzierte Reaktion einer chemischen Substanz, die fest und/oder gasförmige Zersetzungsprodukte bildet.Zersetzungsreaktion beginnt. Übersteigt die Eigenerwärmungsrate einen gewissen Schwellenwert (der typischerweise im Bereich von 0,02 K/min liegt), folgen alle die Probe umgebenden Heizer der Probentemperatur. Ohne Wärmeaustausch wird keine Wärme an die Umgebung abgeführt, die gesamte Reaktionswärme bleibt in der Probe und erhöht somit die Probentemperatur. Je höher die Probentemperatur steigt, desto schneller verläuft die Reaktion. Mit Hilfe eines solchen Experiments können nicht nur die Anfangstemperatur der ZersetzungsreaktionEine Zersetzungsreaktion ist eine thermisch induzierte Reaktion einer chemischen Substanz, die fest und/oder gasförmige Zersetzungsprodukte bildet.Zersetzungsreaktion unter quasi-isothermen Bedingungen, sondern auch der maximale Temperaturanstieg und der maximale Druckanstieg unter weitgehend adiabatischen Bedingungen bestimmt werden.
Der PHI-Faktor (φ) oder „Thermal Inertia“
Aus den beiden gemessenen Signalen, der Temperatur und dem Druck, lassen sich die maximalen Geschwindigkeiten für die Erhöhung von Temperatur und Druck berechnen. Zusätzlich sind Vorhersagen über die Temperatur möglich, bei der mindestens 24 Stunden verstreichen, bis die maximale Reaktionsgeschwindigkeit erreicht wird (time to maximum rate, TMR24h).
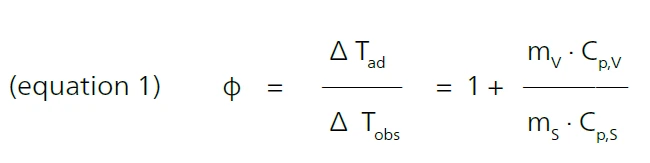
Ein wesentlicher Parameter für das Testszenario ist der so genannte PHI-Faktor (φ). Er gibt das Verhältnis von Masse und spezifischer Wärme der Probe im Vergleich zum Probenbehälter an, wobei ΔTad der Temperaturanstieg unter adiabatischen Bedingungen, ΔTobs der beobachtete Temperaturanstieg unter gegebenen Bedingungen, m die Masse, Spezifische Wärmekapazität (cp)Die spezifische Wärmekapazität oder Wärmekapazität ist eine messbare physikalische Größe, die dem Verhältnis der einem Objekt zugeführten Wärme zur resultierenden Temperaturänderung entspricht.cp die Spezifische Wärmekapazität (cp)Die spezifische Wärmekapazität oder Wärmekapazität ist eine messbare physikalische Größe, die dem Verhältnis der einem Objekt zugeführten Wärme zur resultierenden Temperaturänderung entspricht.spezifische Wärmekapazität, s die Probe und v der Behälter sind [1].
Der φ-Faktor, auch als Thermische TrägheitDie thermische Trägheit entspricht dem PHI-Faktor. Beide beschreiben das Verhältnis von Masse und spezifischer Wärmekapazität einer Probe oder Probenmischung im Vergleich zu der des Probenbehälters. Je näher der PHI-Faktor bei 1 liegt, desto geringer ist der Einfluss des Probenbehälters und umso repräsentativer ist das Ergebnis für die Probe selbst.thermische Trägheit bekannt, kommt dem ideal adiabatischen Zustand näher, je mehr er sich an 1 annähert. Das wiederum bedeutet, dass die Messergebnisse im Idealfall durch die Probe und nicht durch den Einfluss des Probenbehälters bestimmt werden. Andererseits gibt es Limitierungen hinsichtlich der verfügbaren Probenmenge und des maximal möglichen Behältervolumens. Um aufzuzeigen, wie diese Parameter den φ-Faktor beeinflussen, zeigt Tabelle 1 eine Zusammenfassung der φ-Faktoren, die für die beiden Proben (organische Peroxide und Wasserstoffperoxid), für die zwei Behältermaterialien (Edelstahl und Titan®) und für eine realistische Auswahl an Probenmassen berechnet wurden.
Tabelle 1: Für unterschiedliche Messbedingungen berechnete Ф-Faktoren
| Masse Wasserstoffperoxid / g | 0,25 | 0,50 | 1,0 | 2,0 | 5,0 | 8,0 |
| Ф für 10,0 g-Titanbehälter | 7,41 | 4,20 | 2,60 | 1,80 | 1,32 | 1,20 |
| Masse organisches Peroxid / g | 0,25 | 0,50 | 1,0 | 1,5 | 5,0 | 8,0 |
| Ф für 7,0 g-Edelstahlbehälter | 9,86 | 5,43 | 3,21 | 1,5 | - | - |
| Masse Wasserstoffperoxid / g | 0,25 | 0,50 | 1,0 | 2,0 | 5,0 | 8,0 |
| Ф für 7,0 g-Edelstahlbehälter | 5,92 | 3,46 | 2,23 | 1,82 | - | - |
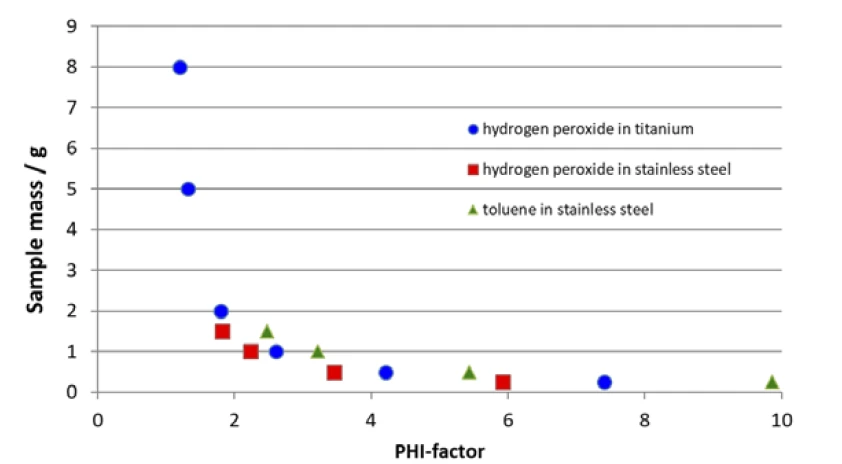
Der bereits erwähnte Zusammenhang von Probenmasse und berechnetem φ-Faktor ist zusätzlich in Abbildung 1 dargestellt. Da die Spezifische Wärmekapazität (cp)Die spezifische Wärmekapazität oder Wärmekapazität ist eine messbare physikalische Größe, die dem Verhältnis der einem Objekt zugeführten Wärme zur resultierenden Temperaturänderung entspricht.spezifische Wärmekapazität der zu untersuchenden Probe ebenso wie die spezifische Wärmekapazität des Behältermaterials gegeben sind, ist der einzige zur Verfügung stehende Parameter für die Änderung des φ-Faktors die Probenmasse.
Einerseits würde eine Erhöhung der Probenmasse den φ-Faktor dem Wert 1 annähern, andererseits ist jedoch das maximale Behältervolumen limitiert und die maximalen Bereiche für die Messgrößen vorgegeben. Es ist zwingend erforderlich, den Druckbereich, den Temperaturbereich sowie die maximale Trackingrate des verwendeten Kalorimeters vom Typ ARC® zu berücksichtigen, um keinen der vorgenannten Werte zu überschreiten, da sonst die erhaltenen Daten nicht aussagekräftig sind. Aus Abbildung 1 ist ersichtlich, dass der Edelstahl-Behälter (Abbildung 3) aufgrund seines Gesamtvolumens von 2,6 ml auf eine Probenmasse von weniger als 2,0 g beschränkt ist. Da die Probenbehälter in der Regel nicht mehr als bis zur Hälfte befüllt werden, liegt der erwartete φ-Faktor zwischen 2 und 4, je nach spezifischer Wärmekapazität der Probe. Lediglich mit 1,5 mg Wasserstoffperoxid, das eine relativ hohe spezifische Wärmekapazität aufweist, kann ein φ-Faktor besser als 2 erreicht werden. Selbst bei Verwendung eines Titanbehälters mit einem Volumen von 8,6 ml sind Probenmassen von über 3,0 g und φ-Faktoren im Bereich von 1,5 nur schwer zu realisieren.
Alle Proben mit thermischem Gefährdungspotenzial weisen auch ein erhöhtes Risiko hinsichtlich der Handhabung in einer Laborumgebung auf. Aus Sicherheitsgründen ist es natürlich vorteilhafter, risikoreiche Proben in geringen Mengen zu verwenden. Unter Berücksichtigung der vorgenannten Einschränkungen wird ein Dilemma deutlich. Je geringer der φ-Faktor, desto aussagekräftiger sollten die Ergebnisse sein. Dies würde jedoch größere Probenmengen voraussetzen. Verringert man aus Sicherheitsgründen die Probenmasse, erhöht sich wiederum der φ-Faktor. Eine Lösung für diese Problematik stellt der patentierte VariPhi-Heizer dar.
Das Multi-Modul-Kalorimeter (MMC 274 Nexus®)
Das Multi-Modul Kalorimetrie (MMC)Das Multi-Modul-Kalorimeter (MMC) besteht aus einer Basiseinheit und austauschbaren Modulen. Ein Modul ist für Accelerating Rate Calorimetry (ARC) vorbereitet, ein zweites wird für Scanning-Tests (Scanning Modul) herangezogen und ein drittes ist auf die Batterieprüfung von Knopfzellen (Knopfzellen-Modul) ausgelegt.MMC 274 Nexus® Multi-Modul-Kalorimeter (Abbildung 4) bietet drei unterschiedliche Messmodule [2]. Das Knopfzellen-ModulDas Kalorimetermodul eines Mult-Modul-Kalorimeters (MMC), das Scanning- und isotherme Tests kompletter Knopfzellen unterschiedlicher Größe erlaubt. Das DSC-ähnliche Zwillingsdesign liefert die Wärmetönung während eines Aufheizprogramms der beim Laden und Entladen von Akkus.Knopfzellen-Modul ist auf die Untersuchung von Batterien spezialisiert und das Scanning-Modul [3, 4] kann für die Auswertung kalorischer Daten aus einer Aufheizung mit konstanter Aufheizrate oder konstanter Leistung eingesetzt werden. Das ARC®-Modul (Abbildung 5) wird zur Untersuchung thermisch induzierter Zersetzungsreaktionen eingesetzt und wurde für die in dieser Arbeit vorgestellten Ergebnisse verwendet.
Testsubstanz: Wasserstoffperoxidlösung
Wasserstoffperoxid (H2O2) zerfällt thermisch in Wasser und Sauerstoff. Diese Zersetzungsreaktion lässt sich thermisch initiieren und ist stark ExothermEin Phasenübergang oder eine Reaktion ist exotherm, wenn von der Probe Wärme freigesetzt wirdexotherm. Deshalb wird Wasserstoffperoxid in der Regel als wässrige Lösung von bis zu maximal 35 % verwendet. Für thermische Sicherheitsstudien ist es eine ideale Substanz, da sie während der Zersetzung lediglich Wasser und Sauerstoff bildet, was die leichte Reinigung und Wiederverwendung der Probenbehälter ermöglicht.
Das ARC®-Modul mit VariPhi
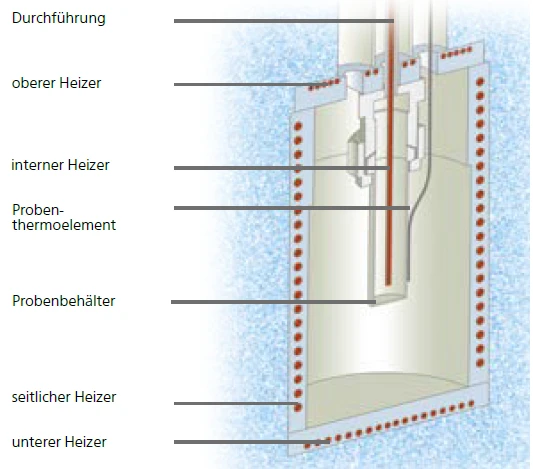
Abbildung 5 zeigt den Aufbau des ARC®-Moduls des MMC. Der Probenbehälter wird innerhalb des Kalorimeterraums platziert und die Probentemperatur wird über ein Thermoelement detektiert, welches direkt an der Außenwand des Probenbehälters befestigt ist. Der Behälter selbst ist über eine Durchführung mit einem Manometer verbunden. Genau in der Mitte dieses Aufbaus wird der interne Heizer, genannt VariPhi, innerhalb der Probe platziert.
Dieser patentierte VariPhi-Heizer ist die Lösung für das vorher beschriebene Dilemma. Einerseits kann er für das Screening eingesetzt werden, um zu ermitteln, ob eine unbekannte Probe ein Gefährdungspotential aufweist. In diesem Fall würde dem VariPhi-Heizer eine konstante Leistung zugeführt. Zusammen mit der resultierenden Heizrate kann ein Wärmeflusssignal zur Unterscheidung von endothermen und exothermen Probeneffekten berechnet werden. Andererseits kann der VariPhi-Heizer auch für die teilweise oder vollständige Kompensation des Einflusses des Probenbehälters (φ-Faktor; Gl. 1) verwendet werden. In diesem Fall führt der VariPhi-Heizer der Probe genau die Wärmemenge zu, die normalerweise für das Aufheizen des Probenbehälters benötigt würde. Da während einer Zersetzungsreaktion die Probe der wärmste Teil des Gesamtsystems ist, wird der Behälter von der Probe erwärmt, bevor die Reaktionswärme durch das außen am Behälter angebrachte Thermoelement (Abbildung 5) erfasst wird. Gemäß Gleichung 1 kann der φ-Faktor teilweise oder vollständig kompensiert werden. Auf diese Weise ist es möglich, den φ-Faktor auf einen Wert einzustellen, der die realen Bedingungen eines Reaktors widerspiegelt, oder er kann zur Untersuchung von Worst-Case-SzenarienIm Zusammenhang mit einem chemischen Reaktor ist ein Worst-Case-Szenario die Situation, in der die durch die Reaktion verursachte Temperatur und/oder Druckerzeugung außer Kontrolle gerät.Worst-Case-Szenarien auf φ = 1 angepasst werden. Die erforderliche Leistungsaufnahme zur Kompensation ergibt sich aus Masse und spezifischer Wärmekapazität des Behälters.
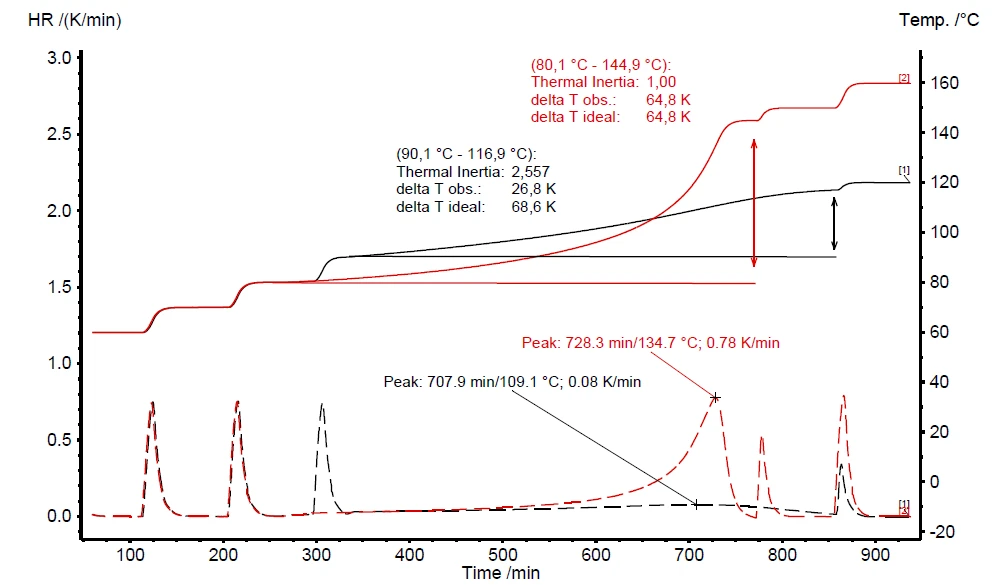
Wurde beim Screening-Test ein thermisches Gefährdungspontial mittels Eigenerwärmung und Druckaufbau festgestellt (Abbildung 6), ist es zwingend erforderlich, weitergehende Untersuchungen zum „Thermal Runaway“ durchzuführen. Die Ergebnisse für einen solchen Heat-Wait-Search (HWS)HWS ist die Bezeichnung für eine Sequenz, die die Probe auf eine bestimmte Temperatur aufheizt (Heat), eine thermische Stabilisierung des Systems ermöglicht (Wait) und schließlich erkennt (Search), ob ein Anstieg der Probentemperatur festgestellt wird, der durch eine exotherme Zersetzungsreaktion der Probe verursacht wird.Heat-Wait-Search (Heat-Wait-Search (HWS)HWS ist die Bezeichnung für eine Sequenz, die die Probe auf eine bestimmte Temperatur aufheizt (Heat), eine thermische Stabilisierung des Systems ermöglicht (Wait) und schließlich erkennt (Search), ob ein Anstieg der Probentemperatur festgestellt wird, der durch eine exotherme Zersetzungsreaktion der Probe verursacht wird.HWS)-Test sind in Abbildung 7 dargestellt. Darin werden die Unterschiede zwischen den kompensierten (rote Kurve) und den nicht kompensierten Messergebnissen (schwarze Kurve) verglichen. Die dazugehörigen Messbedingungen sind in Tabelle 2 zusammengefasst.
Im Gegensatz zum Scanning-Test detektiert der entsprechende Heat-Wait-Search (HWS)HWS ist die Bezeichnung für eine Sequenz, die die Probe auf eine bestimmte Temperatur aufheizt (Heat), eine thermische Stabilisierung des Systems ermöglicht (Wait) und schließlich erkennt (Search), ob ein Anstieg der Probentemperatur festgestellt wird, der durch eine exotherme Zersetzungsreaktion der Probe verursacht wird.Heat-Wait-Search-Test an Wasserstoffperoxid die Eigenerwärmung bereits bei 90 °C (Abbildung 7, schwarze Kurve). Die maximale Eigenerwärmungsrate wurde mit 0,08 K/min zusammen mit einem Temperaturanstieg von 26,8 K (ΔTobs) ermittelt. Der beobachtete Temperaturanstieg wird durch Subtraktion der Onsettemperatur (Tstart, Beginn des exothermen Vorgangs) von der Endtemperatur des exothermen Vorgangs (Tfinal) ausgewertet [1].

Die oben diskutierten Messergebnisse wurden ohne Verwendung von VariPhi durchgeführt; der zugehörige φ-Faktor ist 3,14. Beim Einsatz von VariPhi für den gleichen Probenaufbau mit der Fähigkeit, Masse und spezifische Wärmekapazität des Behälters zu kompensieren (φ = 1), wurde der gemessene Temperaturanstieg mit 64,8 K bestimmt (rote Kurve, Abbildung 7). Wie erwartet ist in diesem Fall der Temperaturanstieg (ΔTobs) deutlich größer. Je niedriger der φ-Faktor, desto weniger Wärme geht an den Probenbehälter verloren; desweiteren verbleibt die gesamte Reaktionswärme im Probenbehälter und beschleunigt so die Zersetzungsreaktion. Die gestrichelte Linie in Abbildung 7 bestätigt eine nahezu zehnmal höhere Eigenerwärmungsrate für die Messung mit VariPhi (rote Kurve, Abbildung 7) im Vergleich zur nicht kompensierten Messung. Diese Ergebnisse belegen den großen Einfluss des φ-Faktors im Hinblick auf das zu erwartende Gefahrenpotential chemischer Reaktionen.
Steht VariPhi nicht zur Verfügung, können die Messungen aufgrund von Einschränkungen durch die Materialeigenschaften des Probenbehälters, der maximalen Probenmenge, dem erwarteten Druck usw. nicht unter niedrigen φ-Bedingungen durchgeführt werden. In diesem Fall schlägt die ASTM E1981 – 81(2012) für ideale Messbedingungen folgende Annäherung vor:

Der Wert “ΔTideal” entspricht dem ΔTad und wird bei der Datenauswertung in der NETZSCH-Proteus®- Software gemäß Gleichung 3 berechnet. Das nicht kompensierte Ergebnis (schwarze Kurve in Abbildung 7) zeigt für “ΔTobs” 26,8 K und einen φ-Faktor von 2,557. Die Annahme eines Messergebnisses unter idealen Bedingungen (φ = 1) ergibt für “ΔTideal” 68,6 K. Diese Annahme gemäß Gleichung 3 liegt nahe am Messergebnis von 64.8 K, das mittels VariPhi-Heizer (rote Kurve in Abbildung 7) erhalten wurde.
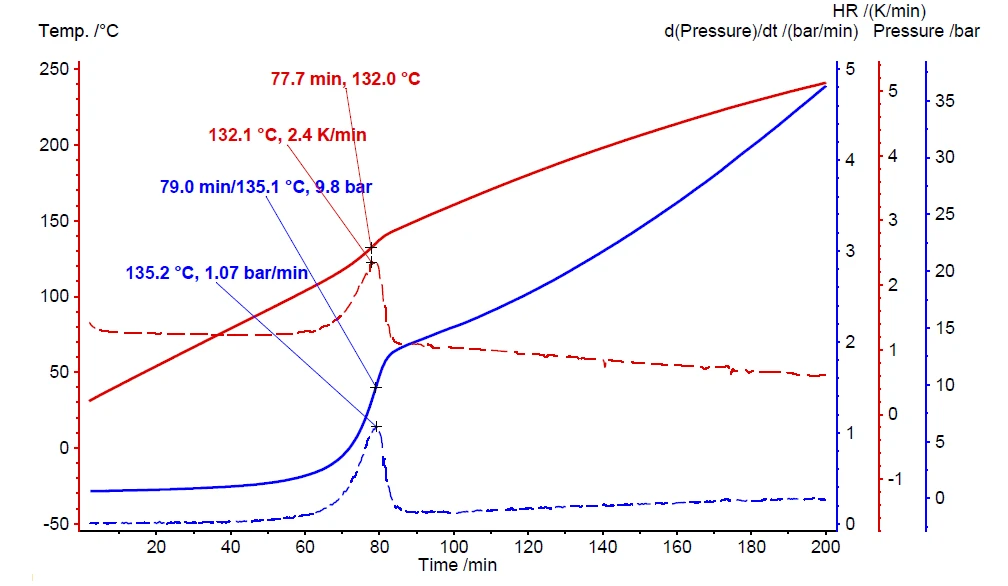
Tabelle 2: Messbedingungen für Scanning- (Abbildung 6) und Heat-Wait-Seach-Tests (Abbildung 7)
MMC 274 Nexus® | |||
|---|---|---|---|
| MMC-Modul | Scanning | ARC® | |
ARC® ohne Kompensation | ARC® mit Kompensation | ||
| Behältermaterial | Edelstahl | Edelstahl | Edelstahl |
| Behältertyp | geschlossen | geschlossen | geschlossen |
| Behältermasse | 717,00 mg | 7119,74 mg | 7119,66 mg |
| Aufheizung | konstante Leistung (250 mW) | HWS | |
| Atmosphäre | Luft | Luft | Luft |
| Spülgasrate | Statisch | Statisch | Statisch |
| Temperaturbereich | RT ... 250°C | RT ... 250°C | RT ... 250°C |
| Probenmasse | 512,35 mg | 749,79 mg | 749,46 mg |
| Ф-Faktor | 4,15 | 3,14 | 3,14 |
| Ф-Faktor (komp.) | 3,14 | 1,00 | |
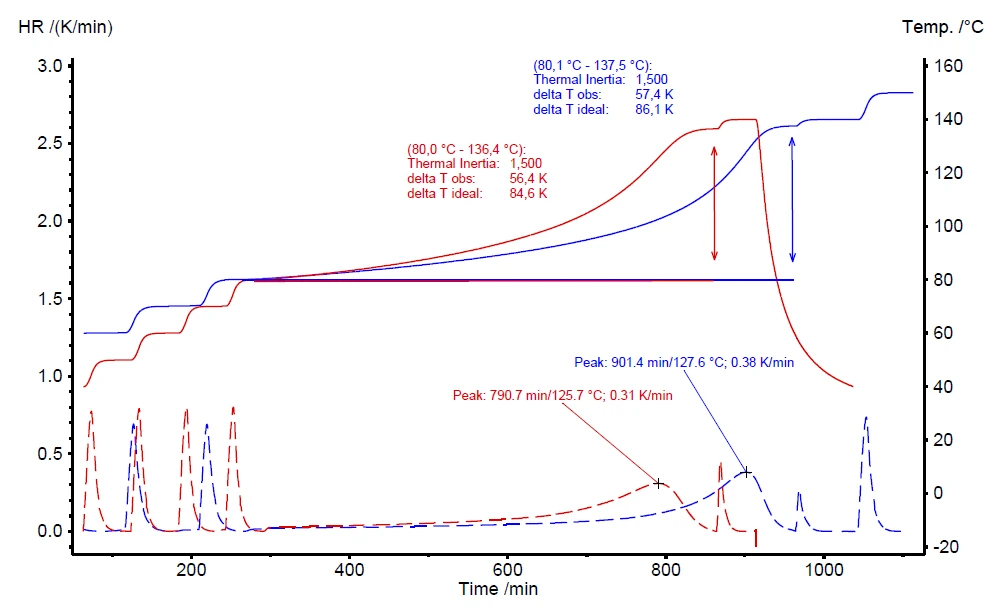
Ein weiterer Vorteil des VariPhi-Heizers ist die Kompensation des φ-Faktors zur besseren Vergleichbarkeit unterschiedlicher Messbedingungen. In Abbildung 8 sind zwei Messungen mit unterschiedlichen Mengen Wasserstoffperoxid verglichen. Die rote Kurve zeigt eine Messung mit 0,500 g H2O2 (φ = 4,21) und das blau dargestellte Messergebnis wurde mit 1,00 g (φ = 2,60) durchgeführt. Aufgrund der unterschiedlichen Probeneinwaagen unterscheiden sich die φ-Faktoren deutlich: 4,21 bzw. 2,60. Der VariPhi-Heizer wurde zur Kompensation des φ-Faktors auf φ = 1,5 bei beiden Messungen eingesetzt. Die ausgewerteten Ergebnisse für die beiden Messungen sind sehr ähnlich, einschließlich der Onsettemperatur (Tstart), der Eigenerwärmungsrate (HR) und des beobachteten Temperaturanstiegs (ΔTobs).
Zusammenfassung
Das Testszenario zur Untersuchung der Zersetzungsreaktion von Wasserstoffperoxid (H2O2) zeigt deutlich die Vorteile der Verwendung des zusätzlichen Heizers in Geräten der Accelerating Rate Calorimetry (ARC®). Der patentierte VariPhi-Heizer kann eingesetzt werden, um den Testaufbau entweder auf einen realen φ-Faktor oder auf den Idealwert von φ = 1 zu kompensieren. Diese Kompensation des Wärmeverlustes erlaubt Messungen mit niedrigen φ-Faktoren, selbst mit kleinen Probenmengen. Die Möglichkeit, den φ-Faktor zu variieren, ist besonders für Labore von Vorteil, die im Bereich thermische Sicherheit das Gefahrenpotential von Chemikalien und Reaktionsgemischen untersuchen.


