Происхождение и применение
Слюдяной сланец добывают еще с доисторических времен. До появления промышленного производства стекла слюда использовалась для изготовления оконных стекол, поскольку ее слоистая структура позволяет легко разбивать ее на тонкие листы. В настоящее время слюда используется в качестве пигмента в красках и косметике. Благодаря хорошей теплопроводности и электроизоляционным свойствам, еще одной важной областью применения слюды является электронная промышленность, где она используется в качестве изолирующих дисков для полупроводниковых компонентов или диэлектрика для конденсаторов с очень низкими потерями [1].
Структура
Слюда - это общий термин для группы минералов, относящихся к листовым силикатам. Их общий химический состав - DG2.3 [T4O10]X2. Один слой образован угловыми соединенными тетраэдрами SiO2 (для T = Si); другой слой состоит из октаэдров GO6. Каждый октаэдрический слой вложен между двумя тетраэдрическими слоями. Эта последовательность слоев T-O-T (тетраэдрический-октаэдрический-тетраэдрический), однако, не является нейтральной по заряду. Выравнивание заряда достигается за счет мостиковых межслоевых анионов (X) [2].

Условия измерения
- Инструмент
- TG 209 F1 Libra®
- Образец
- Слюда
- Масса образца
- 5.106 мг
- Тигель
- Al2O3
- Атмосфера
- Азот
- Скорость потока газа
- 40 мл/мин
- Скорость нагрева
- 10 К/мин
Термогравиметрия
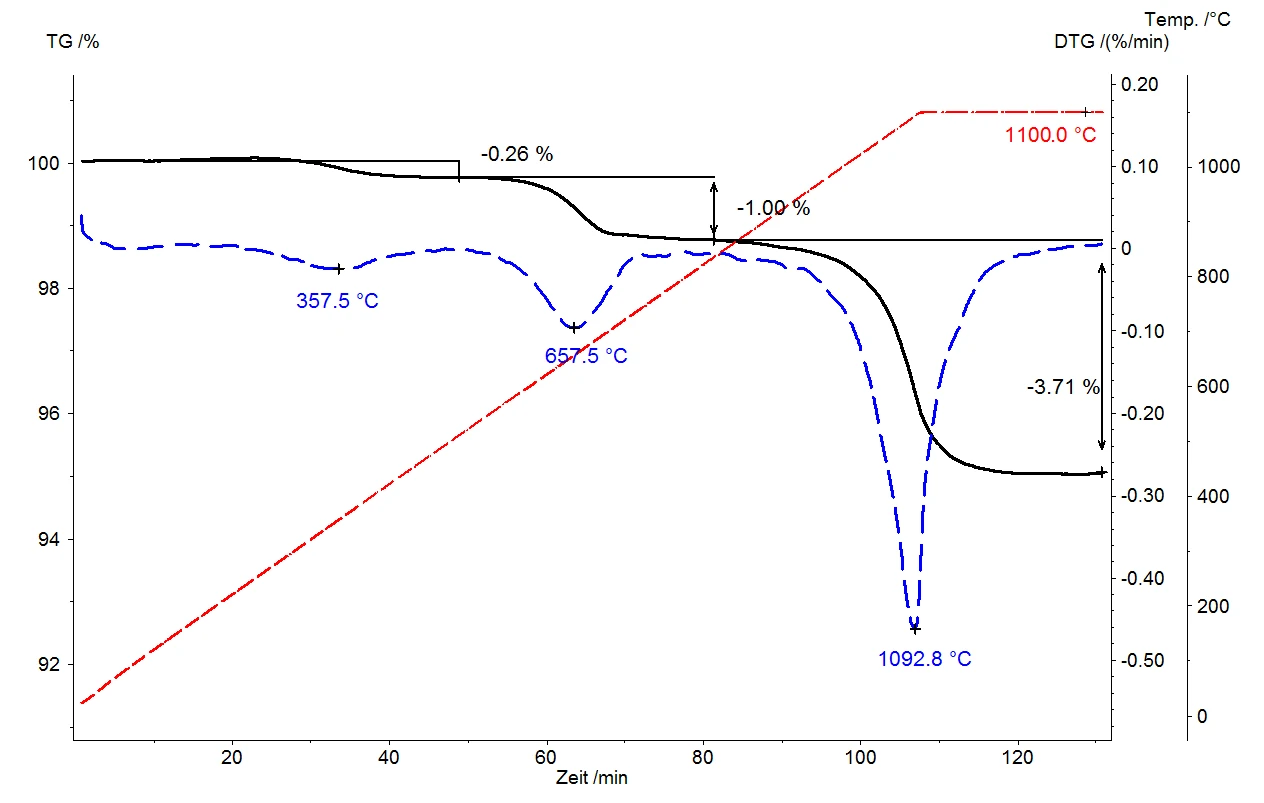
Термобаллон может обеспечить отличную характеристику теплового поведения неорганических веществ. Он непрерывно регистрирует любые изменения в составе образца, а использование динамической скорости нагрева (10 К/мин в нашем примере) позволяет оценивать происходящее с образцом в зависимости от температуры. Поскольку скорость нагрева является мерой энергии, подводимой к образцу, она позволяет сделать выводы о необходимой энергии высвобождения и/или энергии связывания высвобождающихся веществ.
Представленный здесь пример с образцом слюды демонстрирует три хорошо разделенных этапа потери массы: один при 357°C, другой при 657°C и третий при 1092°C. Хорошее разделение этих ступеней потери массы позволяет легко количественно определить количество газа, выделившегося из образцов, путем оценки ступеней при различных температурах. Относительные изменения массы составляют 0,26 %, 1,00 % и 3,71 %. Температура выделения является показателем прочности адсорбции или связи: чем выше ее значение, тем сильнее адсорбция газа на поверхности кристалла или связь с кристаллической структурой до выделения. В отличие от "молниеносного пиролиза", при котором образец нагревается до максимальной температуры за несколько секунд и все газы выделяются очень резко, в термогравиметрии очень переменная скорость нагрева и сочетание динамического и изотермического сегментов позволяют выделять газообразные продукты разложения в зависимости от температуры и, следовательно, ступенчато. Наш пример со слюдой дополнительно показывает, что нагрев образца до 1100°C со скоростью 10 К/мин был недостаточен для завершения полной реакции разложения и, следовательно, недостаточен для ее количественного определения.
Фактически, для полного завершения реакции потребовалась последующая изотермическая фаза продолжительностью 30 минут. Такая гибкость в регулировании температуры не только облегчает количественное определение, но и позволяет идентифицировать газы, выделяющиеся из образца в процессе термогравиметрии. Для этого хорошо подходит техника, называемая "сопряжением", когда термоаналитические измерительные приборы соединяются с приборами для спектроскопических методов, таких как масс-спектрометрия или ИК-Фурье спектроскопия.