Origine e applicazione
Lo scisto di mica è stato estratto fin dalla preistoria. Prima della produzione industriale del vetro, la mica veniva utilizzata per i vetri delle finestre, poiché la sua struttura stratificata permette di romperla facilmente in fogli sottili. Oggi la mica è utilizzata come pigmento nelle vernici e nei cosmetici. Grazie alle sue buone proprietà di conduzione termica e isolamento elettrico, un altro importante campo di applicazione della mica è l'industria elettronica, dove viene utilizzata come disco isolante per i componenti dei semiconduttori o come dielettrico per condensatori a bassissima perdita [1].
Struttura
Mica è il termine generico per un gruppo di minerali appartenenti ai silicati di foglio. La loro composizione chimica generale è DG2.3 [T4O10]X2. Uno strato è formato da tetraedri SiO2 collegati ad angolo (per T = Si); un altro strato è costituito da ottaedri GO6. Ogni strato di ottaedri è incastrato tra due strati di tetraedri. Questa sequenza di strati T-O-T (tetraedrico-ottaedrico-tetraedrico), tuttavia, non è neutra in termini di carica. L'equazione di carica è ottenuta per mezzo di anioni ponte interstrato (X) [2].

Condizioni di misura
- Strumento
- TG 209 F1 Libra®
- Campione
- Mica
- Massa del campione
- 5.106 mg
- Crogiolo
- Al2O3
- Atmosfera
- Azoto
- Portata del gas
- 40 ml/min
- Velocità di riscaldamento
- 10 K/min
Termogravimetria
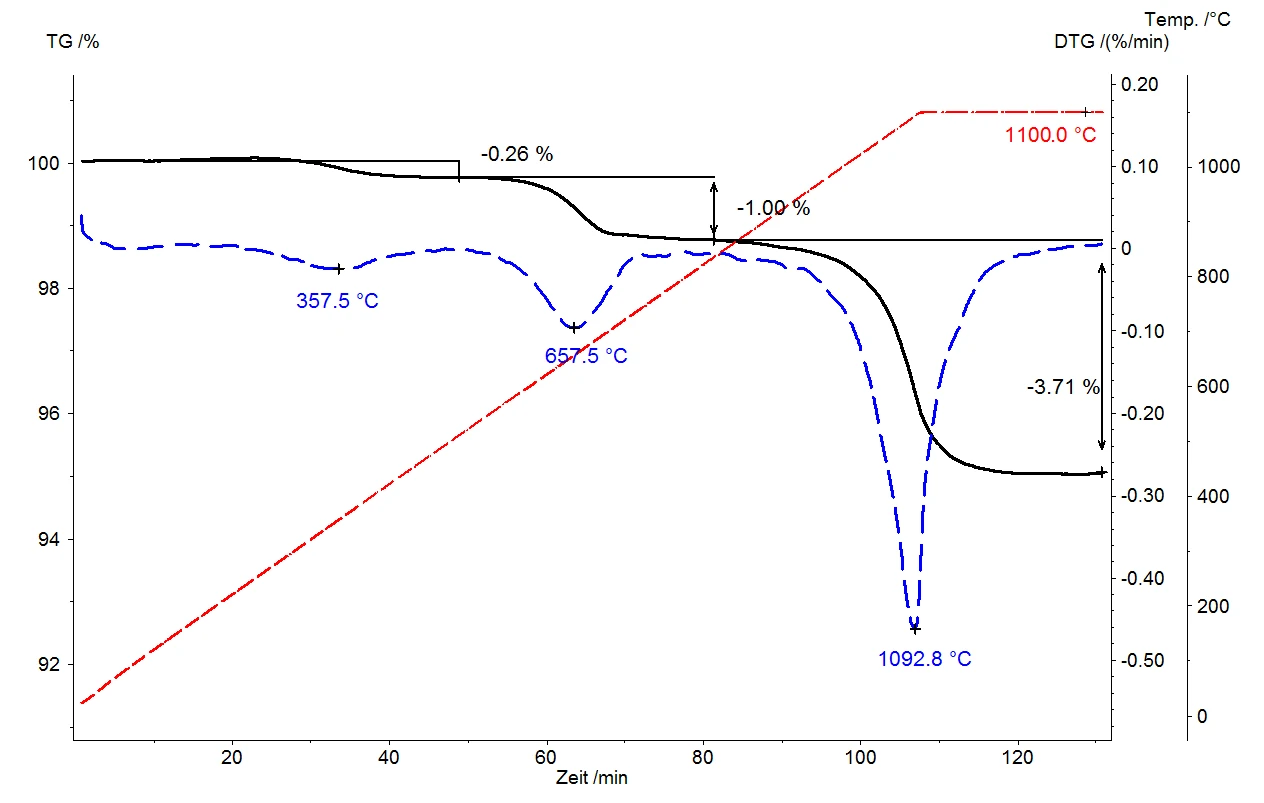
Una termobilancia può fornire un'eccellente caratterizzazione del comportamento termico delle sostanze inorganiche. La termobilancia registra continuamente qualsiasi cambiamento nella composizione del campione, mentre l'uso di una velocità di riscaldamento dinamica (10 K/min nel nostro esempio) consente di valutare le occorrenze del campione in funzione della temperatura. Poiché la velocità di riscaldamento è una misura dell'energia fornita al campione, consente di trarre conclusioni sull'energia di rilascio richiesta e/o sull'energia di legame delle sostanze rilasciate.
L'esempio presentato qui con un campione di mica mostra tre fasi di perdita di massa ben separate: una a 357°C, un'altra a 657°C e la terza a 1092°C. La buona separazione di questi passaggi di perdita di massa consente di quantificare facilmente le quantità di gas evolute dai campioni attraverso la valutazione dei passaggi alle varie temperature. Le variazioni di massa relative ammontano a 0,26%, 1,00% e 3,71%. La temperatura di rilascio è un indicatore della forza dell'adsorbimento o del legame: più alto è il suo valore, più forte è l'adsorbimento del gas sulla superficie del cristallo o il legame con la struttura del cristallo prima del rilascio. A differenza della "PirolisiLa pirolisi è la decomposizione termica di composti organici in atmosfera inerte.pirolisi flash" - in cui il campione viene riscaldato alla massima temperatura in pochi secondi e tutti i gas vengono quindi rilasciati molto bruscamente - la velocità di riscaldamento molto variabile della termogravimetria e la combinazione di segmenti dinamici e isotermici consentono di rilasciare i prodotti di Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. decomposizione gassosa in funzione della temperatura e quindi in modo graduale. Il nostro esempio con la mica mostra inoltre che un trattamento di riscaldamento del campione a 1100°C a 10 K/min non è stato sufficiente a consentire la conclusione della Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. reazione di decomposizione completa, e quindi non è stato sufficiente nemmeno per la sua quantificazione.
Infatti, una successiva fase isotermica di 30 minuti è stata necessaria per completare completamente la reazione. Una tale flessibilità nel controllo della temperatura non solo facilita la quantificazione, ma consente anche di identificare i gas emessi dal campione durante il processo termogravimetrico. A questo scopo, la tecnica chiamata "accoppiamento", in cui gli strumenti di misura termoanalitici sono accoppiati a strumenti per metodi spettroscopici come la spettrometria di massa o la spettroscopia FT-IR.