Köken ve Uygulama
Mika şist tarih öncesi çağlardan beri çıkarılmaktadır. Mika aslında camın endüstriyel üretiminden önce pencere camlarında kullanılıyordu, çünkü katmanlı yapısı kolayca ince tabakalara kırılmasına izin veriyordu. Günümüzde mika, boya ve kozmetik ürünlerinde pigment olarak kullanılmaktadır. İyi ısı iletimi ve elektrik yalıtımı özellikleri nedeniyle, mika için bir diğer önemli uygulama alanı, yarı iletken bileşenler için yalıtım diskleri veya çok düşük kayıplı kapasitörler için bir dielektrik olarak kullanıldığı elektronik endüstrisidir [1].
Yapı
Mika, tabaka silikatlara ait bir grup mineral için kullanılan genel bir terimdir. Genel kimyasal bileşimleri DG2.3 [T4O10]X2'dir. Bir katman köşe bağlantılı SiO2 tetrahedronlardan oluşur (T = Si için); diğer katman GO6 oktahedronlardan oluşur. Her oktahedron katmanı iki tetrahedron katmanı arasına gömülüdür. Ancak bu T-O-T (tetrahedral-oktahedral-tetrahedral) katman dizisi yük bakımından nötr değildir. Yük eşitliği, katmanlar arası anyonların (X) köprülenmesi yoluyla sağlanır [2].

Ölçüm Koşulları
- Enstrüman
- TG 209 F1 Libra®
- Örnek
- Mika
- Örnek kütle
- 5.106 mg
- Pota
- Al2O3
- Atmosfer
- Azot
- Gaz akış hızı
- 40 ml/dak
- Isıtma oranı
- 10 K/dak
Termogravimetri
Bir termobalans, inorganik maddelerin termal davranışının mükemmel bir şekilde karakterize edilmesini sağlayabilir. Numune bileşimindeki herhangi bir değişikliği sürekli olarak kaydederken, dinamik bir ısıtma hızının (örneğimizde 10 K/dak) kullanılması, numune oluşumlarının sıcaklığın bir fonksiyonu olarak değerlendirilmesine olanak tanır. Isıtma hızı numuneye verilen enerjinin bir ölçüsü olduğundan, gerekli salım enerjisi ve/veya salınan maddelerin bağlanma enerjisi ile ilgili sonuçlara varılmasını sağlar.
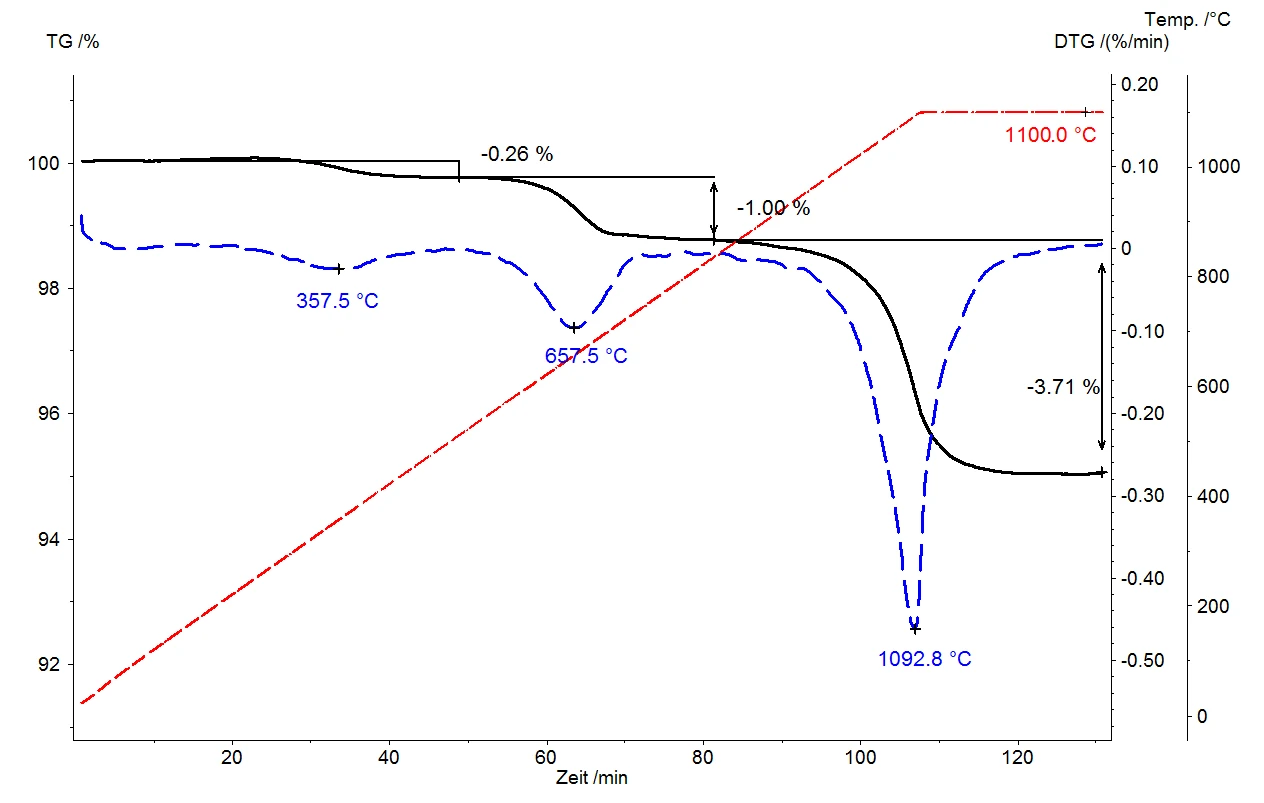
Burada bir mika örneği ile sunulan örnekte, biri 357°C'de, diğeri 657°C'de ve üçüncüsü 1092°C'de olmak üzere üç iyi ayrılmış kütle kaybı adımı görülmektedir. Bu kütle kaybı adımlarının iyi bir şekilde ayrılması, çeşitli sıcaklıklarda adım değerlendirmesi yoluyla örneklerden çıkan gaz miktarlarının kolayca ölçülmesini sağlar. Bağıl kütle değişimleri %0,26, %1,00 ve %3,71'dir. Serbest bırakma sıcaklığı, adsorpsiyonun veya bağın gücünün bir göstergesidir: değeri ne kadar yüksekse, gazın kristal yüzeyine adsorpsiyonu veya serbest bırakılmadan önce kristal yapıya olan bağı o kadar güçlüdür. Numunenin birkaç saniye içinde maksimum sıcaklığa ısıtıldığı ve böylece tüm gazların aniden açığa çıktığı "ani pirolizin" aksine, termogravimetrinin çok değişken ısıtma hızları ve dinamik ve İzotermalKontrollü ve sabit sıcaklıkta yapılan testlere izotermal denir.izotermal segmentlerin kombinasyonu, gazlı bozunma ürünlerinin sıcaklığın bir fonksiyonu olarak ve dolayısıyla kademeli bir şekilde açığa çıkmasını sağlar. Mika örneğimiz ayrıca numunenin 10 K/dk'da 1100°C'ye kadar ısıtılmasının tam Ayrışma reaksiyonuBir ayrışma reaksiyonu, katı ve/veya gaz ürünler oluşturan kimyasal bir bileşiğin termal olarak indüklenen reaksiyonudur. ayrışma reaksiyonunun sonuçlanması için yeterli olmadığını ve dolayısıyla miktar tayini için de yeterli olmadığını göstermektedir.
Aslında, reaksiyonu tamamen tamamlamak için 30 dakikalık bir İzotermalKontrollü ve sabit sıcaklıkta yapılan testlere izotermal denir.izotermal faz gerekliydi. Sıcaklık kontrolündeki bu esneklik sadece miktar tayinini kolaylaştırmakla kalmaz, aynı zamanda termogravimetrik işlem sırasında numuneden çıkan gazların tanımlanmasına da olanak sağlar. Termoanalitik ölçüm cihazlarının kütle spektrometrisi veya FT-IR spektroskopisi gibi spektroskopik yöntemler için kullanılan cihazlara bağlandığı "kuplaj" adı verilen bir teknik bunun için çok uygundur.