Giriş
Eczacılıkta, hakkında asetilsalisilik asitten (ya da kısaca ASA; İngilizce konuşulan ülkelerde Aspirin™ markası bile sıklıkla eşanlamlı olarak kullanılmaktadır) daha fazla şey yazılan bir etken madde neredeyse yoktur. Başarı öyküsü 19. yüzyılın sonunda Dr. Felix Hoffmann'ın bu maddeyi BAYER laboratuvarlarında ilk kez safsızlık içermeyen bir şekilde sentezlemesiyle başlamıştır. Günümüzde hala geniş bir terapötik aralıkta kullanılan en popüler farmasötiklerden biridir. Steroid olmayan anti-enflamatuar ilaçlar (NSAID'ler) grubuna aittir ve ağrı, ateş ve enflamasyon tedavisinde endikedir. Ayrıca, yüksek riskli hastalarda kalp krizi veya inmenin tekrarlamasını önlemek için kullanılır. ASA, 1977 yılında DSÖ'nün (Dünya Sağlık Örgütü) "temel ilaç listesine" analjezik olarak eklenmiştir [1].
Bu, asetilsalisilik asidin termal davranışını daha ayrıntılı olarak inceleyen dört uygulama notundan ikincisidir: Farklı gaz atmosferlerinde Ayrışma reaksiyonuBir ayrışma reaksiyonu, katı ve/veya gaz ürünler oluşturan kimyasal bir bileşiğin termal olarak indüklenen reaksiyonudur. ayrışma, Ayrışma reaksiyonuBir ayrışma reaksiyonu, katı ve/veya gaz ürünler oluşturan kimyasal bir bileşiğin termal olarak indüklenen reaksiyonudur. ayrışma kinetiği ve ortaya çıkan gaz türleri [2] [3] [4].
Termoanalitik Verilerin Kinetik Analizi
Termoanalitik yöntemlerin ölçüm verileriyle, Ayrışma reaksiyonuBir ayrışma reaksiyonu, katı ve/veya gaz ürünler oluşturan kimyasal bir bileşiğin termal olarak indüklenen reaksiyonudur. ayrışma, PirolizPiroliz, organik bileşiklerin inert bir atmosferde termal olarak ayrışmasıdır.piroliz veya yanma nedeniyle kütle kaybı, Erime Sıcaklıkları ve EntalpileriGizli ısı olarak da bilinen bir maddenin füzyon entalpisi, bir maddeyi katı halden sıvı hale dönüştürmek için gerekli olan enerji girdisinin, tipik olarak ısının bir ölçüsüdür. Bir maddenin erime noktası, katı (kristal) halden sıvı (izotropik eriyik) hale geçtiği sıcaklıktır. erime veya KristalleşmeKristalleşme, kristallerin oluşumu ve büyümesi sırasında sertleşmenin fiziksel sürecidir. Bu işlem sırasında kristalleşme ısısı açığa çıkar.kristalleşme gibi enerjik değişiklikler hakkında veya ayrıca örneğin seramik malzemelerde termal genleşme veya SinterlemeSinterleme, seramik veya metalik bir tozdan mekanik olarak güçlü bir gövde oluşturmak için kullanılan bir üretim sürecidir. sinterleme nedeniyle numune boyutundaki değişiklikler hakkında bilgi edinilebilir. Ancak bu ifadelerle bilgi içeriği tam olarak kullanılmamaktadır. Daha kapsamlı bir kinetik analiz yardımıyla, bir reaksiyonun farklı sıcaklıklardaki zamanında seyri, yani reaksiyon hızı hakkında bilgi edinmek de mümkündür. Bir reaksiyonun seyri bir matematiksel denklemler sistemi yardımıyla yeterince iyi tanımlanabiliyorsa, reaksiyonun seyri hakkında deneysel olarak erişilemeyen veya sadece zorlukla erişilebilen tahminler yapmak da mümkündür. Bu da süreçleri optimize etmek veya malzeme ve ürünlerin hizmet ömrünü, oksidatif kararlılığını veya yaşlanma davranışını tahmin etmek için kullanılabilir.
Sonuçlar ve Tartışma
Asetilsalisilik asidin termal davranışını daha iyi anlamak amacıyla, deneysel verilerin tanımlanması için bir matematiksel denklem sistemi bulmak amacıyla kinetik bir yaklaşım gerçekleştirilmiştir. Termal davranış, bir NETZSCH TG 209 F1 Libra® kullanılarak ve tablo 1'de özetlenen ölçüm koşulları uygulanarak incelenmiştir. Kinetik bir yaklaşım, genel olarak kinetik değerlendirmelerin ana hedefi olan zaman-sıcaklık korelasyonunu tanımlamak için en az üç farklı ısıtma hızı serisi gerektirir.
Tablo 1: TGA ölçüm parametreleri
| Parametreler | Asetilsalisilik Asit |
|---|---|
| Örnek kütlesi [mg] | 4.982 │ 5.014 │ 5.053 |
| Atmosfer | Argon |
| Pota | Al2O3, 85 μl, açık |
| Sıcaklık programı | RT - 450°C |
| Isıtma oranları [K/dak] | 3 │ 10 │ 30 |
| Gaz akış hızı [ml/dak] | 40 |
| Örnek tutucu | TGA |
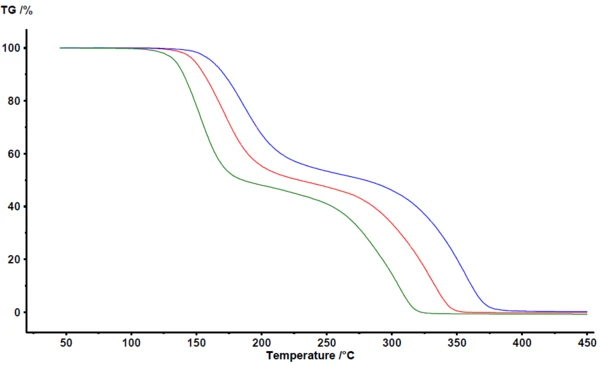
Şekil 1'de NETZSCH Proteus® analiz yazılımında elde edilen sonuçlar gösterilmektedir. Termogravimetri, 100°C ile 400°C arasında asetilsalisilik asidin pirolizi için iki ana kütle kaybı adımı tespit eder. TGA eğrileri, artan ısıtma hızıyla birlikte daha yüksek sıcaklıklara kaymaktadır. large ly paralel kaymanın yanı sıra neredeyse aynı nihai kütle, ısıtma hızının kendisinin reaksiyon mekanizmasını önemli ölçüde değiştirmediğini göstermektedir. Bu da reaksiyon mekanizmasının bu durumda çok karmaşık olmadığının açık bir göstergesidir. Öte yandan, kütle kaybı adımlarının mükemmel bir şekilde ayrılmadığı açıkça görülebilir. İlk kütle kaybı adımının sonunu veya ikinci kütle kaybı adımının başlangıcını açıkça tanımlayan bir plato görünmemektedir. TGA-FT-IR, TGA-MS veya TGA-GC-MS gibi birleştirme teknikleriyle doğrulandığı üzere, hem PirolizPiroliz, organik bileşiklerin inert bir atmosferde termal olarak ayrışmasıdır.piroliz hem de BuharlaşmaBir elementin veya bileşiğin buharlaşması, sıvı fazdan buhara bir faz geçişidir. İki tür buharlaşma vardır: buharlaşma ve kaynama.buharlaşma eş zamanlı olarak gerçekleşmektedir [2][4][5].
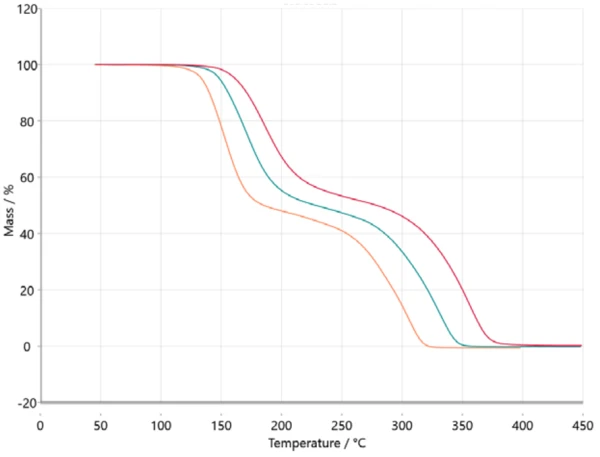
Kinetik analiz için, ölçülen veriler NETZSCH Kinetics Neo yazılımına ASCII aracılığıyla aktarılır. Aktarılan veriler şekil 2'de gösterilmiştir.
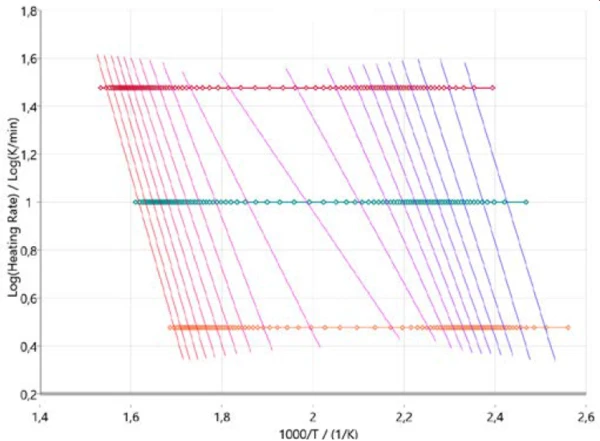
Reaksiyon mekanizması hakkında bir ilk fikir edinmek için kinetik analize modelsiz yaklaşımlarla başlamak faydalı olacaktır. Şekil 3, ısıtma hızının logaritmasının ters sıcaklığa karşı çizildiği Ozawa-Flynn-Wall'a uygun sonuçları göstermektedir. Bu yaklaşım sadece ölçülen tüm veri noktalarını dikkate almakla kalmaz, aynı zamanda reaksiyonun tüm seyri boyunca aktivasyon enerjisindeki değişimin yanı sıra ön-eksponansiyel faktör hakkında da bilgi verir (dönüşüm derecesi). Bu, çok adımlı reaksiyonlar için özellikle yardımcıdır. Çizim, her üç ısıtma hızı (yatay semboller) için reaksiyonun ilerleyişini (sağdan sola) açıklamaktadır. Neredeyse dikey çizgiler her ısıtma hızı için aynı dönüşüm derecesini birbirine bağlar ve bu nedenle izo-dönüşüm çizgileri olarak adlandırılır.
Bu izo-dönüşüm çizgileri, tüm sürecin başında ve sonunda iki ana PirolizPiroliz, organik bileşiklerin inert bir atmosferde termal olarak ayrışmasıdır.piroliz adımı için aralıklarda az çok paraleldir. Yaklaşık %50 dönüşümde, izo-dönüşüm çizgileri reaksiyon mekanizmasında bir değişiklik olduğunu gösteren farklı bir eğim gösterir. Reaksiyonun bu aşamasında, daha önce de belirtildiği gibi PirolizPiroliz, organik bileşiklerin inert bir atmosferde termal olarak ayrışmasıdır.piroliz ve BuharlaşmaBir elementin veya bileşiğin buharlaşması, sıvı fazdan buhara bir faz geçişidir. İki tür buharlaşma vardır: buharlaşma ve kaynama.buharlaşma aynı anda gerçekleşir [2][4][5].
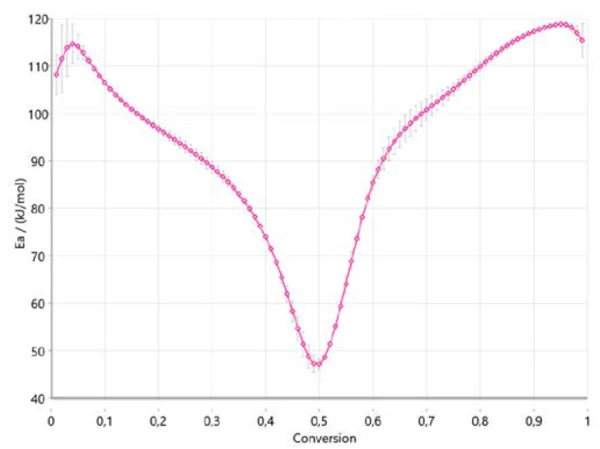
Şekil 4, Ozawa-Flynn-Wall'a uygun olarak reaksiyonun ilerlemesiyle aktivasyon enerjisinin nasıl değiştiğini göstermektedir. Bu çok önemli bir bilgidir çünkü başlangıçta 110 kJ/mol civarında, %40 ile %50 dönüşüm arasında 40 kJ/mol civarında ve reaksiyonun sonunda 120 kJ/mol civarında bir aktivasyon enerjisi ile tüm süreç için üç aralığı göstermektedir. Dönüşüm derecesi ile aktivasyon enerjisindeki değişim, çok adımlı bir reaksiyon mekanizmasını doğrulamaktadır. Elde edilen değerler literatürde yayınlanan sonuçlarla iyi bir korelasyon içindedir [6].
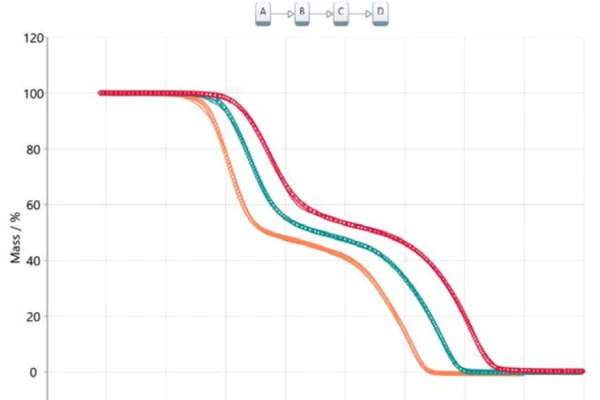
Bu bilginin model tabanlı bir analize aktarılması, A'nın başlangıç maddesini (asetilsalisilik asit) temsil ettiği, B ve C'nin literatürden bilinen ara ürünler olduğu [6, 7] ve D'nin nihai ürün olduğu üç aşamalı ardışık bir modele (t:FnFnFn) yol açar. Bu durumda, nihai ürün elbette gerçek bir madde değildir, ancak her üç termogravimetrik eğri için artık kütle sıfır olduğundan reaksiyonun sonunu veya %100 dönüşümü tanımlar. Oluşan tüm ürünler gaz halindedir ve bu nedenle son sıcaklığa kadar ısıtılırken potadan buharlaşır. Şekil 5, bu model tabanlı yaklaşımın sonucunu göstermektedir. Ölçülen veriler sembollerle, hesaplanan üç aşamalı ardışık modelin sonuçları ise farklı ısıtma hızlarıyla ilişkili renklerle düz çizgiler halinde sunulmuştur. Hesaplanan model deneysel verilere neredeyse mükemmel bir şekilde uymaktadır ve bu da 0,99986 korelasyon katsayısı ile doğrulanmaktadır.
Hesaplanan parametreler ön-eksponansiyel faktör, aktivasyon enerjisi ve reaksiyon sırası her bir reaksiyon adımı için Tablo 2'de özetlenmiştir. Aktivasyon enerjisi için tüm değerler, Ozawa-Flynn-Wall yaklaşımı tarafından önerilen değerlerin yanı sıra literatürde bildirilen değerlerle de iyi bir uyum içindedir [6]. Üç reaksiyon adımının her birinin katkısı sırasıyla %40,3, %13,6 ve %46,1'dir ve bu da sunulan kütle kaybı adımlarıyla iyi bir korelasyon göstermektedir.
Tablo 2: n 'inci dereceden üç adımlı ardışık bir model kullanılarak model-tabanlı yaklaşımdan elde edilen parametreler
| Parametre | 1. Adım (Fn) | 2. Adım (Fn) | 3. Adım (Fn) |
|---|---|---|---|
| Log (PreExp) | 9.88 | 0.88 | 8.02 |
| EA (kJ/mol) | 101.3 | 30.7 | 116.6 |
| Reaksiyon düzeni | 1.01 | 0.91 | 0.77 |
| Katkı (%) | 40.3 | 13.6 | 46.1 |
Sonuç
Literatürde önerilen asetilsalisilik asidin PirolizPiroliz, organik bileşiklerin inert bir atmosferde termal olarak ayrışmasıdır.piroliz mekanizması, ara maddelerin eş zamanlı buharlaşmasını içeren iki aşamalı bir mekanizmadır [6]. Gregory ve arkadaşları, asetik asidin ilk kütle kaybı adımı sırasında açığa çıkan ana bileşik olduğunu bulmuşlardır. Ayrıca, kütle spektrometresi (MS) ile tespit edilen atomik kütle birimleri (amu) ile gösterildiği gibi, çeşitli oligomerler oluşturan bir PirolizPiroliz, organik bileşiklerin inert bir atmosferde termal olarak ayrışmasıdır.piroliz mekanizması önermektedirler [6][7]. Ana gaz ürünlerinin asetik asit, salisilik asit, fenol ve asetilsalisilik asit olduğunun doğrulanmasının yanı sıra, diğer PirolizPiroliz, organik bileşiklerin inert bir atmosferde termal olarak ayrışmasıdır.piroliz ürünlerini ayırmak ve tanımlamak için daha da sofistike bir TGA-GC-MS birleştirme tekniği kullanılmıştır [2]. Tüm yazarlar, reaksiyonun ilerlemesinin %40 ila %60'ı arasında PirolizPiroliz, organik bileşiklerin inert bir atmosferde termal olarak ayrışmasıdır.piroliz ve buharlaşmanın üst üste geldiğini bildirmektedir.
Mevcut çalışmada, bu sonuçları n. dereceden üç aşamalı ardışık bir modelle model tabanlı bir kinetik yaklaşıma uygulamak mümkün olmuştur. Deneysel veriler ve matematiksel model arasındaki iyi korelasyon, 0.99986 korelasyon katsayısı ile doğrulanmıştır. Örneğin aktivasyon enerjisi değerleri, literatürde bildirilen değerlerle iyi bir uyum içindedir. Bununla birlikte, burada tanıtılan üç aşamalı ardışık modelin model tabanlı yaklaşımı, kinetik veriler her bir reaksiyon adımı için bağımsız olarak mevcut olduğundan, Ozawa-Flynn-Wall veya diğerlerine [6] dayanan izo-dönüşümlü modelsiz yaklaşımların kesinlikle bir adım ötesindedir.