Herkunft und Anwendung
Bereits in prähistorischer Zeit wurde Glimmerschiefer abgebaut. Weil sich Glimmer, durch den schichtartigen Aufbau, sehr leicht zu dünnen Schichten brechen lässt, wurde er vor der industriellen Herstellung von Gläsern als Glasersatz in Fenstern verwendet. Heute wird Glimmer als Pigment in Lacken und Kosmetika eingesetzt. Aufgrund der guten Wärmeleitung und der guten elektrischen Isolationseigenschaften ist ein weiteres wichtiges Anwendungsgebiet die Elektronikindustrie, wo Glimmer in Form von Isolierscheiben in Halbleiterbauelementen oder auch als Dielektrikum für sehr verlustarme Kondensatoren eingesetzt wird [1].Bereits in prähistorischer Zeit wurde Glimmerschiefer abgebaut. Weil sich Glimmer, durch den schichtartigen Aufbau, sehr leicht zu dünnen Schichten brechen lässt, wurde er vor der industriellen Herstellung von Gläsern als Glasersatz in Fenstern verwendet. Heute wird Glimmer als Pigment in Lacken und Kosmetika eingesetzt. Aufgrund der guten Wärmeleitung und der guten elektrischen Isolationseigenschaften ist ein weiteres wichtiges Anwendungsgebiet die Elektronikindustrie, wo Glimmer in Form von Isolierscheiben in Halbleiterbauelementen oder auch als Dielektrikum für sehr verlustarme Kondensatoren eingesetzt wird [1].
Struktur
Als Glimmer bezeichnet man eine Gruppe von Mineralien, die zu den Schichtsilikaten gehören. Sie folgen der allgemeinen chemischen Zusammensetzung DG2.3 [T4O10]X2. Eine Schicht wird von miteinander eckenverknüpften SiO2-Tetraedern (für T = Si) gebildet, eine weitere Schicht besteht aus GO6-Oktaedern. Jede Oktaederschicht wird von zwei Tetraederschichten eingeschlossen. Diese T-O-T-Schichtfolge ist jedoch nicht ladungsneutral. Für den Ladungsausgleich sorgen verbrückende Zwischenschichtanionen (X) [2].

Messbedingungen
- Gerät
- TG 209 F1 Libra®
- Probe
- Mica
- Einwaage
- 5.106 mg
- Tiegel
- Al2O3
- Atmosphäre
- Stickstoff
- Gasflussrate
- 40 ml/min
- Heizrate
- 10 K/min
Thermogravimetrie
Das thermische Verhalten von anorganischen Substanzen lässt sich hervorragend mit der Thermowaage charakterisieren. Diese registriert kontinuierlich jede Veränderung der Probenzusammensetzung. Die Verwendung einer dynamischen Heizrate (hier 10 K/min) erlaubt zudem die temperaturabhängige Auswertung von Probenereignissen. Da die verwendete Heizrate ein Maß für die Energiezufuhr darstellt, der die Probe ausgesetzt ist, sind Rückschlüsse über die notwendige Freisetzungsenergie beziehungsweise die Bindungsenergie der freigesetzten Substanzen möglich.
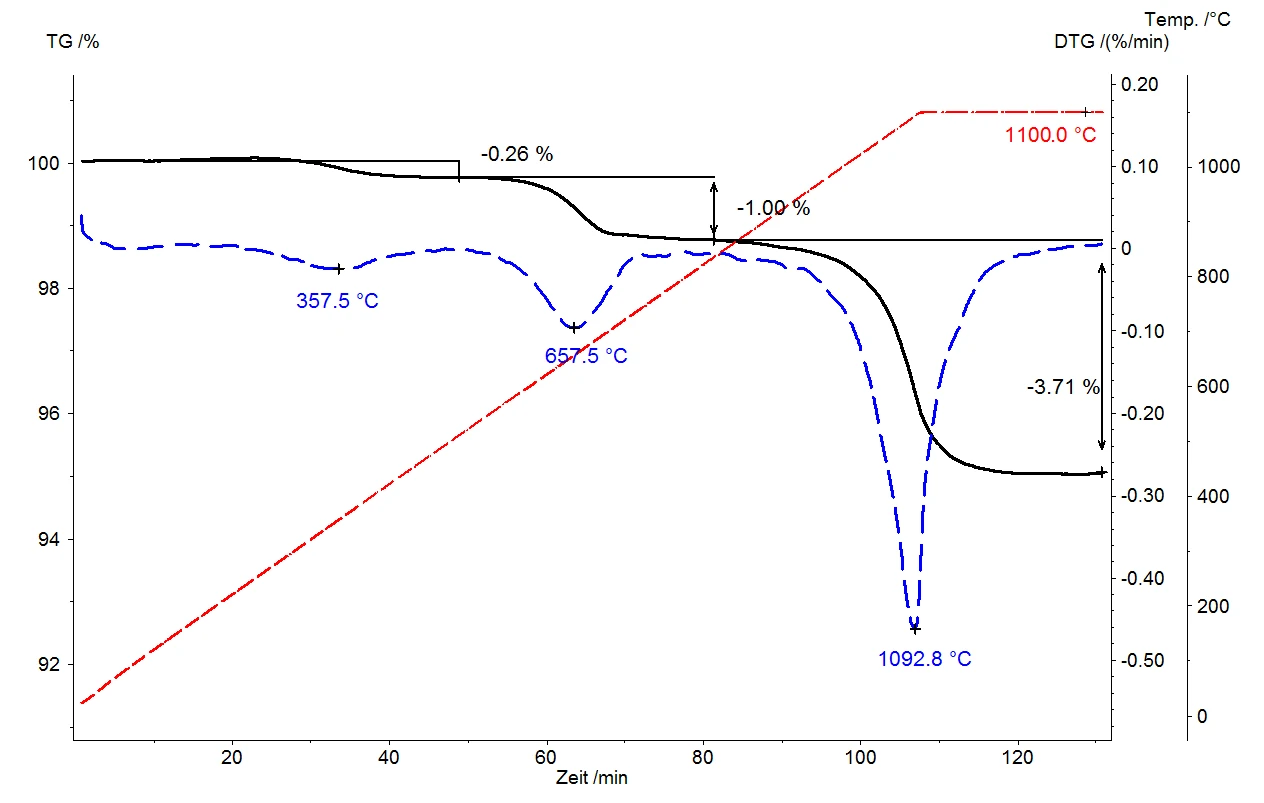
Das Beispiel der Glimmerprobe zeigt drei gut voneinander getrennte Massenverluststufen, eine bei 357 °C, eine weitere bei 657 °C und eine bei 1092 °C. Durch die gute Separierung der Massenverluststufen lassen sich die aus den Proben freigesetzten Gasmengen über die Stufenauswertung bei den jeweiligen Temperaturen leicht quantifizieren. Die relativen Massenänderungen ergeben sich zu 0,26 %, 1,00 % und 3,71 %. Je höher die Freisetzungstemperatur, desto stärker war das freigesetzte Gas vorher an der Kristalloberfläche adsorbiert oder in der Kristallstruktur gebunden. Im Gegensatz zu einer sogenannten „Flash-Pyrolyse“, bei der die Probe in wenigen Sekunden auf die Maximaltemperatur erhitzt wird und somit alle Gase schlagartig freigesetzt werden, ist die Thermogravimetrie speziell durch die sehr variablen Heizraten und die Kombination von dynamischen und isothermen Segmenten in der Lage, die gasförmigen Zersetzungsprodukte temperaturabhängig und damit schrittweise freizusetzen. Das vorliegende Beispiel der Untersuchung einer Glimmerprobe zeigt darüber hinaus, dass das Erwärmen der Probe mit einer Heizrate von 10 K/min auf 1100 °C nicht ausreicht, um die ZersetzungsreaktionEine Zersetzungsreaktion ist eine thermisch induzierte Reaktion einer chemischen Substanz, die fest und/oder gasförmige Zersetzungsprodukte bildet.Zersetzungsreaktion vollständig zu beobachten und damit quantifizieren zu können. Vielmehr war die Kombination mit einer anschließenden Isothermphase von 30 Minuten notwendig, um die Reaktion zu vervollständigen.
Diese Flexibilität in der Temperaturführung erleichtert nicht nur die Quantifizierung, sondern ermöglicht auch die weiterführende Identifizierung der aus der Probe thermogravimetrisch freigesetzten Gase. Dazu eignen sich Gerätekombinationen, die thermoanalytische Messgeräte mit spektroskopischen Methoden wie Massenspektrometrie oder FT-IR-Spektroskopie verbinden, sogenannte Kopplungsapparaturen.