Introduzione
La presenza di ossigeno residuo è un problema ben noto nell'analisi termica (fare riferimento alla terminologia riportata nella norma DIN 51 005). Quando i campioni devono essere analizzati in condizioni di gas inerte, utilizzando ad esempio azoto, argon o elio come gas di lavaggio, la presenza di ossigeno residuo è decisiva nella maggior parte dei casi, poiché l'eventuale OssidazioneL'ossidazione può descrivere diversi processi nel contesto dell'analisi termica.ossidazione del campione porterebbe a risultati indesiderati e a interpretazioni errate.
I campioni metallici che si ossidano in superficie mostrano un segnale DSC EsotermicoUna transizione campionaria o una reazione è esotermica se viene generato calore.esotermico e un aumento della massa del campione. L'OssidazioneL'ossidazione può descrivere diversi processi nel contesto dell'analisi termica.ossidazione può anche essere responsabile di uno spostamento delle temperature di trasformazione di fase. I polimeri o i compositi contenenti sostanze organiche brucerebbero parzialmente in presenza di ossigeno residuo, falsificando il risultato della misurazione durante la Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. decomposizione nominalmente pirolitica.
L'ossigeno residuo negli analizzatori termici viene in genere ridotto al minimo evacuando, riempiendo e spurgando l'apparecchiatura con un gas inerte altamente puro. Questo processo deve essere ripetuto più volte per ridurre al minimo la concentrazione di ossigeno. Il prerequisito più importante per ottenere la più bassa concentrazione di ossigeno possibile è ovviamente uno strumento a tenuta di vuoto. Pertanto, la concentrazione di ossigeno residuo dipende dalla tenuta del vuoto dell'analizzatore termico, delle linee del gas e delle connessioni del gas, nonché dalla purezza del gas inerte di lavaggio. Un'ulteriore pulizia del gas di lavaggio all'esterno dello strumento può essere utile, ma di solito non produce risultati completamente soddisfacenti.
Il sistema OTS®
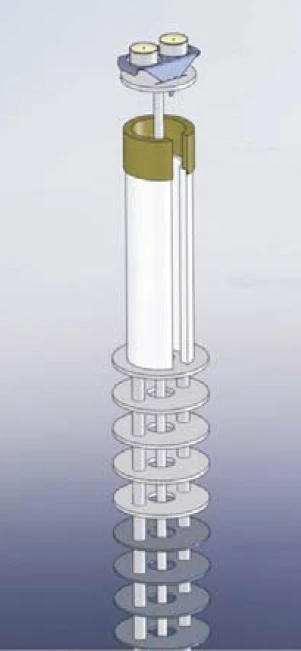
Il sistema OTS® consente un'ulteriore ed efficiente riduzione in situ della concentrazione di ossigeno nel sito del campione. La Figura 1 mostra il sistema OTS® installato in un analizzatore termico simultaneo (STA = TGA + DSC): Al di sotto del crogiolo del campione e del crogiolo di riferimento, e quindi nella zona calda dello strumento, si trova un materiale getter altamente resistente alla temperatura che assorbe l'ossigeno residuo a temperature sufficientemente elevate. Il materiale getter è posizionato da un supporto getter in ceramica, anch'esso altamente resistente alla temperatura e che non reagisce con il materiale getter. Entrambe le parti, il materiale getter e il supporto getter in ceramica, sono posizionate sullo schermo antiradiazioni del portacampioni TGA-DSC.
La simmetria rotazionale garantisce che il sistema OTS® non sia in contatto diretto con il portacampioni. Inoltre, grazie al design a fessura del materiale getter e del supporto getter in ceramica, il sistema OTS® può essere facilmente montato o rimosso. Il gas di lavaggio inerte che scorre verso l'alto entra in contatto prima con il materiale getter e poi con il campione. Pertanto, l'ossigeno residuo presente nel gas di lavaggio viene completamente assorbito dal materiale getter e non può quindi raggiungere il campione.
Risultati e discussione
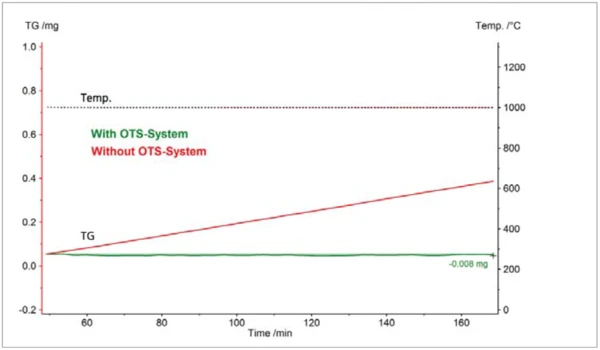
Nella figura 2 sono confrontate due misure TGA sullo zirconio, una con il sistema OTS® e l'altra senza. Entrambe le misurazioni sono state eseguite in un'atmosfera dinamica di elio con una purezza nominale del 99,996%. I campioni sono stati tenuti isotermicamente a 1000°C per circa 2 ore. Senza il sistema OTS®, la massa del campione è aumentata a un ritmo costante, arrivando infine a 0,33 mg. Questo aumento di massa che riflette l'OssidazioneL'ossidazione può descrivere diversi processi nel contesto dell'analisi termica.ossidazione del campione è stato evitato con il sistema OTS®: La massa del campione è rimasta quasi costante. Da questi risultati, si può stimare che il sistema OTS® riduce la concentrazione di ossigeno residuo nel sito di campionamento a meno di ~1 ppm.
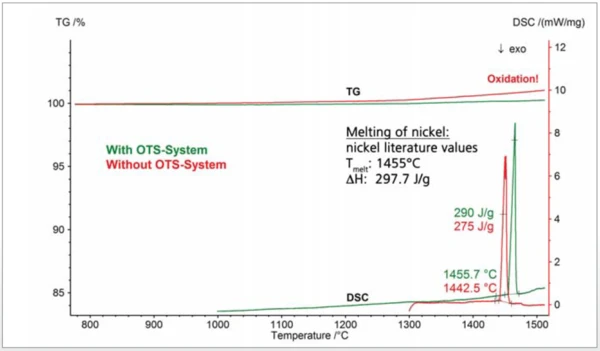
Un altro esempio che dimostra i vantaggi del sistema OTS® è riportato nella figura 3. Due campioni di nichel sono stati analizzati con un analizzatore termico simultaneo. In entrambi i casi è stato utilizzato gas di spurgo argon con una purezza del 99,996%. Il Temperature di fusione ed entalpieL'entalpia di fusione di una sostanza, nota anche come calore latente, è una misura dell'apporto di energia, tipicamente calore, necessario per convertire una sostanza dallo stato solido a quello liquido. Il punto di fusione di una sostanza è la temperatura alla quale essa cambia stato da solido (cristallino) a liquido (fusione isotropa).punto di fusione del nichel, pari a 1455°C, è spesso utilizzato per la termometria ad alta temperatura. Il nichel, tuttavia, è molto sensibile all'OssidazioneL'ossidazione può descrivere diversi processi nel contesto dell'analisi termica.ossidazione che può portare a una riduzione indefinita del Temperature di fusione ed entalpieL'entalpia di fusione di una sostanza, nota anche come calore latente, è una misura dell'apporto di energia, tipicamente calore, necessario per convertire una sostanza dallo stato solido a quello liquido. Il punto di fusione di una sostanza è la temperatura alla quale essa cambia stato da solido (cristallino) a liquido (fusione isotropa).punto di fusione e quindi a una termometria errata. Questo si può notare nella misura senza il sistema OTS®: Il campione si è ossidato, provocando un aumento della curva TGA a causa dell'incremento di massa. Il picco diTemperature di fusione ed entalpieL'entalpia di fusione di una sostanza, nota anche come calore latente, è una misura dell'apporto di energia, tipicamente calore, necessario per convertire una sostanza dallo stato solido a quello liquido. Il punto di fusione di una sostanza è la temperatura alla quale essa cambia stato da solido (cristallino) a liquido (fusione isotropa). fusione DSC si è verificato già a 1443°C, 12°C in meno rispetto al valore di letteratura. Anche l'entalpia diTemperature di fusione ed entalpieL'entalpia di fusione di una sostanza, nota anche come calore latente, è una misura dell'apporto di energia, tipicamente calore, necessario per convertire una sostanza dallo stato solido a quello liquido. Il punto di fusione di una sostanza è la temperatura alla quale essa cambia stato da solido (cristallino) a liquido (fusione isotropa). fusione, pari a 275 J/g, è significativamente inferiore al valore di letteratura, pari a circa 300 J/g. Risultati corretti, corrispondenti ai valori di letteratura, sono stati ottenuti con il sistema OTS®: Il picco diTemperature di fusione ed entalpieL'entalpia di fusione di una sostanza, nota anche come calore latente, è una misura dell'apporto di energia, tipicamente calore, necessario per convertire una sostanza dallo stato solido a quello liquido. Il punto di fusione di una sostanza è la temperatura alla quale essa cambia stato da solido (cristallino) a liquido (fusione isotropa). fusione DSC è stato rilevato a 1455°C e l'entalpia diTemperature di fusione ed entalpieL'entalpia di fusione di una sostanza, nota anche come calore latente, è una misura dell'apporto di energia, tipicamente calore, necessario per convertire una sostanza dallo stato solido a quello liquido. Il punto di fusione di una sostanza è la temperatura alla quale essa cambia stato da solido (cristallino) a liquido (fusione isotropa). fusione è risultata pari a 290 J/g.
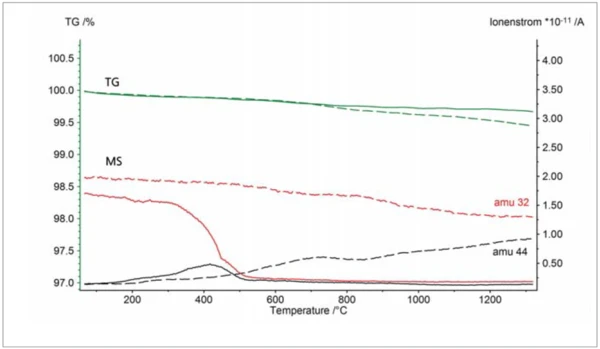
Grazie al sistema OTS®, il campione non si è ossidato in modo significativo. Ciò è visibile attraverso la curva TGA orizzontale, che significa che la massa del campione è rimasta costante nel corso dell'esperimento. Infine, nella figura 4 sono rappresentate due misure TGA-MS su due grafiti, eseguite ancora una volta in gas di purga argon con una purezza del 99,996%. La leggera perdita di massa al di sotto di ~600°C è probabilmente dovuta a idrocarburi volatili, mentre la perdita di massa a temperature più elevate osservata senza il sistema OTS® riflette la parziale combustione della grafite dovuta all'ossigeno residuo (linee tratteggiate): Lo spettrometro di massa ha rilevato un aumento del segnale con numero di massa 44, dovuto all'evoluzione dellaCO2; la graduale diminuzione del segnale con numero di massa 32 riflette il corrispondente consumo di ossigeno residuo. Con il sistema OTS®, la massa del campione è rimasta praticamente costante sopra i ~600°C, il che significa che il campione non ha mostrato ulteriore OssidazioneL'ossidazione può descrivere diversi processi nel contesto dell'analisi termica.ossidazione (linee solide). Inoltre, non è stata rilevata alcuna evoluzione diCO2 in quell'intervallo di temperatura. Dal segnale dell'ossigeno (numero di massa 32), si può anche concludere che il sistema OTS® inizia ad assorbire l'ossigeno residuo sopra i ~300°C e riduce la concentrazione di ossigeno al minimo sopra i ~500°C.
Conclusione
I sistemi di trappola per ossigeno OTS® possono essere utilizzati con diversi analizzatori termici (DSC, TGA, STA, DIL). Rimuove le tracce di ossigeno residuo nell'atmosfera gassosa all'interno dello strumento fino a concentrazioni ben inferiori a 1 ppm.