Introducción
En farmacia, apenas hay un principio activo sobre el que se haya escrito más que sobre el ácido acetilsalicílico (o AAS para abreviar; en los países de habla inglesa y alemana, la marca Aspirin™ se utiliza a menudo incluso como sinónimo). Su historia de éxito comenzó a finales del siglo XIX, cuando el Dr. Felix Hoffmann sintetizó la sustancia en los laboratorios BAYER por primera vez sin impurezas. Hoy en día, sigue siendo uno de los fármacos más populares, utilizado en una amplia gama terapéutica. Pertenece al grupo de los antiinflamatorios no esteroideos (AINE) y está indicado para el tratamiento del dolor, la fiebre y la inflamación. Además, se utiliza para prevenir la recurrencia de infartos de miocardio o ictus en pacientes de alto riesgo. En 1977, el AAS se añadió como analgésico a la "lista de medicamentos esenciales" de la OMS (Organización Mundial de la Salud). [1]
Esta es la última de cuatro notas de aplicación que examinan con más detalle el comportamiento térmico del ácido acetilsalicílico; las tres primeras abordaban la Reacción de descomposiciónUna reacción de descomposición es una reacción inducida térmicamente de un compuesto químico que forma productos sólidos y/o gaseosos. descomposición en diferentes atmósferas gaseosas, la cinética de Reacción de descomposiciónUna reacción de descomposición es una reacción inducida térmicamente de un compuesto químico que forma productos sólidos y/o gaseosos. descomposición y las especies gaseosas resultantes [2, 3, 4].
Experimental
Para la investigación de la Reacción de descomposiciónUna reacción de descomposición es una reacción inducida térmicamente de un compuesto químico que forma productos sólidos y/o gaseosos. descomposición térmica del ácido acetilsalicílico se realizaron mediciones termogravimétricas (TGA) con el NETZSCH TG 209 Libra® bajo atmósfera de helio. Para una interpretación de apoyo, el analizador térmico se acopló adicionalmente a un espectrómetro de masas cuadrupolar 403 Aëolos®. Las condiciones exactas de medición se detallan en la tabla 1.
Cuadro 1: Parámetros de medición
| Parámetros | Ácido acetilsalicílico |
|---|---|
| Analizador | TG 209 Libra® con QMS 403 Aëolos® |
| Soporte de muestras | TGA, tipo S |
| Crisol | Al2O3, 85 μl, abierto |
| Masa de la muestra | 8.35 mg |
| Programa de temperatura | RT a 500°C, velocidad de calentamiento 10 K/min |
| Atmósfera | Helio* (100 ml/min) |
*En este trabajo, una atmósfera de helio se ajustaba a las mediciones incluidas en las anteriores Notas de Aplicación 208, 209 y 210 (Parte 1 a 3).
Resultados de las mediciones y debate
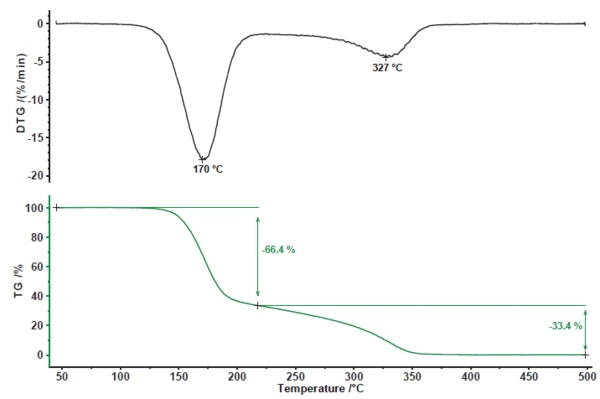
La PirólisisLa pirólisis es la descomposición térmica de compuestos orgánicos en una atmósfera inerte.pirólisis del ácido acetilsalicílico presenta dos etapas de pérdida de masa (figura 1). El primer paso de pérdida de masa del 66,4% se asocia con un pico en la tasa de pérdida de masa (DTG) a 170°C. El segundo paso de pérdida de masa asciende al 33,4% con un pico en la curva DTG a 327°C.
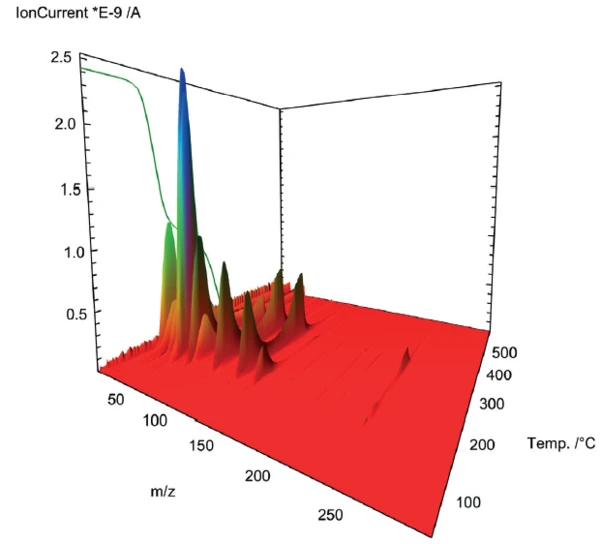
El acoplamiento del espectrómetro de masas utilizado para profundizar en la PirólisisLa pirólisis es la descomposición térmica de compuestos orgánicos en una atmósfera inerte.pirólisis del ácido acetilsalicílico muestra un perfil complejo de desgasificación en los dos pasos de pérdida de masa (figura 2). Para un examen más detallado, se extrajeron los espectros de masas de los respectivos pasos y se sometieron a una comparación de bases de datos con la "NIST MS Library".
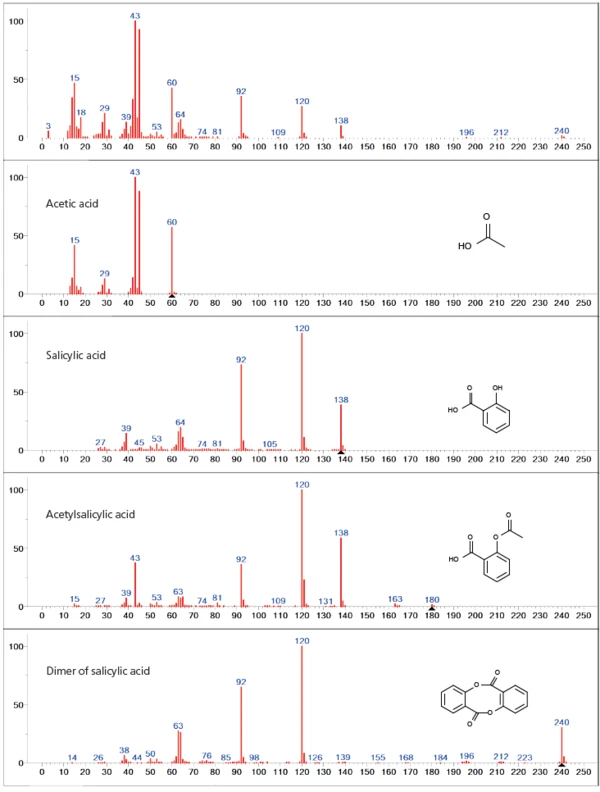
El análisis de la base de datos del primer paso de pérdida de masa muestra principalmente una liberación solapada de ácido acetil y ácido salicílico, lo que indica la degradación de la funcionalidad acetil del ácido acetilsalicílico (figura 3). Junto con los dos principales productos de desgasificación, en el espectro también están representados números de masa más elevados (> 138 u), que pueden atribuirse al dímero del ácido salicílico. Además, no puede excluirse como posibilidad la evaporación parcial del ácido acetilsalicílico no descompuesto dentro del primer paso de pérdida de masa, ya que todas las masas principales del espectro del ácido acetilsalicílico (43, 60, 92, 120, 138 u) se solapan con los productos de Reacción de descomposiciónUna reacción de descomposición es una reacción inducida térmicamente de un compuesto químico que forma productos sólidos y/o gaseosos. descomposición anteriormente mencionados.
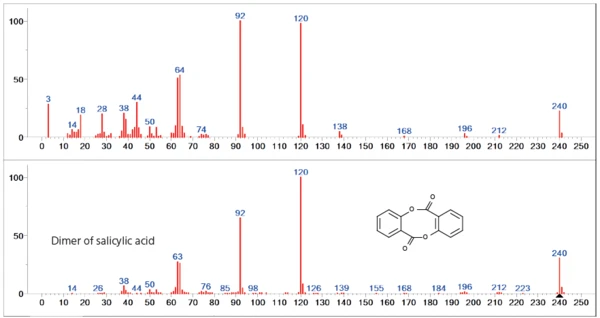
El segundo paso de pérdida de masa está dominado principalmente por la liberación del dímero del ácido salicílico. Sin embargo, especialmente en el rango de masas inferior (< 60u), se observan diferencias con el espectro de la base de datos, lo que indica una liberación de especies gaseosas adicionales (figura 4).
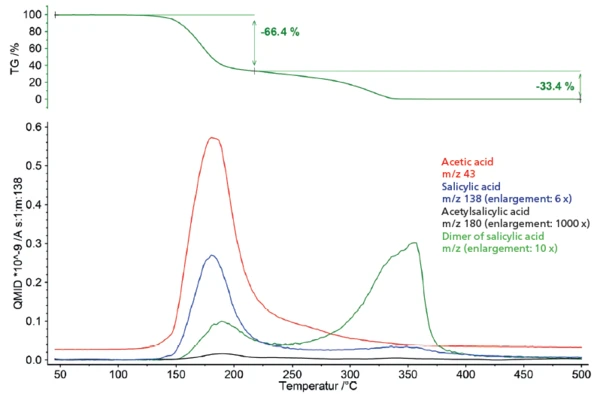
Gracias a los productos de desgasificación detectados, es posible obtener una visión del comportamiento de la desgasificación en función de la temperatura. Para ello, se seleccionaron los números de masa específicos de cada uno de los productos de desgasificación y se representaron en comparación con la curva de pérdida de masa (figura 5). La representación correspondiente ilustra el solapamiento de la degradación térmica del ácido acetilsalicílico y la evaporación del ácido salicílico formado como producto de Reacción de descomposiciónUna reacción de descomposición es una reacción inducida térmicamente de un compuesto químico que forma productos sólidos y/o gaseosos. descomposición dentro del primer paso de pérdida de masa. También resulta obvio que la formación y evaporación de los oligómeros del ácido salicílico ya comienza en el mismo intervalo de temperatura y es el proceso de degradación dominante en el siguiente curso de temperatura.
Resumen
La combinación de termogravimetría y espectrometría de masas es una poderosa herramienta para obtener una visión profunda de los procesos de descomposición térmica y de los gases liberados. El acoplamiento con un espectrómetro de masas permite obtener una visión general de los productos de desgasificación dependientes de la temperatura de una calidad similar a la del método que combina la termogravimetría con la espectroscopia infrarroja. Sin embargo, debido al carácter más específico de los espectros de masas, el acoplamiento con un espectrómetro de masas permite extraer conclusiones más precisas con respecto a las especies gaseosas liberadas.
En resumen, la descomposición térmica del ácido acetilsalicílico en una atmósfera de helio se produce en un proceso de dos pasos compuesto por la separación de la funcionalidad acetilo y la liberación asociada de ácido acético junto con la evaporación del ácido salicílico en forma de oligómero (por ejemplo, dímero). Una vista analítica de gases de los respectivos pasos de pérdida de masa evidenció un solapamiento parcial de los dos procesos debido a la liberación simultánea de ácido acético y salicílico dentro del primer paso de pérdida de masa.
El análisis detallado de los espectros MS obtenidos sugiere que no se puede acceder a todos los productos de desgasificación mediante el acoplamiento directo del TGA a un espectrómetro de masas. Así, especialmente en el segundo paso de pérdida, sólo fue posible asignar claramente partes de los números de masa observados. Sin embargo, la combinación de cromatografía de gases y espectrometría de masas (GC-MS), como ya se mostró en la parte 3 de esta serie de notas de aplicación, presenta una metodología de acoplamiento aún más especializada, que se desarrolló particularmente para este tipo de tarea [4].