Wprowadzenie
Czystość produktów farmaceutycznych i spożywczych idzie w parze z ich jakością. Dostarczane substancje nie powinny zawierać żadnych zanieczyszczeń, które mogłyby być szkodliwe dla organizmu. Szczególnie w przypadku preparatów, zanieczyszczenia nie powinny zakłócać działania substancji czynnej, a tym samym utrudniać jej prawidłowego funkcjonowania. Z tych powodów purity determination ma zasadnicze znaczenie dla substancji leczniczych, kosmetycznych i spożywczych.
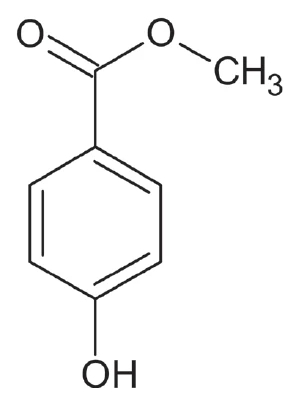
W niniejszym przykładzie określono czystość Nipaginu. Ten biały proszek jest znany pod nazwą chemiczną metyloparaben (rysunek 1) i jest stosowany jako środek konserwujący w kosmetykach, lekach i żywności pod nazwą E218 [1, 2].
Norma ASTM E928-08 opisuje procedurę dla purity determination za pomocą pomiarów DSC. Uwzględnia ona fakt, że "zakres temperatur topnienia związku rozszerza się wraz ze wzrostem poziomu zanieczyszczeń" [3]. Metoda ta ma zastosowanie do mieszanin z zanieczyszczeniami, które rozpuszczają się w stopie i są nierozpuszczalne w krysztale, a więc do tak zwanych zanieczyszczeń eutektycznych.
Warunki testu
Znaczenie rezystancji termicznej - oszczędzające czas oprogramowanie NETZSCH
Zmiany temperatury podczas pomiaru DSC są zwykle mierzone po stronie odniesienia. "Prawdziwa" temperatura próbki zależy od oporu cieplnego pomiędzy tyglem referencyjnym i tyglem próbki, a także od entalpii procesów zachodzących w próbce. Ponieważ znajomość prawidłowej temperatury próbki odgrywa ważną rolę w określaniu czystości, opór cieplny musi zostać obliczony przed testami.libralibraW oprogramowaniu NETZSCH Proteus® dla DSC, obliczanie oporu cieplnego odbywa się jednocześnie z obliczaniem temperatury i entalpii, dzięki czemu uzyskane krzywe automatycznie pokazują rzeczywistą temperaturę wewnątrz próbki.
Pomiary
Przed pomiarami za pomocą DSC 204 F1 Phoenix® , aluminiowe szalki Concavus® zostały umyte w acetonie i podgrzane do 425°C przez jedną minutę. Po umieszczeniu próbki (masa próbki 2,12 mg) w tyglu, została ona hermetycznie zamknięta i umieszczona w celi DSC.
Zakres temperatur musi być starannie dobrany, aby rozpocząć ogrzewanie na długo przed stopieniem, ponieważ Temperatury i entalpie topnieniaEntalpia syntezy substancji, znana również jako ciepło utajone, jest miarą nakładu energii, zazwyczaj ciepła, która jest niezbędna do przekształcenia substancji ze stanu stałego w ciekły. Temperatura topnienia substancji to temperatura, w której zmienia ona stan ze stałego (krystalicznego) na ciekły (stopiony izotropowo).temperatura topnienia może zostać obniżona przez wpływ zanieczyszczeń. Ponadto należy wziąć pod uwagę wstępne topienie, które jest minimalne w przypadku bardzo czystych materiałów, ale może wzrosnąć wraz ze wzrostem zanieczyszczenia.
W pierwszym segmencie próbka została podgrzana od temperatury pokojowej do 100°C z szybkością 20 K/min. W kolejnym segmencie szybkość ogrzewania zmniejszono do 0,7 K/min, a temperaturę zwiększono do 130°C. Podczas całego eksperymentu cela DSC była przedmuchiwana suchym azotem.
Wyniki testów
Rysunek 2 przedstawia krzywą DSC drugiego segmentu ogrzewania. Pik EndotermicznyPrzemiana próbki lub reakcja jest endotermiczna, jeśli do konwersji potrzebne jest ciepło.endotermiczny wynika z topnienia Nipaginy. Wykryta temperatura początku przy 125,4°C jest zgodna z literaturową wartością temperatury topnienia (125,2°C [1]).
Wykres Van't Hoffa, punkty topnienia i czystość
Do obliczenia czystości zastosowano równanie Van't Hoffa, jak opisano w metodzie A ASTM E928-08:
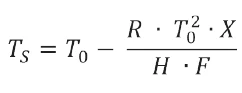
TS: temperatura próbki [K]
T0: Temperatury i entalpie topnieniaEntalpia syntezy substancji, znana również jako ciepło utajone, jest miarą nakładu energii, zazwyczaj ciepła, która jest niezbędna do przekształcenia substancji ze stanu stałego w ciekły. Temperatura topnienia substancji to temperatura, w której zmienia ona stan ze stałego (krystalicznego) na ciekły (stopiony izotropowo).temperatura topnienia czystej Nipaginy [K]
R: stała gazowa (= 8,314 J/mol-1-K-1)
X: ułamek molowy zanieczyszczenia
H: ciepło topnienia [J-mol-1], obliczone na podstawie powierzchni piku
F: frakcja stopiona
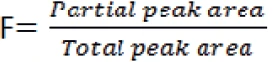
Wykres Van't Hoffa jest graficzną prezentacją danych z purity determination. Porównuje on rzeczywiste dane pomiarowe dla 1/F (odwrotność ułamka piku topnienia) z temperaturą, w której obserwuje się topnienie. Dane te są zazwyczaj nieliniowe; nieliniowość wzrasta wraz ze spadkiem czystości. Odchylenie od liniowości jest spowodowane wstępnym topieniem, którego nie można wykryć za pomocą DSC. Należy zauważyć, że na krzywiznę ma wpływ program temperaturowy pomiaru DSC (rozpoczynający się zbyt blisko piku topnienia) i limity obliczania powierzchni piku (np. lewy limit zbyt blisko piku topnienia).
W celu linearyzacji krzywej oprogramowanie oblicza poprawioną wartość dla F, dodając współczynnik korekcji c do całkowitego obszaru i do każdego obszaru ułamkowego. Ta procedura ostatecznie osiąga liniowość krzywejTs=f(1/F).
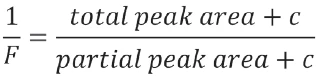
Ponadto masa cząsteczkowa musi zostać wprowadzona do oprogramowania w celu obliczenia wartości mol%.
Rysunek 3 przedstawia obserwowane i skorygowane dane (krzywa liniowa).
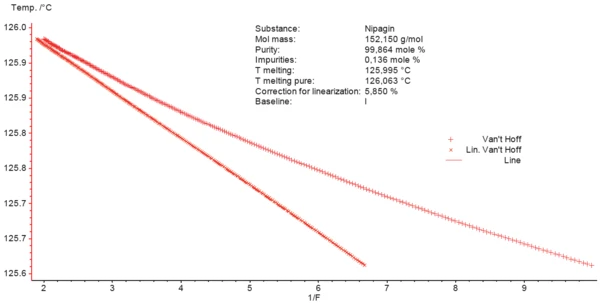
Czystość jest obliczana na podstawie nachylenia skorygowanych danych liniowych. Teoretyczną temperaturę topnienia 100% czystego materiału można również uzyskać z wykresu jako punkt, w którym frakcja stopiona (1/F) wynosi 0 (T topnienia czystego w ramce na rysunku 3). Wynosi ona 126,063°C w porównaniu do temperatury topnienia 125,995°C. Oprogramowanie NETZSCH Purity oblicza zawartość zanieczyszczeń w zmierzonej próbce Nipagin na 0,14% molowych.
Wyniki są wiarygodne tylko wtedy, gdy skorygowane dane wykazują liniowość, poziom czystości jest wyższy niż 98,5%, a współczynnik korekcji c jest niższy niż 20% [3].
Po pomiarze próbka została ponownie zważona, aby upewnić się, że podczas pomiaru nie nastąpiła utrata masy. Zmiana masy początkowej wskazywałaby na OdparowanieOdparowanie pierwiastka lub związku jest przejściem fazowym z fazy ciekłej do pary. Istnieją dwa rodzaje parowania: parowanie i wrzenie.odparowanie substancji lotnych, co skutkowałoby efektem endotermicznym. W ten sposób pik EndotermicznyPrzemiana próbki lub reakcja jest endotermiczna, jeśli do konwersji potrzebne jest ciepło.endotermiczny byłby spowodowany nie tylko topnieniem, ale także uwalnianiem substancji lotnych. Zniekształciłoby to ocenę piku.
Wnioski
Metoda DSC zapewnia łatwy sposób określania czystości czystych materiałów krystalicznych. Czystość jest obliczana na podstawie szybkości topnienia badanego materiału. Na podstawie piku topnienia DSC określa się obniżenie temperatury topnienia, co jest bezpośrednio związane z obecnością zanieczyszczeń.
Warunkiem wstępnym dla purity determination za pomocą DSC jest to, że zanieczyszczenia rozpuszczają się w stopie i są nierozpuszczalne w krysztale. W celu prawidłowego purity determination, należy również zapobiec sublimacji próbki.