Введение
Далее приводятся некоторые термины, характерные для фармацевтической отрасли:
- Термическая стабильность
- Совместимость
- Полиморфизм
- Псевдополиморфизм
1. Термическая стабильность
Стандарт ASTM E2550 описывает термическую стабильность материала как "температуру, при которой материал начинает разлагаться или реагировать, и степень изменения массы с помощью термогравиметрии". Кроме того, "отсутствие реакции или разложения используется как показатель термической стабильности".
На рисунке 1 представлена кривая ТГА ацетилсалициловой кислоты при нагревании до 600°C в атмосфере азота.
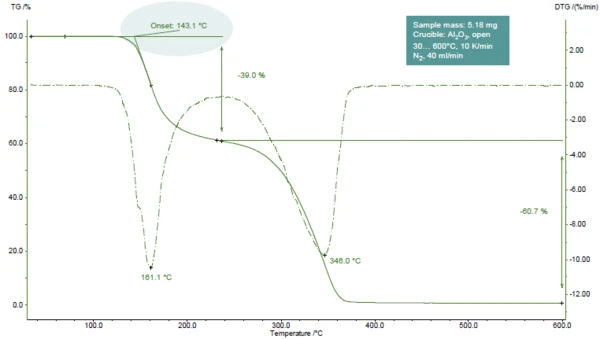
Обнаружены два этапа потери массы, легко узнаваемые по двум пикам на кривой DTG (1-я производная кривой TGA). ТГА-ФТ-ИК-исследования показали, что на первом этапе выделяются уксусная кислота (основная часть) и салициловая кислота. На втором этапе выделяются салициловая кислота иCO2 (образующийся при дальнейшем разложении ацетилсалициловой кислоты) [1].
Каждый из этих этапов потери массы определяется:
- температурой
- изменением массы
Теоретически для одного этапа потери массы можно выделить три температуры:
- Температура пика ДТГ (1-я производная кривой ТГА)
- Экстраполированная температура начала процесса в соответствии со стандартом ISO 11358-1. Это "точка пересечения базовой линии в начале измерения и касательной к кривой ТГА в точке максимального градиента"
Температура начала измерения в соответствии с ASTM E2550. Это "точка на кривой ТГА, где впервые наблюдается отклонение от установленной базовой линии до термического события"
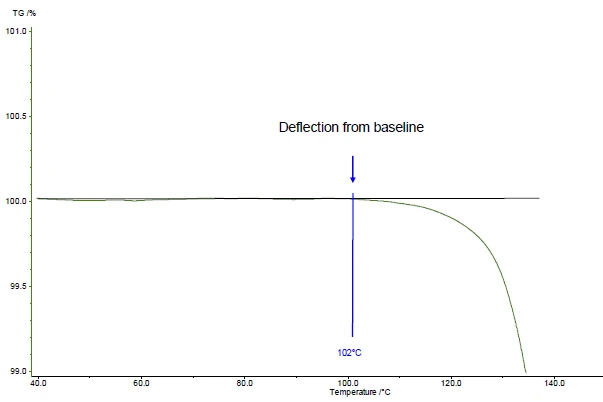
В представленном примере первый шаг потери массы происходит при 161°C (пик кривой DTG, рисунок 1), при 143°C (экстраполированная температура начала кривой TGA, рисунок 1) или 102°C (температура начала согласно ASTM E2550, рисунок 2). Это третье значение используется для оценки термической стабильности.
Метод ограничен материалами, которые реагируют или разлагаются в исследуемом диапазоне температур, и не может быть использован для сублимации или испарения.
Примечания относительно условий измерения:
Поскольку на результаты влияют масса образца, атмосфера (газ и скорость потока), скорость нагрева и тип тигля, крайне важно указать условия измерения. По этой же причине результаты для двух образцов можно сравнивать только в том случае, если измерения проводились в абсолютно одинаковых условиях.
В целом, рекомендуются следующие условия измерений:
- Масса образца: от 1 до 10 мг, например, 5 мг
- Скорость нагрева: от 10 до 20 К/мин (для энергичных реакций ниже: от 1 до 10 К/мин)
- Скорость потока атмосферы: 20-100 мл/мин
В представленном примере термическая стабильность при 102°C для ацетилсалициловой кислоты приведена для измерения в динамической атмосфере азота (поток газа: 40 мл/мин), проведенного на образце массой 5 мг при скорости нагрева 10 К/мин (рис. 2).
Термическая стабильность и срок годности
Анализ по методу кинетики Нео
Термогравиметрические измерения показывают влияние температуры на материал в заданной атмосфере. Если наблюдаемая потеря массы зависит от скорости нагрева, то можно использовать измерения ТГА при различных скоростях нагрева для проведения кинетического анализа реакции. Для этого NETZSCH предлагает программное обеспечение Kinetics Neo. Оно позволяет моделировать кинетику одно- и многостадийных реакций. Программа может отнести каждый отдельный этап к различным типам реакций с собственными кинетическими параметрами, такими как энергия активации, порядок реакции и предэкспоненциальный коэффициент. На основе полученных результатов Kinetics Neo может смоделировать реакцию(и) для заданных пользователем температурных программ, например, для изотерм с длительным периодом. Поэтому прогнозы, рассчитанные с помощью Kinetics Neo, дают информацию о сроке годности с учетом термической стабильности материала, то есть о времени, в течение которого он остается стабильным в заданных атмосферных и температурных условиях.
Определение термической стабильности
Пример определения срока годности с учетом термической стабильности фармацевтического продукта приведен на сайте NETZSCH Application Note 122 [2].
Примечания по определению срока годности лекарственного средства с учетом термической стабильности:
- Проведите измерения ТГА при различных скоростях нагрева
- Проведите оценку кинетики с помощью программы Kinetics Neo
- Используйте полученную кинетическую модель для прогнозирования поведения образца при заданных температурах и времени
- Проверьте кинетическую модель, сравнив измерение при изотермической температуре с кривой, рассчитанной Kinetics Neo.
Важные замечания:
- На срок годности продукта влияют и другие факторы, помимо температуры и атмосферы, например, влажность, свет или потеря смешиваемости в случае с мазями. Поэтому прогнозы, выполненные с помощью TGA и Kinetics Neo, не дают информации о полном сроке годности продукта, а только о его сроке годности в отношении термической стабильности.
- Прогнозы справедливы для веществ, которые находятся в одинаковом физическом состоянии при температуре прогнозирования и при температуре начала разложения. Если вещество находится в твердом состоянии при комнатной температуре и плавится до начала разложения, то кинетический анализ разложения действителен только для жидкого состояния. В этом случае прогнозирование с использованием рассчитанной модели невозможно при температурах ниже точки плавления.
2. Совместимость
Как правило, фармацевтическая формула содержит один активный фармацевтический ингредиент и несколько вспомогательных веществ.
Активный фармацевтический ингредиент, также называемый API (Active Pharmaceutical Ingredient), - это вещество, оказывающее "прямое воздействие на диагностику, лечение, смягчение, терапию или профилактику заболевания" [3].
Различные вспомогательные вещества преследуют разные цели: они могут облегчить производственный процесс, улучшить внешний вид конечного продукта (цвет, вкус) и помочь правильно доставить API.
Присутствие вспомогательных веществ в рецептуре не должно влиять на эффективность, стабильность или безопасность препарата. Другими словами, необходимо убедиться в совместимости АФИ и вспомогательных веществ.
Первоначальную информацию о совместимости лекарственного средства и вспомогательного вещества можно получить с помощью термического анализа, в частности, ДСК и ТГА.
Указания по определению взаимодействия API и эксипиента:
- Проведите измерения ДСК и ТГА для API и, отдельно, для эксипиента
- Смешайте API и эксципиент (50/50 по весу)
- Проведите измерения ДСК и ТГА для смеси API+эксципиент
Кривые ДСК API, вспомогательных веществ и смесей
На рисунке 3 показано, как кривые ДСК дают информацию о потенциальном взаимодействии между двумя компонентами. Кривая ДСК, которая не показывает взаимодействия между API и эксципиентом (рисунок 3c), указывает на то, что эксципиент рекомендуется для рецептуры с использованием API. Появление нового пика в смеси, исчезновение пика или изменение пика плавления (по форме, положению или энтальпии) указывает на наличие взаимодействия между двумя компонентами (рис. 3д). Однако это не обязательно означает, что лекарство и эксципиент несовместимы. Для подтверждения несовместимости необходимо провести дополнительные исследования с помощью других методов (рентгенография, спектроскопия, хроматография и т. д.).
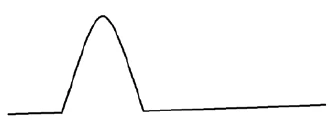
a) Кривая ДСК API с пиком плавления

b) Кривая ДСК вспомогательного вещества с пиком плавления
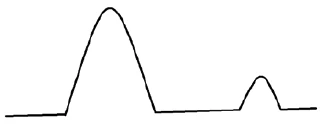
в) Кривая ДСК смеси API+эксципиент БЕЗ взаимодействия между двумя компонентами. Обнаружен один пик плавления при той же температуре, что и на кривых ДСК для отдельных компонентов. Это означает, что API и эксципиент совместимы.
в) Кривая ДСК смеси API+эксципиент БЕЗ взаимодействия между двумя компонентами. Обнаружен один пик плавления при той же температуре, что и на кривых ДСК для отдельных компонентов. Это означает, что API и эксципиент совместимы.
Функция "Наложение" в программе оценки NETZSCH позволяет изобразить кривую, которая была бы получена для смеси при отсутствии взаимодействия между двумя компонентами. Для этого кривые отдельных веществ загружаются в программу оценки, и рассчитывается "наложенная" кривая. Затем очень легко провести сравнение между измеренной кривой смеси и кривой, рассчитанной с помощью метода наложения.
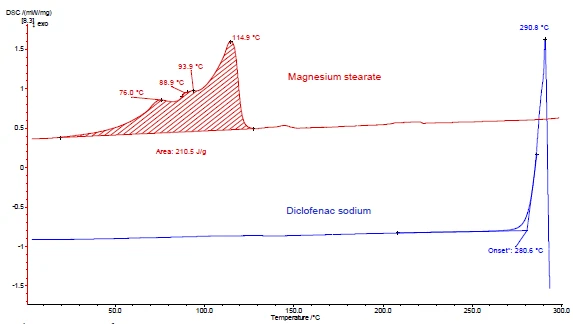
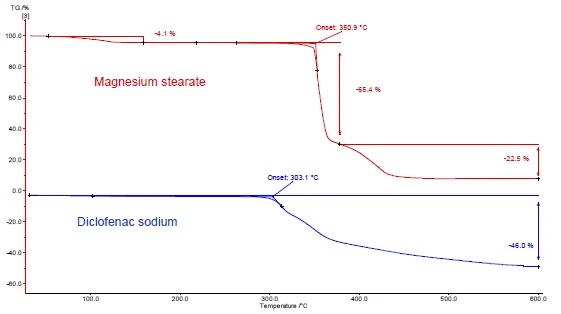
На рисунках 4 и 5 показано, как это делается на примере диклофенака натрия и стеарата магния. Были проведены измерения ДСК и ТГА. На рисунках 4а и 5а представлены кривые ДСК и ТГА, соответственно, двух веществ при нагревании.
Эндотермический пик между комнатной температурой и 130°C, обнаруженный на кривой ДСК стеарата магния (рис. 4a, красная кривая, вверху), частично обусловлен испарением воды. Он соответствует потере массы на кривой ТГА (4,1 %) для этого температурного диапазона. Пик выделения воды перекрывается плавлением стеарата магния [9].
Диклофенак натрия (рис. 4a, синяя кривая, ниже) демонстрирует эндотермический пик при 291°C, соответствующий его плавлению. Экзотермический процесс, следующий сразу за плавлением, связан с потерей массы на 46 % и является результатом разложения диклофенака.

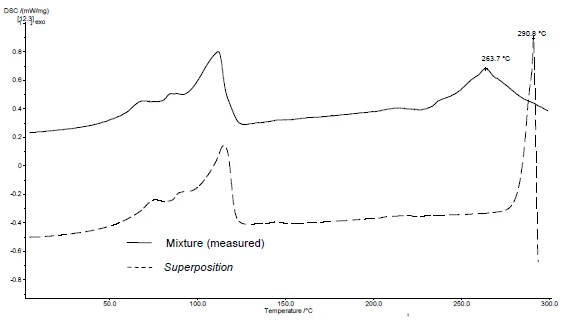

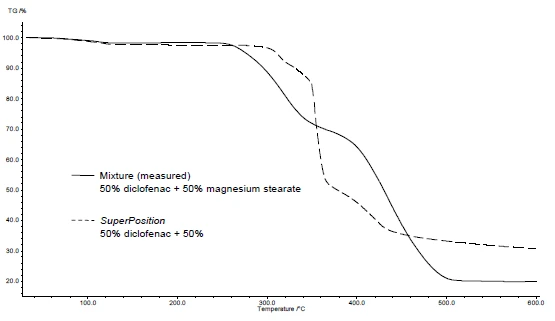
Применение SuperPosition (рис. 4b, 5b) позволяет сравнить измеренную кривую смеси с расчетной кривой, которая была бы получена в случае отсутствия взаимодействия. Отсутствие разницы между двумя кривыми указывает на совместимость смеси.
В данном примере разложение смеси начинается при 278°C, т.е. при более низкой температуре, чем для одного только эксципиента (рис. 5c). Пик плавления, характерный для диклофенака, в смеси больше не наблюдается. Вместо этого обнаруживается широкий эндотермический пик при 264°C (рис. 4c).
Тот факт, что в данном примере обнаружены различия, указывает на наличие взаимодействия между диклофенаком натрия и стеаратом магния (рисунки 4c и 5c).
Еще один пример исследования совместимости диклофенака натрия с различными вспомогательными веществами с помощью ДСК и ТГА приведен в NETZSCH Application Note 120 [4].
3. Полиморфизм
Полиморфизм - это способность материала существовать более чем в одной кристаллической форме. Различные полиморфные формы фармацевтической субстанции обычно называют α, β, ... или I, II, ... или A, B, ..., где модификация α/I/A является наиболее стабильной.
В фармацевтической промышленности полиморфизм представляет собой очень сложную задачу, поскольку даже если два полиморфных вещества имеют одинаковый химический состав, они отличаются по своим свойствам. Поскольку полиморфное вещество может менять свою структуру с течением времени, при хранении могут произойти неожиданные изменения в его биодоступности, физических свойствах, стабильности и т.д. По этой причине, а также для регистрации патента, очень важно знать и быть осведомленным о существовании всех возможных модификаций полиморфного вещества, а также о свойствах, стабильности и качестве каждой из них.
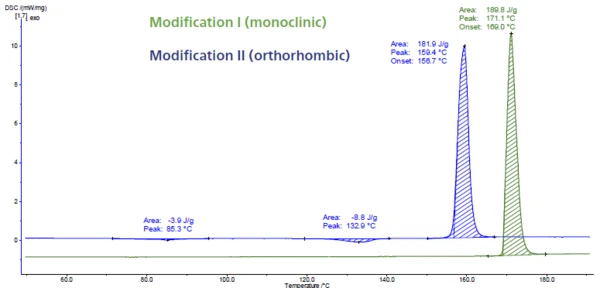
На рисунке 6 показано измерение ДСК парацетамола. Этот API (активный фармацевтический ингредиент) имеет три модификации, называемые I, II и III. Модификация III нестабильна, поэтому ее трудно охарактеризовать. Модификации I и II отличаются термодинамической стабильностью и способностью к сжатию. Их можно легко идентифицировать с помощью ДСК, поскольку температура плавления определяется при разных температурах. Пик плавления при 169 °C (экстраполированная температура начала плавления, зеленая кривая) характерен для моноклинной формы. Это модификация с самой высокой температурой плавления, а также самая стабильная. Пик при 157°C (экстраполированная температура начала плавления, синяя кривая) принадлежит орторомбической форме, которая отличается лучшими компрессионными свойствами [5, 6].
Хотя форма II может быть непосредственно спрессована без добавления вспомогательных веществ для улучшения сжимаемости, коммерческий парацетамол производится из моноклинной формы (форма I) из-за ее лучшей стабильности [7, 8].
Другие примеры характеристики различных модификаций полиморфного вещества приведены в NETZSCH Application Note 127 [10].
4. Псевдополиморфизм
Две псевдополиморфные модификации имеют различные кристаллические формы, возникающие в результате гидратации или сольватации.
В сольвате молекулы растворителя оказываются втянутыми в кристаллическую структуру вещества. Если он содержит более двух растворителей, его называют гетеросольватом.
В гидрате растворителем в соединении с лекарством является вода.
Характеристика сольватов и гидратов осуществляется с помощью термогравиметрии, возможно, в сочетании с анализом улетучивающихся газов. Измерение методом ТГА дает информацию о количестве растворителя/воды, присутствующих в образце, и, следовательно, о степени сольватации/гидратации. Сопряжение позволяет идентифицировать растворители, выделяющиеся при нагревании.
Заключение
С помощью термического анализа, в частности ДСК и ТГА, можно исследовать различные свойства API и вспомогательных веществ. Это, в свою очередь, позволяет определить термическую стабильность, совместимость, а также полиморфизм и псевдополиморфизм лекарственных препаратов.