Giriş
Aşağıda, farmasötik alana özgü bazı terimler açıklanmaktadır:
- Termal stabilite
- Uyumluluk
- PolimorfizmPolimorfizm, katı bir maddenin farklı kristal yapılar oluşturma yeteneğidir (eşanlamlılar: formlar, modifikasyonlar).Polimorfizm
- Sözde PolimorfizmPolimorfizm, katı bir maddenin farklı kristal yapılar oluşturma yeteneğidir (eşanlamlılar: formlar, modifikasyonlar).polimorfizm
1. Termal Kararlılık
ASTM E2550 standardı bir malzemenin termal kararlılığını "malzemenin ayrışmaya veya reaksiyona girmeye başladığı sıcaklık ve termogravimetri kullanılarak kütle değişiminin derecesi" olarak tanımlamaktadır. "Reaksiyon veya ayrışmanın olmaması termal kararlılığın bir göstergesi olarak kullanılır" diye de ekler.
Şekil 1, asetilsalisilik asidin azot atmosferinde 600°C'ye ısıtılması sırasındaki TGA eğrisini göstermektedir.
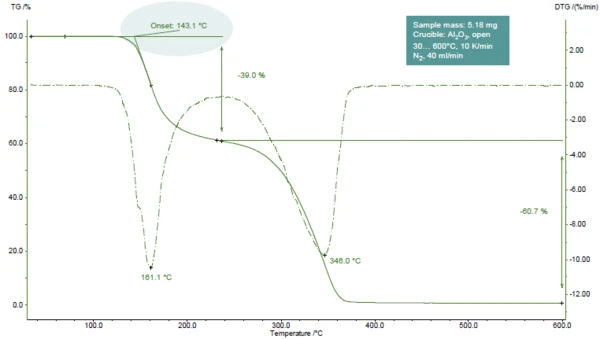
DTG eğrisindeki (TGA eğrisinin1. türevi) iki tepe noktası ile kolayca tanınabilen iki kütle kaybı adımı tespit edilmiştir. TGA-FT-IR incelemeleri, ilk adım sırasında asetik asit (ana kısım) ve salisilik asidin geliştiğini göstermiştir. İkinci adımda, salisilik asit veCO2 (asetilsalisilik asidin daha fazla ayrışmasından kaynaklanan) açığa çıkar [1].
Bu kütle kaybı adımlarının her biri aşağıdakiler tarafından belirlenir:
- sıcaklık
- kütle değişimi
Teorik olarak, bir kütle kaybı adımı için üç sıcaklık gösterilebilir:
- DTG'nin tepe sıcaklığı (TGA eğrisinin 1. türevi)
- ISO 11358-1 standardına göre ekstrapole edilmiş başlangıç sıcaklığı. Bu, "ölçümün başlangıcındaki taban çizgisi ile maksimum gradyan noktasında TGA eğrisine teğet olan kesişme noktasıdır"
ASTM E2550'ye göre başlangıç sıcaklığı. Bu, "TGA eğrisinde, termal olaydan önce belirlenen temel çizgiden sapmanın ilk gözlemlendiği noktadır"
Sunulan örnekte, ilk kütle kaybı adımı 161°C'de (DTG eğrisinin tepe noktası, şekil 1), 143°C'de (TGA eğrisinin ekstrapole edilmiş başlangıç sıcaklığı, şekil 1) veya 102°C'de (ASTM E2550'ye göre başlangıç sıcaklığı, şekil 2) gerçekleşir. Bu üçüncü değer termal stabilitenin değerlendirilmesi için kullanılır.
Yöntem, incelenen sıcaklık aralığında reaksiyona giren veya ayrışan malzemelerle sınırlıdır ve süblimleşme veya BuharlaşmaBir elementin veya bileşiğin buharlaşması, sıvı fazdan buhara bir faz geçişidir. İki tür buharlaşma vardır: buharlaşma ve kaynama.buharlaşma için kullanılamaz.
Ölçüm koşullarına ilişkin notlar:
Sonuçlar numune kütlesi, atmosfer (gaz ve akış hızı), ısıtma hızı ve kroze tipinden etkilendiğinden, ölçüm koşullarından bahsetmek çok önemlidir. Aynı nedenle, iki numune için sonuçlar ancak ölçümler tamamen aynı koşullar altında gerçekleştirilirse karşılaştırılabilir.
Genel olarak, aşağıdaki ölçüm koşulları tavsiye edilir:
- Numune kütlesi: 1 ila 10 mg arasında, örneğin 5 mg
- Isıtma hızı: 10 ila 20 K/dak (enerjik reaksiyonlar için daha düşük: 1 ila 10 K/dak)
- Atmosferin akış hızı: 20 ila 100 ml/dak
Sunulan örnekte, asetilsalisilik asit için 102°C'deki Termal KararlılıkBir malzeme sıcaklığın etkisi altında ayrışmıyorsa termal olarak kararlıdır. Bir maddenin termal kararlılığını belirlemenin bir yolu TGA (termogravimetrik analizör) kullanmaktır. termal kararlılık, 10 K/dak'lık bir ısıtma hızında 5 mg'lık bir numune üzerinde gerçekleştirilen dinamik bir azot atmosferindeki (gaz akışı: 40 ml/dak) bir ölçüm için verilmiştir (Şekil 2).
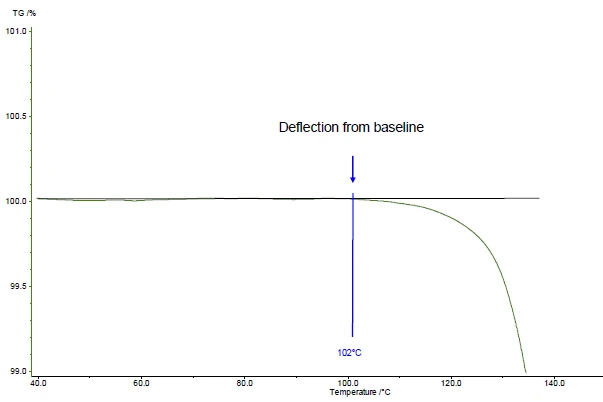
Termal Stabilite ve Raf Ömrü
Kinetik Neo ile Analiz
Bir termogravimetrik ölçüm, belirli bir atmosferde sıcaklığın bir malzeme üzerindeki etkisini gösterir. Gözlenen kütle kaybı ısıtma hızına bağlıysa, reaksiyonun kinetik analizini yapmak için farklı ısıtma hızlarında TGA ölçümlerini kullanmak mümkündür. Bunun için NETZSCH Kinetics Neo yazılımını sunmaktadır. Tek ila çok adımlı reaksiyonların kinetiğinin modellenmesine olanak tanır. Bu yazılım, her bir adımı aktivasyon enerjisi, reaksiyon sırası ve ön-eksponansiyel faktör gibi kendi kinetik parametrelerine sahip farklı reaksiyon türlerine atayabilir. Sonuçlara dayanarak Kinetics Neo, kullanıcı tarafından belirlenen sıcaklık programları için, örneğin uzun süreli izotermler için reaksiyon(lar)ı simüle edebilmektedir. Bu nedenle Kinetics Neo ile hesaplanan tahminler, bir malzemenin termal kararlılığına ilişkin raf ömrü, yani belirli bir atmosfer ve sıcaklık koşulları altında kararlı kaldığı süre hakkında bilgi verir.
Termal Stabilitenin Belirlenmesi
Bir farmasötik ürünün termal stabilitesi açısından raf ömrünün belirlenmesine ilişkin bir örnek NETZSCH Uygulama Notu 122'de açıklanmaktadır [2].
Bir ilacın raf ömrünün termal stabilite açısından belirlenmesine ilişkin notlar:
- TGA ölçümlerini farklı ısıtma hızlarında gerçekleştirin
- Kinetik değerlendirmesini Kinetics Neo ile gerçekleştirin
- Belirlenen sıcaklık ve süreler için numune davranışını tahmin etmek üzere belirlenen kinetik modeli kullanın
- Kinetik modeli, İzotermalKontrollü ve sabit sıcaklıkta yapılan testlere izotermal denir.izotermal sıcaklıkta yapılan bir ölçüm ile Kinetics Neo tarafından hesaplanan eğriyi karşılaştırarak doğrulayın.
Önemli Açıklamalar:
- Sıcaklık ve atmosfer dışındaki faktörler de bir ürünün raf ömrünü etkiler, örneğin nem, ışık veya merhemler söz konusu olduğunda karışabilirlik kaybı. Bu nedenle TGA ve Kinetics Neo ile yapılan tahminler bir ürünün tüm raf ömrü hakkında bilgi vermez, sadece termal stabilite açısından raf ömrü hakkında bilgi verir.
- Tahminler, tahmin sıcaklığında ve ayrışmanın başladığı sıcaklıkta aynı fiziksel durumda olan maddeler için geçerlidir. Eğer bir madde oda sıcaklığında katı haldeyse ve ayrışmaya başlamadan önce eriyorsa, ayrışmanın kinetik analizi sadece sıvı hal için geçerlidir. Böyle bir durumda, Erime Sıcaklıkları ve EntalpileriGizli ısı olarak da bilinen bir maddenin füzyon entalpisi, bir maddeyi katı halden sıvı hale dönüştürmek için gerekli olan enerji girdisinin, tipik olarak ısının bir ölçüsüdür. Bir maddenin erime noktası, katı (kristal) halden sıvı (izotropik eriyik) hale geçtiği sıcaklıktır.erime noktasının altındaki sıcaklıklarda hesaplanan model kullanılarak hiçbir tahmin yapılamaz.
2. Uyumluluk
Genel olarak, bir farmasötik formülasyon bir aktif farmasötik bileşen ve birkaç yardımcı madde içerir.
API (Aktif Farmasötik Bileşen) olarak da adlandırılan aktif farmasötik bileşen, "hastalığın teşhisi, tedavisi, hafifletilmesi, tedavisi veya önlenmesi üzerinde doğrudan etkisi olan" maddedir [3].
Çeşitli yardımcı maddeler için farklı hedefler vardır: üretim sürecini kolaylaştırabilir, nihai ürünün görünümünü iyileştirebilir (renk, tat) ve API'nin doğru şekilde iletilmesine yardımcı olabilirler.
Formülasyondaki yardımcı maddelerin varlığı ilacın etkinliğini, stabilitesini veya güvenliğini etkilememelidir. Başka bir deyişle, API ve yardımcı maddelerin uyumlu olması sağlanmalıdır.
Bir ilaç ve yardımcı maddenin uyumluluğu hakkında ilk bilgiler termal analizle, daha spesifik olarak DSC ve TGA ile elde edilebilir.
API ve eksipiyan üzerindeki etkileşimlerin belirlenmesine ilişkin notlar:
- API ve ayrı olarak eksipiyan üzerinde DSC ve TGA ölçümleri yapın
- API ve eksipiyanı karıştırın (50/50 ağırlık)
- API+excipient karışımı üzerinde DSC ve TGA ölçümlerini çalıştırın
API, Yardımcı Madde ve Karışımların DSC Eğrileri
Şekil 3, DSC eğrilerinin iki bileşen arasındaki potansiyel etkileşim hakkında nasıl bilgi verdiğini göstermektedir. API ve eksipiyan arasında etkileşim olmadığını gösteren bir DSC eğrisi (şekil 3c), eksipiyanın API kullanılan formülasyon için tavsiye edildiğini gösterir. Karışımda yeni bir pikin oluşması, bir pikin kaybolması veyaErime Sıcaklıkları ve EntalpileriGizli ısı olarak da bilinen bir maddenin füzyon entalpisi, bir maddeyi katı halden sıvı hale dönüştürmek için gerekli olan enerji girdisinin, tipik olarak ısının bir ölçüsüdür. Bir maddenin erime noktası, katı (kristal) halden sıvı (izotropik eriyik) hale geçtiği sıcaklıktır. erime pikinde (şekil, konum veya entalpi olarak) bir değişiklik olması iki bileşen arasında bir etkileşim olduğunu gösterir (şekil 3d). Ancak bu, ilaç ve yardımcı maddenin uyumlu olmadığı anlamına gelmez. Uyumsuzluğu doğrulamak için diğer tekniklerle (X-ışını, spektroskopi, kromatografi vb.) ek incelemeler yapılması gerekecektir.
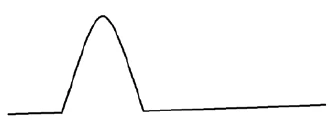
a) Erime piki ile API'nin DSC eğrisi

b) Erime piki ile birlikte eksipiyanın DSC eğrisi
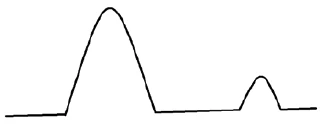
c) İki bileşen arasında etkileşim OLMADAN API+eksipiyan karışımının DSC eğrisi. Tek tek bileşenler için DSC eğrilerinde olduğu gibi aynı sıcaklıkta birErime Sıcaklıkları ve EntalpileriGizli ısı olarak da bilinen bir maddenin füzyon entalpisi, bir maddeyi katı halden sıvı hale dönüştürmek için gerekli olan enerji girdisinin, tipik olarak ısının bir ölçüsüdür. Bir maddenin erime noktası, katı (kristal) halden sıvı (izotropik eriyik) hale geçtiği sıcaklıktır. erime piki tespit edilmiştir. Bu, API ve eksipiyanın uyumlu olduğu anlamına gelir.
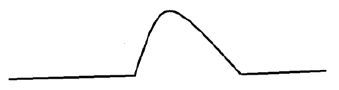
c) İki bileşen arasında etkileşim OLMADAN API+eksipiyan karışımının DSC eğrisi. Tek tek bileşenler için DSC eğrilerinde olduğu gibi aynı sıcaklıkta birErime Sıcaklıkları ve EntalpileriGizli ısı olarak da bilinen bir maddenin füzyon entalpisi, bir maddeyi katı halden sıvı hale dönüştürmek için gerekli olan enerji girdisinin, tipik olarak ısının bir ölçüsüdür. Bir maddenin erime noktası, katı (kristal) halden sıvı (izotropik eriyik) hale geçtiği sıcaklıktır. erime piki tespit edilmiştir. Bu, API ve eksipiyanın uyumlu olduğu anlamına gelir.
NETZSCH değerlendirme yazılımındaki Süperpozisyon özelliği, iki bileşen arasında hiçbir etkileşim olmaması durumunda bir karışım için elde edilecek eğrinin tasvir edilmesine olanak tanır. Bunu gerçekleştirmek için, tek tek maddelerin eğrileri değerlendirme yazılımına yüklenir ve "üst üste bindirilmiş" eğri hesaplanır. Daha sonra karışımın ölçülen eğrisi ile Süperpozisyon yoluyla hesaplanan eğri arasında bir karşılaştırma yapmak çok kolaydır.
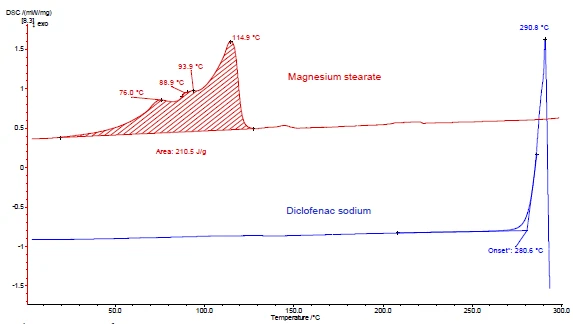
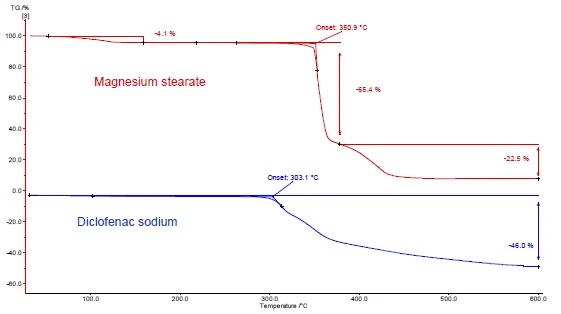
Şekil 4 ve 5, diklofenak sodyum ve magnezyum stearat örneğinde nasıl ilerleneceğini göstermektedir. DSC ve TGA ölçümleri gerçekleştirilmiştir. Şekil 4a ve 5a, ısıtma sırasında iki maddenin sırasıyla DSC ve TGA eğrilerini göstermektedir.
Magnezyum stearatın DSC eğrisinde tespit edilen oda sıcaklığı ile 130°C arasındaki endotermal pik (şekil 4a, kırmızı eğri, üstte) kısmen suyun buharlaşmasından kaynaklanmaktadır. Bu sıcaklık aralığı için TGA eğrisinde bir kütle kaybına (%4,1) karşılık gelir. Su salınımı piki magnezyum stearatın erimesi ile örtüşmektedir [9].
Diklofenak sodyum (Şekil 4a, mavi eğri, aşağıda) 291°C'de erimeye karşılık gelen bir endotermal pik gösterir. Erimenin hemen ardından gelen EkzotermikBir örnek geçişi veya bir reaksiyon ısı üretiyorsa ekzotermiktir.ekzotermik bir süreç %46'lık bir kütle kaybıyla ilişkilidir ve diklofenakın ayrışmasından kaynaklanır.

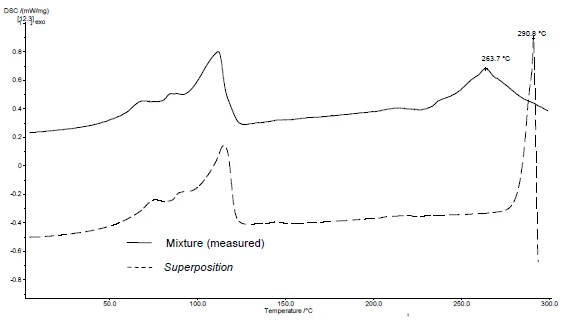

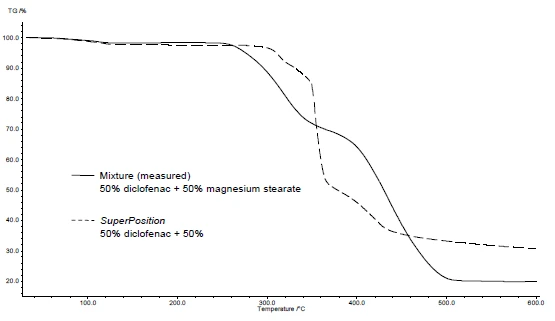
SuperPosition uygulaması (şekil 4b, 5b), karışımın ölçülen eğrisinin, etkileşim olmaması durumunda elde edilecek hesaplanan eğri ile karşılaştırılmasına olanak tanır. İki eğri arasında fark olmaması uyumlu bir karışım olduğunu gösterir.
Bu örnekte, karışımın ayrışması 278°C'de, yani tek başına yardımcı maddeye göre daha düşük bir sıcaklıkta başlar (Şekil 5c). Diklofenak için tipik olanErime Sıcaklıkları ve EntalpileriGizli ısı olarak da bilinen bir maddenin füzyon entalpisi, bir maddeyi katı halden sıvı hale dönüştürmek için gerekli olan enerji girdisinin, tipik olarak ısının bir ölçüsüdür. Bir maddenin erime noktası, katı (kristal) halden sıvı (izotropik eriyik) hale geçtiği sıcaklıktır. erime piki artık karışımda sergilenmemektedir. Bunun yerine 264°C'de geniş bir endotermal pik tespit edilmiştir (şekil 4c).
Örnekte tespit edilen farklılıklar, diklofenak sodyum ile magnezyum stearat arasında bir etkileşim olduğunu göstermektedir (şekil 4c ve 5c).
Diklofenak sodyum ile farklı yardımcı maddeler arasında DSC ve TGA kullanılarak yapılan uyumluluk çalışmasının bir başka örneği NETZSCH Uygulama Notu 120'de verilmiştir [4].
3. Polimorfizm
PolimorfizmPolimorfizm, katı bir maddenin farklı kristal yapılar oluşturma yeteneğidir (eşanlamlılar: formlar, modifikasyonlar).Polimorfizm, bir maddenin birden fazla kristal formda bulunabilme yeteneğidir. Bir farmasötik maddenin farklı polimorfik formları genellikle α, β, ... veya I, II, ... veya A, B, ... olarak adlandırılır; burada α/I/A modifikasyonu en kararlı olanıdır.
İlaç endüstrisinde PolimorfizmPolimorfizm, katı bir maddenin farklı kristal yapılar oluşturma yeteneğidir (eşanlamlılar: formlar, modifikasyonlar).polimorfizm çok zorlayıcıdır çünkü iki polimorfik madde aynı kimyasal bileşime sahip olsalar bile özellikleri bakımından farklılık gösterirler. Polimorfik bir madde zaman içinde yapısını değiştirebildiğinden, depolama sırasında biyo-yararlanımında, fiziksel özelliklerinde, stabilitesinde vb. beklenmedik değişiklikler meydana gelebilir. Bu nedenle ve patent tescili ile ilgili olarak, bir polimorfik maddenin tüm potansiyel modifikasyonlarının varlığının ve her birinin özelliklerinin, stabilitesinin ve kalitesinin farkında olmak ve bunlar hakkında bilgi sahibi olmak çok önemlidir.
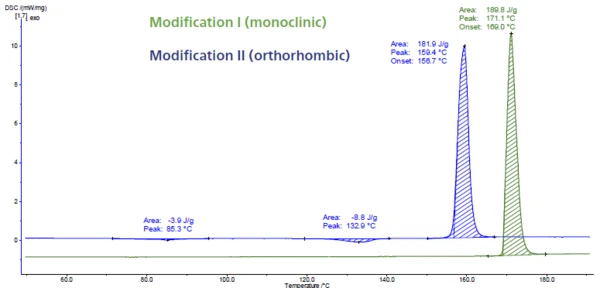
Şekil 6, parasetamol üzerindeki DSC ölçümünü göstermektedir. Bu API (Aktif İlaç Hammaddesi) I, II ve III olarak adlandırılan üç modifikasyona sahiptir. Modifikasyon III kararsızdır ve bu nedenle karakterize edilmesi zordur. I ve II modifikasyonları termodinamik kararlılıkları ve sıkıştırma yetenekleri bakımından farklılık gösterir. Erime sıcaklığı farklı sıcaklıklarda tespit edildiği için DSC aracılığıyla kolayca tanımlanabilirler. 169°C'dekiErime Sıcaklıkları ve EntalpileriGizli ısı olarak da bilinen bir maddenin füzyon entalpisi, bir maddeyi katı halden sıvı hale dönüştürmek için gerekli olan enerji girdisinin, tipik olarak ısının bir ölçüsüdür. Bir maddenin erime noktası, katı (kristal) halden sıvı (izotropik eriyik) hale geçtiği sıcaklıktır. erime zirvesi (ekstrapole edilmiş başlangıç sıcaklığı, yeşil eğri) monoklinik form için tipiktir. En yüksek Erime Sıcaklıkları ve EntalpileriGizli ısı olarak da bilinen bir maddenin füzyon entalpisi, bir maddeyi katı halden sıvı hale dönüştürmek için gerekli olan enerji girdisinin, tipik olarak ısının bir ölçüsüdür. Bir maddenin erime noktası, katı (kristal) halden sıvı (izotropik eriyik) hale geçtiği sıcaklıktır.erime noktasına sahip ve aynı zamanda en kararlı olan modifikasyondur. 157°C'deki pik (ekstrapole edilmiş başlangıç sıcaklığı, mavi eğri) daha iyi sıkıştırma özelliklerine sahip olan ortorombik forma aittir [5, 6].
Form II, sıkıştırılabilirliği artırmak için bir yardımcı madde eklenmeden doğrudan sıkıştırılabilmesine rağmen, ticari parasetamol daha iyi stabilitesi nedeniyle monoklinik formdan (form I) üretilmektedir [7, 8].
Polimorfik bir maddenin farklı modifikasyonlarının karakterizasyonuna ilişkin diğer örnekler NETZSCH Uygulama Notu 127'de verilmiştir [10].
4. Sözde Polimorfizm
İki sözde polimorfik modifikasyon, hidrasyon veya solvasyondan kaynaklanan farklı kristal formlarına sahiptir.
Bir solvatta, çözücü molekülleri maddenin kristal yapısına hapsolmuştur. Eğer bu ikiden fazla çözücü içeriyorsa, hetero-solvat olarak adlandırılır.
Bir hidratta, ilaçla birlikte bulunan çözücü sudur.
Solvatların ve hidratların karakterizasyonu, muhtemelen evrimleşmiş gaz analizi ile birlikte termogravimetri ile gerçekleştirilir. Bir TGA ölçümü, bir numunede bulunan çözücü/su miktarı ve dolayısıyla solvasyon/hidrasyon derecesi hakkında bilgi verir. Birleştirme, ısıtma sırasında açığa çıkan çözücülerin tanımlanmasını sağlar.
Sonuç
Termal analiz, özellikle DSC ve TGA aracılığıyla, API ve eksipiyanların farklı özellikleri araştırılabilir. Bu da farmasötiklerin termal stabilitesinin, uyumluluğunun, polimorfizminin ve yalancı polimorfizminin belirlenmesini sağlar.