Wprowadzenie
Stabilność API (aktywnych składników farmaceutycznych) i substancji pomocniczych jest bezpośrednio związana z warunkami ich przechowywania: Przechowywanie w niewłaściwej temperaturze (zbyt ciepłej lub zbyt zimnej) może wpływać na ich skuteczność, bezpieczeństwo i okres przydatności do użycia. Testy stabilności przechowywania farmaceutyków opisane w wytycznych WHO (Światowej Organizacji Zdrowia) i ICH (Międzynarodowej Rady Harmonizacji Wymagań Technicznych dla Stosowania u Ludzi) wymagają co najmniej 6 miesięcy. [1, 2]
Wstępne informacje na temat stabilności substancji w określonych warunkach temperaturowych można uzyskać w ciągu pierwszych kilku godzin. W tym celu kinetyka procesu degradacji substancji (rozkład termiczny, desolwatacja, odwodnienie) jest oceniana i wykorzystywana do określenia jej zachowania podczas długotrwałych izoterm. Pozwala to na szybkie przeprowadzenie wstępnego sortowania API / substancji pomocniczych.
Poniżej przedstawiono kinetykę reakcji odwodnienia dla dwuwodnego wodorofosforanu wapnia, CaHPO4-2H2O(zwanego również DCP). W tym celu pomiary termograwimetryczne przeprowadzone przy różnych szybkościach ogrzewania są wykorzystywane do oceny kinetyki reakcji za pomocą oprogramowania NETZSCH Kinetics Neo.
Warunki pomiaru
DCP jest wypełniaczem powszechnie stosowanym do tabletkowania. Substancja użyta do pomiarów została uprzejmie dostarczona przez JRS Pharma (nazwa handlowa: Emcompress®). Warunki eksperymentalne podsumowano w tabeli 1.
Tabela 1: Warunki testowe
Urządzenie | TG 209 F1 Nevio sprzężone ze spektrometrem FT-IR od Bruker Optics (PERSEUS® sprzężenie) | TG 209 F1 Nevio |
|---|---|---|
| Próbka | DCP Emcompress® (JRS Pharma) | |
| Masa próbki | 3.71 mg | 3.71 mg do 4,30 mg |
| Tygiel | Zamknięty Concavus® (Al) z przebitą pokrywką | |
| Program temperatury | 30°C do 300°C | |
| Szybkość ogrzewania | 10 K/min | 1 K/min do 20 K/min |

Wyniki pomiarów
Pomiar TGA-FT-IR na DCP
Rysunek 1 przedstawia krzywą ubytku masy (zielona) i wykres Grama Schmidta (czarny) uzyskane w wyniku pomiaru TGA-FTIR na DCP. Krzywa Grama Schmidta wskazuje zakresy temperatur, w których wykryto uwolnione gazy. Między temperaturą pokojową a 300°C widoczne są trzy stopnie utraty masy, odpowiadające trzem maksimom na wykresie Grama-Schmidta. Zmierzona masa resztkowa wynosząca 79% odpowiada teoretycznej masie resztkowej po utracie 2H2Oz DCP.
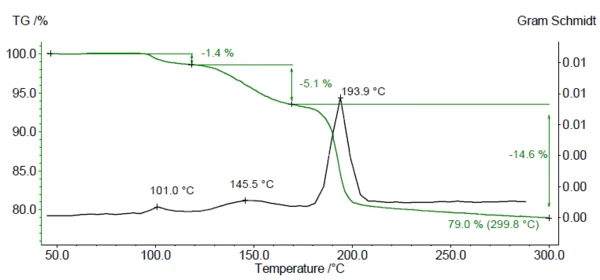
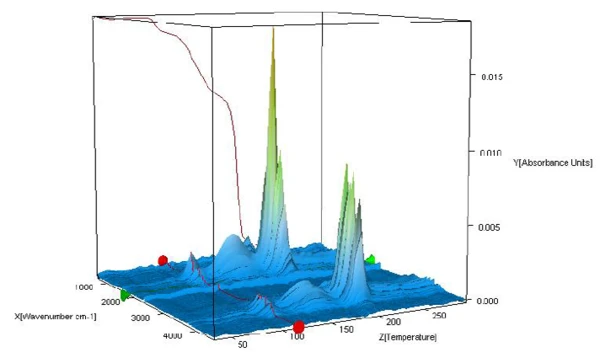
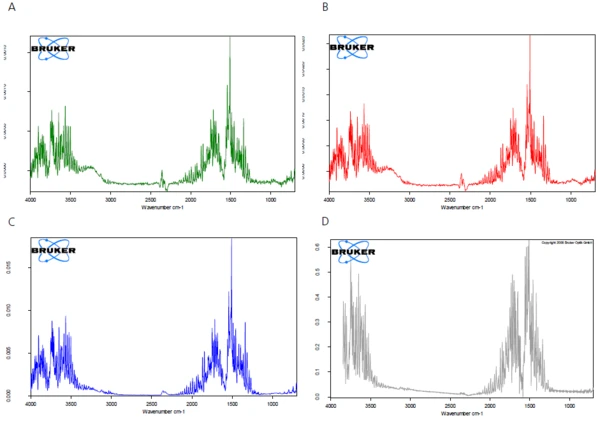
Widma FT-IR produktów uwalnianych podczas ogrzewania są analizowane w celu sprawdzenia, czy w tym zakresie temperatur uwalniana jest tylko woda, czy także inne składniki. Rysunek 2 przedstawia widma FT-IR substancji uwolnionych podczas pomiaru w widoku trójwymiarowym. Ekstrakcja widm w różnych temperaturach pokazuje, że wykryte etapy utraty masy są spowodowane jedynie wydzielaniem się wody (patrz rysunki 3A, 3B i 3C, widma FT-IR substancji uwolnionych w temperaturach 110°C, 159°C i 205°C oraz 3D, widmo porównawcze wody z EPA-NIST library).
Z literatury [4] wiadomo, że woda powierzchniowa i woda strukturalna zaczynają opuszczać strukturę krystaliczną około 80°C, w którym to momencie zaczyna tworzyć się faza amorficzna. Ilość substancji w fazie amorficznej wzrasta podczas rozkładu do 200-220°C i zmienia się wraz z szybkością ogrzewania.
Analiza kinetyki procesu odwadniania
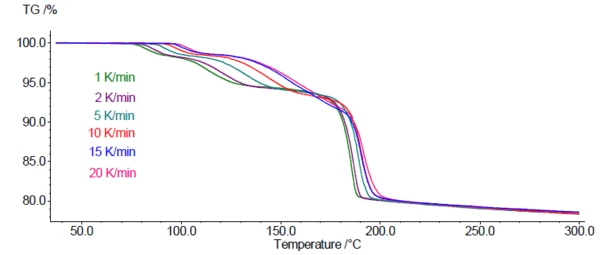
Rysunek 4 przedstawia krzywe pomiarowe TGA dla DCP przy 6 różnych szybkościach ogrzewania w zakresie od 1 do 20 K/min. Zgodnie z oczekiwaniami dla tego procesu kinetycznego, etapy utraty masy przesuwają się do wyższych temperatur wraz ze wzrostem szybkości ogrzewania.
Ta zależność etapów utraty masy od szybkości ogrzewania pozwala na wykorzystanie krzywych TGA do analizy kinetyki odwodnienia. W tym celu wykorzystano oprogramowanie Kinetics Neo ( NETZSCH-Gerätebau GmbH). Może ono przypisać każdemu etapowi różne typy reakcji z własnymi parametrami kinetycznymi, takimi jak energia aktywacji, kolejność reakcji i współczynnik przedwykładniczy. W oparciu o wyniki, Kinetics Neo jest w stanie symulować reakcję (reakcje) dla programów temperaturowych określonych przez użytkownika, np. długotrwałych izoterm w określonej temperaturze.
Poniższe obserwacje pomagają określić liczbę i rodzaj etapów kinetyki.
- Obecność trzech etapów utraty masy sugeruje, że proces przebiega w co najmniej trzech etapach.
- Fakt, że krzywe przy niskiej szybkości ogrzewania przecinają się z krzywymi przy wysokiej szybkości ogrzewania (patrz zakres temperatur 150°C-190°C) wskazuje, że etap reakcji powinien być opisany przez model reakcji konkurencyjnej lub równoległej.
- Po trzecim etapie utraty masy masa nadal maleje; można to opisać dodatkowym etapem w modelu kinetyki.
Ostatecznie uznano, że następujący model najlepiej opisuje ten proces:
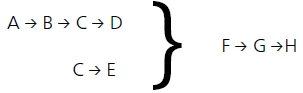
- Etap reakcji A → B opisuje pierwszy etap utraty masy na krzywej TGA i pochodzi z uwolnienia wody powierzchniowej.
Etapy reakcji
B → C → D
C → E
mogą odpowiadać etapom opisanym przez Rabatina i in. [3]:
CaHPO4 - 2H2O→ CaHPO4- xH2O+ (2-x)H2O(I)
H2O(I) →H2O(g)
co prowadzi do powstawania różnych stechiometrycznych ilości wody z CaHPO4 -H2O[produkt D] i CaHPO4 - yH2O[produkt E].
Dodatkowo rozpoczęło się tworzenie fazy amorficznej, które zależy od szybkości ogrzewania. Im niższa szybkość ogrzewania, tym dłuższy czas trwania fazy amorficznej. Różne czasy trwania fazy amorficznej wynikające z różnych szybkości ogrzewania mogą być odpowiedzialne za różne wartości TGA po drugim etapie rozkładu w temperaturze 180°C i odpowiedzialne zaReakcja rozkładuReakcja rozkładu to wywołana termicznie reakcja związku chemicznego tworząca produkty stałe i/lub gazowe. rozkład na równoległe sposoby. W Kinetics Neo produkty D i E są opisane za pomocą F (F = D + E). - Temperatura detekcji trzeciego etapu utraty masy jest zgodna z pomiarem DTA opisanym przez Rabatin et al. [3], w którym wykryto pik w 195°C. Autorzy powiązali ten pik z następującym mechanizmem: CaHPO4- xH2O→ CaHPO4 (amorficzny) + xH2O
To z kolei korelowało z etapem F → G z Kinetics Neo. - Etap reakcji G → H opisuje ciągły spadek masy powyżej 200°C.
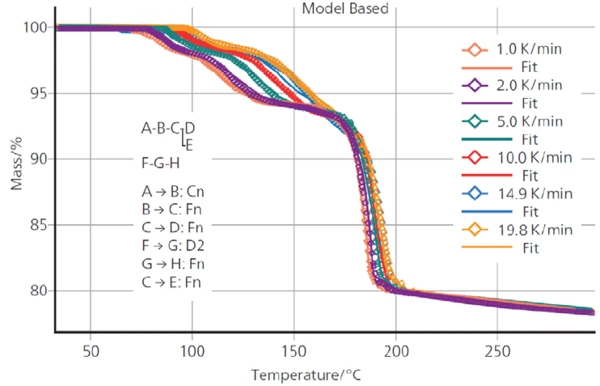
Rysunek 5 pokazuje dobre dopasowanie zmierzonych krzywych TGA do krzywych obliczonych przez Kinetics Neo przy użyciu opisanego modelu kinetyki. Współczynnik korelacji pomiędzy zmierzonymi i obliczonymi krzywymi wynosi 0,999.
Parametry każdego etapu reakcji obliczone przez Kinetics Neo podsumowano w tabeli 2.
Tabela 2: Parametry kinetyczne etapów reakcji
| Etap reakcji | A → B | B → C | C → D | D → E | F (D+E) → G | G → H |
| Typ reakcji | n-tego rzędu z autokataliza | n-ty rząd | n-ty rząd | n-ty rząd | dyfuzja | n-ty rząd |
| Energia aktywacji [kJ-mol-1] | 144.8 | 104.2 | 111.3 | 50.7 | 611.9 | 19.9 |
| Log (współczynnik przedwykładniczy) | 17.9 | 11.5 | 11.9 | 0.5 | 67.2 | 4.1 |
| Kolejność reakcji | 1.59 | 0.43 | 0.91 | 0.01 | - | 3.17 |
| Wkład | 0.063 | 0.067 | 0.150 | 0.235 | 0.495 | 0.182 |
Od oceny kinetyki do przewidywania zachowania próbki
Znajomość kinetyki reakcji pozwala na symulację procesu odwodnienia dla dowolnego programu temperatury selected, w tym izotermy długoterminowej.
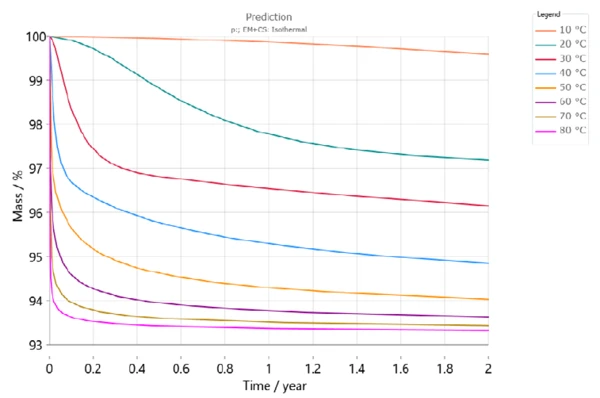
Rysunek 6 przedstawia odwodnienie DCP w ciągu dwóch lat dla różnych temperatur przechowywania. Zgodnie z tą symulacją, utrata masy wyniesie ponad 3% po 6 miesiącach w temperaturze przechowywania 30°C (czerwona krzywa). Jednak w temperaturze 50°C utrata masy wyniesie już ponad 5% w tym samym okresie (kolor jasnopomarańczowy).
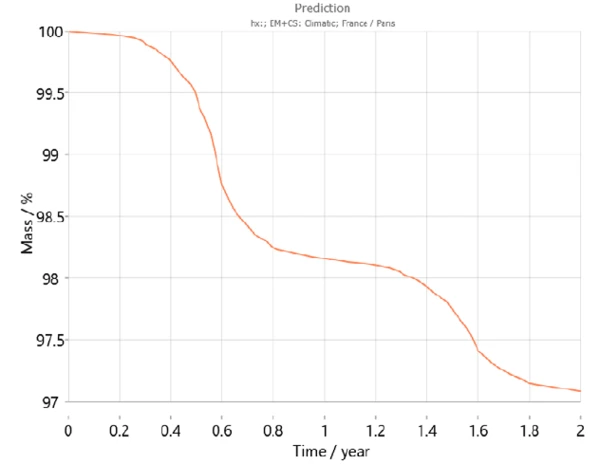
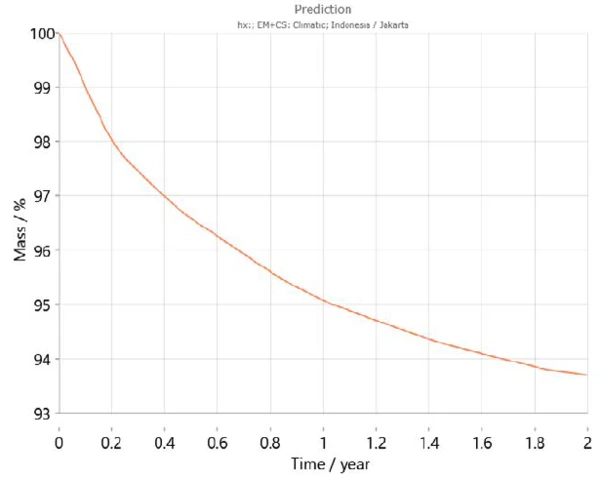
Dodatkowo, Kinetics Neo zawiera mapę klimatyczną uwzględniającą wzorce średniej temperatury w ciągu ostatnich lat dla różnych regionów świata, w tym wahania temperatury w ciągu roku. Korzystając z tych informacji, Kinetics Neo jest w stanie dostosować swoje przewidywania dotyczące zachowania próbki dla danego kraju. Na przykład rysunki 7 i 8 przedstawiają krzywe przewidywania dla dwuwodnego fosforanu wapnia w ciągu dwóch lat odpowiednio w Paryżu (Francja) i Dżakarcie (Indonezja). Zgodnie z oczekiwaniami, zachowanie próbki różni się znacznie między tymi dwoma miastami. Odwodnienie przebiega szybciej w Dżakarcie ze względu na wyższe temperatury niż w Paryżu.
Wnioski
Połączenie termograwimetrii i kinetyki Neo jest potężnym narzędziem do uzyskiwania wstępnych informacji na temat stabilności substancji w określonych temperaturach przechowywania.
Może być stosowany do badań przesiewowych API (aktywnych składników farmaceutycznych) i zaróbek podczas opracowywania nowego produktu farmaceutycznego w celu uzyskania wstępnychselectjonów do badań stabilności o dłuższym czasie trwania.