Wprowadzenie
Liofilizacja to technika szeroko stosowana w technologiach farmaceutycznych do przekształcania substancji termolabilnych, takich jak białka lub liposomy - bez obróbki termicznej - w formy nadające się do użytku i przechowywania. Celem liofilizacji jest delikatne usunięcie wody z roztworów w celu uzyskania stabilnego proszku o określonej wilgotności resztkowej i porowatości.
Skład produktu ma decydujący wpływ na parametry procesu, a tym samym na rodzaj, jakość i stabilność otrzymanego liofilizatu. Dynamiczna kalorymetria skaningowa (DSC) dostarcza ważnych informacji dla selectjon odpowiednich warunków.
Roztwory przeznaczone do liofilizacji są zazwyczaj złożonymi, wieloskładnikowymi systemami składającymi się ze składników aktywnych, dodatków i wody. Substancje pomocnicze obejmują sole tonizujące (do regulacji izotoniczności), substancje buforowe, krioprotektory (do ochrony przed uszkodzeniem podczas zamrażania) i substancje budujące, które nadają strukturę liofilizowanemu produktowi. Cukry takie jak sacharoza lub trehaloza okazały się bardzo skuteczne w stabilizacji białek [5]. Poniższe rozważania opierają się na sacharozie jako substancji modelowej. Wspomniane roztwory zostały wyprodukowane z dostępnej w handlu sacharozy o jakości farmaceutycznej (Caesar & Loretz, Hilden) i wody podwójnie destylowanej.
Proces liofilizacji można ogólnie podzielić na 3 kolejne etapy:
Głębokie mrożenie
Roztwory cukru mają tendencję do przesycania. Po schłodzeniu powstaje lód i coraz bardziej lepki roztwór sacharozy. Rosnąca lepkość komplikuje procesy dyfuzji, które byłyby niezbędne do krystalizacji. W rezultacie układ nie krystalizuje, ale krzepnie jako niedostatecznie schłodzona ciecz bez całkowitego rozdzielenia faz (szkło). Temperatura zeszkleniaPrzejście szkliste jest jedną z najważniejszych właściwości materiałów amorficznych i półkrystalicznych, np. szkieł nieorganicznych, metali amorficznych, polimerów, farmaceutyków i składników żywności itp. i opisuje obszar temperatury, w którym właściwości mechaniczne materiałów zmieniają się z twardych i kruchych na bardziej miękkie, odkształcalne lub gumowate.Temperatura zeszklenia maksymalnie stężonego roztworu jest określana jako Tg' i jest zależna od substancji [3].
Podczas chłodzenia często można zaobserwować przechłodzenie. Roztwory farmaceutyczne do stosowania pozajelitowego (podawanie z pominięciem przewodu pokarmowego), które muszą być wolne od cząstek, stanowią skrajny przypadek. Nie zawierają one praktycznie żadnych heterogenicznych zanieczyszczeń, które mogłyby działać jako jądra krystalizacji. Dlatego zarodkowanie kryształów w takich roztworach jest często prawdopodobne tylko wtedy, gdy temperatura zbliża się do -40°C.
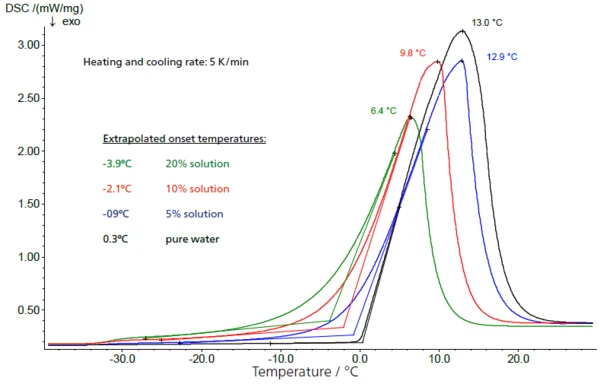
Zachowanie zamrażania 10% roztworu sacharozy pokazano na rysunku 2. Próbka została schłodzona za pomocą urządzenia NETZSCH DSC 204 F1 (patrz rysunek 1) w zamkniętym aluminiowym tyglu z kontrolowaną szybkością chłodzenia 5 K/min. Przechłodzony roztwór zestala się bardzo szybko w temperaturze -20°C (ekstrapolowana temperatura początkowa).

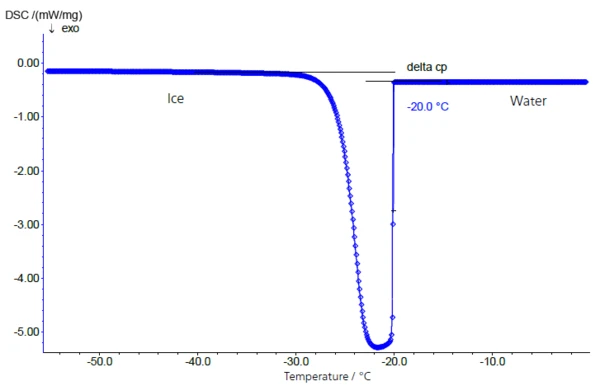
Szorstki spots wewnątrz tygla lub ślady zanieczyszczeń spowodowanych przygotowaniem mogą służyć jako kryształy zalążkowe. Z tego powodu temperatury krzepnięcia określone w ten sposób nie mogą być skorelowane ze stężeniem użytych roztworów cukru.
Podczas przejścia z wody do lodu następuje zmiana ciepła właściwego z 4,18 J/g-K (woda) do 2,1 J/g-K (lód, tuż poniżej punktu zamarzania), co jest przede wszystkim odpowiedzialne za wyraźne przesunięcie linii bazowej przed i po piku krzepnięcia/topnienia (rys. 2: przejście z wody do lodu - i rys. 3: przejście z lodu do wody).
Podczas późniejszego ogrzewania z szybkością 5 K/min (rysunek 3), Temperatura zeszkleniaPrzejście szkliste jest jedną z najważniejszych właściwości materiałów amorficznych i półkrystalicznych, np. szkieł nieorganicznych, metali amorficznych, polimerów, farmaceutyków i składników żywności itp. i opisuje obszar temperatury, w którym właściwości mechaniczne materiałów zmieniają się z twardych i kruchych na bardziej miękkie, odkształcalne lub gumowate.przejście szkliste maksymalnie stężonego roztworu pojawia się w temperaturze -32°C (punkt środkowy). Wartość ta jest zgodna z danymi literaturowymi zakładającymi -32°C i -33°C [2], [4].
Po przejściu szklistym następuje pik EndotermicznyPrzemiana próbki lub reakcja jest endotermiczna, jeśli do konwersji potrzebne jest ciepło.endotermiczny podczas ogrzewania (wstawka na rysunku 3), którego ekstrapolowana temperatura początkowa, Tm´, opisuje początek topnienia lodu. Według Roos [1], maksymalne "stężenie zamarzania" można zaobserwować tylko w temperaturach zamarzania pomiędzy Tg´i Tm´.
Obszar poniżej piku topnienia odpowiada części wolnej wody. Punktem odniesienia jest tutaj ciepło topnienia lodu wynoszące 333,7 J/g.
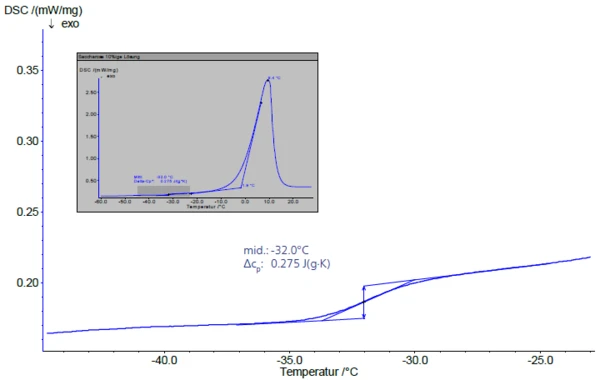
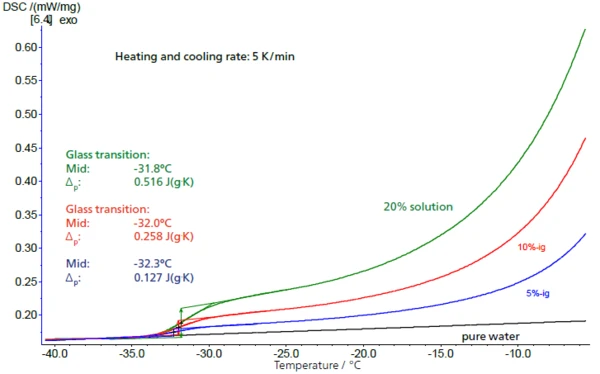
W roztworach o niskim stężeniu udział sacharozy można określić na podstawie wysokości odpowiedniego przejścia szklistego. Na rysunku 4 wysokości stopni (wartości ΔPojemność cieplna właściwa (cp)Pojemność cieplna jest wielkością fizyczną specyficzną dla materiału, określoną przez ilość ciepła dostarczonego do próbki, podzieloną przez wynikający z tego wzrost temperatury. Pojemność cieplna właściwa jest związana z jednostką masy próbki.cp) dla roztworów 5%, 10% i 20% - z wynikami 0,127 J/g-K, 0,258 J/g-K i 0,516 J/g-K - są w bardzo dobrej zgodności ze skalowaniem stężenia o współczynnik 2, podczas gdy temperatury zeszklenia pozostają largely stałe. Istnieje liniowa zależność między wysokością stopnia a stężeniem (rys. 5).
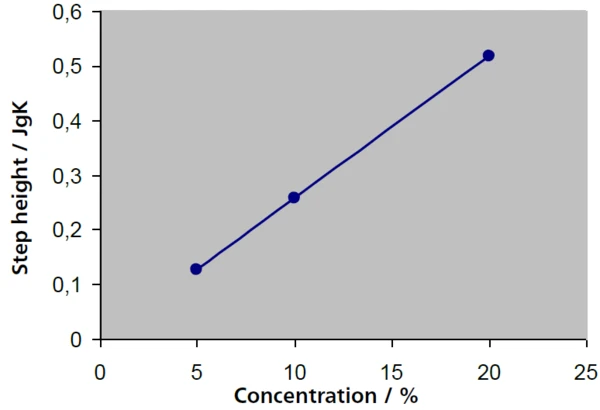
Dodatkowo, wraz ze wzrostem stężenia roztworów sacharozy, początek topnienia lodu (ekstrapolowana temperatura początku) przesuwa się do niższych wartości na rysunku 6. Przy wyższych stężeniach skutkuje to mniejszym odstępem między przejściem szklistym maksymalnie stężonego roztworu a początkiem topnienia wolnej wody.
Niektóre substancje amorficzne ponownie krystalizują po podgrzaniu powyżej temperatury zeszklenia. Efekt ten, zwany dewitryfikacją lub zimną krystalizacją, można wykorzystać do zmiany porowatości i wilgotności resztkowej liofilizatu [2] poprzez odpuszczanie materiału powyżej temperatury rekrystalizacji (ekstrapolowany początek). W wyniku rekrystalizacji następuje rozdzielenie faz, a uwolniona "niezamrożona" woda zamienia się w lód. Jak pokazano na rysunku 3, w przypadku sacharozy nie zachodzi Po krystalizacji (zimna krystalizacja)Postkrystalizacja półkrystalicznych tworzyw sztucznych zachodzi głównie w podwyższonych temperaturach i zwiększonej ruchliwości molekularnej powyżej przejścia szklistego.postkrystalizacja.
Suszenie podstawowe
Na tym etapie zamrożony lód jest usuwany w próżni poprzez sublimację (przejście ze stanu stałego do stanu skupienia gazowego).
Podczas tego procesu - w którym ciepło jest dostarczane z zewnątrz - temperatura w produkcie nie powinna wzrosnąć powyżej temperatury zeszklenia, ponieważ prowadzi to do zmiękczenia struktury szkieletu i zapadnięcia się układu [5]. Zniszczenie struktury szkieletowej podczas fazy suszenia nazywane jest kolapsem.
Chociaż zgłaszane są temperatury zapadania się, które są średnio o 1 do 5 K wyższe niż odpowiadające im temperatury zeszklenia [6], temperatury zeszklenia maksymalnie stężonych roztworów, Tg´, które można określić za pomocą DSC, są dobrymi punktami odniesienia dla ich położenia.
Suszenie wtórne
Na tym etapie produkt jest suszony do pożądanego końcowego poziomu wilgotności poprzez desorpcję wody zawartej w matrycy poprzez powolny wzrost temperatury.
W amorficznych liofilizatach woda musi dyfundować z fazy szklistej na powierzchnię. Ten dość powolny proces jest powodem, dla którego etap po suszeniu jest często tym, który określa szybkość liofilizacji amorficznych liofilizatów [2].
Ze względu na efekt zmiękczający wody, Temperatura zeszkleniaPrzejście szkliste jest jedną z najważniejszych właściwości materiałów amorficznych i półkrystalicznych, np. szkieł nieorganicznych, metali amorficznych, polimerów, farmaceutyków i składników żywności itp. i opisuje obszar temperatury, w którym właściwości mechaniczne materiałów zmieniają się z twardych i kruchych na bardziej miękkie, odkształcalne lub gumowate.temperatura zeszklenia fazy amorficznej jest bezpośrednio związana z zawartością uwięzionej wody. W miarę postępu odwadniania, Tg (Temperatura zeszkleniaPrzejście szkliste jest jedną z najważniejszych właściwości materiałów amorficznych i półkrystalicznych, np. szkieł nieorganicznych, metali amorficznych, polimerów, farmaceutyków i składników żywności itp. i opisuje obszar temperatury, w którym właściwości mechaniczne materiałów zmieniają się z twardych i kruchych na bardziej miękkie, odkształcalne lub gumowate.przejście szkliste sacharozy jako ciała stałego) wzrasta; jego położenie można również szybko i precyzyjnie określić za pomocą DSC.
Wnioski
Zasadniczymi parametrami przy projektowaniu procesu suszenia pierwotnego są Temperatura zeszkleniaPrzejście szkliste jest jedną z najważniejszych właściwości materiałów amorficznych i półkrystalicznych, np. szkieł nieorganicznych, metali amorficznych, polimerów, farmaceutyków i składników żywności itp. i opisuje obszar temperatury, w którym właściwości mechaniczne materiałów zmieniają się z twardych i kruchych na bardziej miękkie, odkształcalne lub gumowate.temperatura zeszklenia maksymalnie stężonego roztworu (Tg´) oraz temperatura kolapsu, w której materiał mięknie tak, że nie może już utrzymać własnej struktury i zaczyna płynąć. Za pomocą DSC (czasami jako TM-DSC*) można łatwo określić Tg´.
Temperatura zapadania się jest nieco wyższa niż Tg´; dokładny przedział między Tg´a temperaturą zapadania się zależy od składu.