POLIMER
Resin Epoksi - Pengawetan, Kontrol Difusi Parsial
Kecepatan reaksi kimia, yang dikontribusikan oleh lebih dari satu reaktan dikontrol oleh dua langkah:
1. kecepatan difusi reaktan bersama-sama (ditandai dengan Kdiff),
2. kecepatan reaksi kimia (ditandai dengan Kchem).
Kecepatan reaksi efektif adalah nilai rata-rata geometris dari kedua konstanta kecepatan:
1/Keff= 1/Kdiff + 1/Kchem (persamaan Rabinowitch).
Jelas bahwa Keff sama dengan Kchem, jika Kdiff >> Kchem benar.
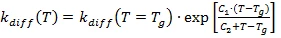
Oleh karena itu, untuk sebagian besar, efek kontrol difusi tidak diperhitungkan. Jika suhu reaksi mendekati atau lebih kecil dari suhu transisi gelas, maka peningkatan viskositas yang kuat akan teramati: bahan yang sedang diselidiki mengalami vitrifikasi. Melalui mobilitas reaktan yang terbatas, proses Pengawetan (Reaksi Pengikatan Silang)Secara harfiah diterjemahkan, istilah "crosslinking" berarti "jaringan silang". Dalam konteks kimia, istilah ini digunakan untuk reaksi di mana molekul dihubungkan bersama dengan memperkenalkan ikatan kovalen dan membentuk jaringan tiga dimensi. pengawetan dikontrol oleh difusi dan Kchem >> Kdiff adalah benar.
Semua perhitungan, pemodelan, kecocokan, dan prediksi untuk aplikasi ini dibuat dalam perangkat lunak NETZSCH Kinetika Neo.
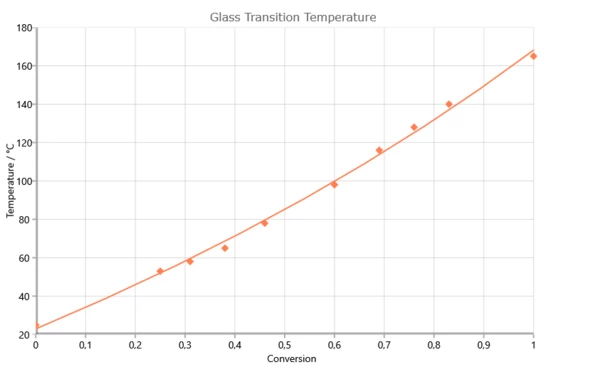
Gambar 1. Ketergantungan suhu transisi gelas pada derajat reaksi untuk sistem 2,2¥,6,6¥-tetrabrom-bisphenol-A-diglikidileter (RUETAPOX VE 3579) + 5% Zn(OCN)2 [Flammersheim, Opfermann: Thermochim. Acta 337 (1999) 141]
Ketergantungan suhu dari Kchem dihitung dengan persamaan Arrhenius. Karena Kdiff berbanding terbalik dengan viskositas, maka ketergantungannya pada suhu digunakan. Jika (a) dasar analisisnya adalah pengukuran DSC, maka suhu transisi gelas dan ketergantungannya pada derajat reaksi digunakan sebagai nilai pengendali viskositas. Menurut proposal khusus, yang diberikan oleh Wise [C.W.Wise, W.D.Cook, A.A.Goodwin: Polymer 38 (1997) 3251], kecepatan difusi dihitung dengan menggunakan persamaan Williams-Landel-Ferry (WLF) yang dimodifikasi
Untuk suhu T yang lebih rendah dari Tg, persamaan WLF ditransformasikan menjadi persamaan Arrhenius dalam kedua kondisi dimana transfer dan turunan pertama bersifat kontinu. Energi aktivasi saat ini untuk T < Tg adalah:
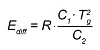
Sebaliknya, jika (b) dasar analisisnya adalah pengukuran viskositas, maka viskositas yang dihitung digunakan sebagai nilai pengendali. Sekarang viskositas dihitung dengan menggunakan persamaan Arrhenius dengan energi aktivasi yang berbeda untuk bahan yang tidak diawetkan dan diawetkan.
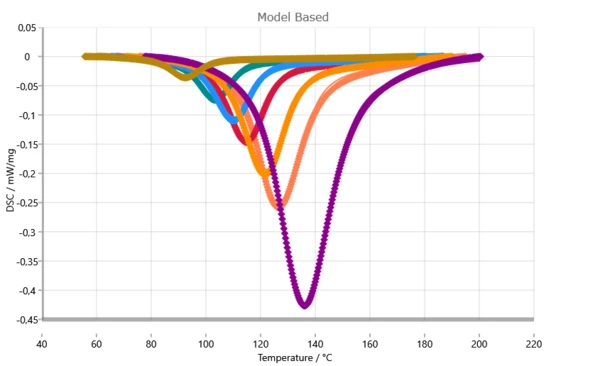
Perbandingan antara kurva DSC yang diukur (simbol) dan yang dihitung (garis padat).
Dengan mempertimbangkan kontrol difusi dalam analisis kinetik, kecocokan yang hampir sempurna dapat dicapai. Kualitas kecocokan yang tinggi ini merupakan kondisi dasar untuk prediksi dengan tingkat kepercayaan yang tinggi.
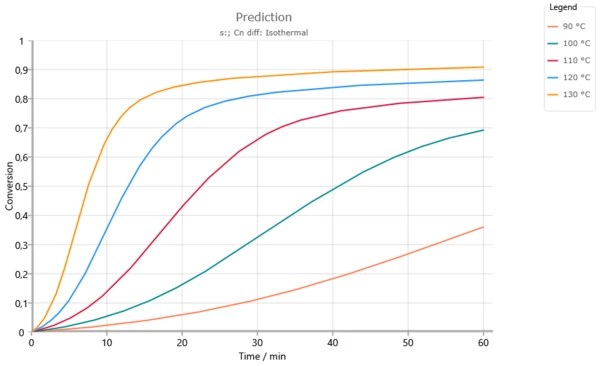
Prediksi IsotermalPengujian pada suhu yang terkendali dan konstan disebut isotermal.isotermal untuk suhu di bawah suhu transisi gelas Tg = 165°C. Peningkatan derajat kekusutan reaksi di mana suhu transisi gelas mencapai suhu reaksi (lihat gambar berikut). Tanpa menggunakan kontrol difusi di atas 120°C, konversi penuh akan tercapai setelah 60 menit.
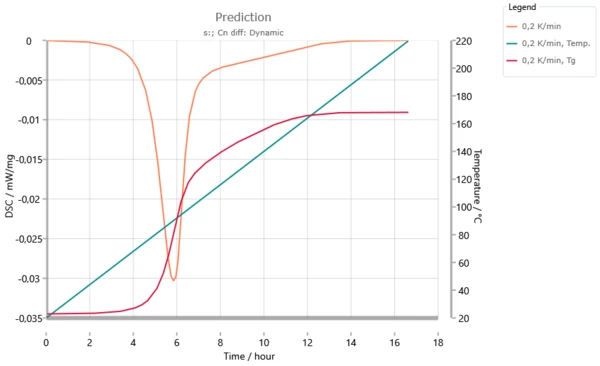
Informasi ini dapat dimengerti dengan menggunakan gambar berikut ini, simulasi untuk laju pemanasan 0,2 K/menit: suhu transisi kaca mencapai suhu reaksi setelah 6 jam. Dari sini hingga waktu reaksi 12 jam, begitu banyak yang bereaksi sehingga peningkatan suhu transisi gelas sama dengan peningkatan suhu reaksi. Dalam rentang ini, reaksi dikontrol oleh difusi.
Prediksi dinamis untuk laju pemanasan 0,2 K/menit. Suhu transisi gelas mencapai suhu reaksi setelah 6 jam. Sinyal DSC terurai kecuali untuk nilai konstan. Di atas 12 jam, suhu transisi gelas Tg meningkat lebih kecil dari suhu reaksi. Sistem menghentikan kondisi "vitrifikasi".