Polymères
Résine époxy - Durcissement, contrôle de la diffusion partielle
La vitesse d'une réaction chimique, à laquelle contribuent plusieurs réactifs, est contrôlée par deux étapes :
1. la vitesse de diffusion des réactifs entre eux (caractérisée par Kdiff),
2. la vitesse de réaction chimique (caractérisée par Kchem).
La vitesse de réaction effective est la moyenne géométrique des deux constantes de vitesse :
1/Keff = 1/Kdiff + 1/Kchem (équation de Rabinowitch).
Il est évident que Keff est égal à Kchem, si Kdiff >> Kchem est vrai.
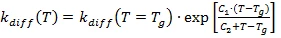
Par conséquent, la plupart du temps, l'effet du contrôle de la diffusion n'est pas pris en compte. Si la température de réaction est proche ou inférieure à la température de transition vitreuse, on observe une forte augmentation de la viscosité : le matériau étudié se vitrifie. Grâce à la mobilité restreinte des réactifs, le processus de Durcissement (réactions de réticulation)Le terme "crosslinking" signifie littéralement "mise en réseau". Dans le contexte chimique, il est utilisé pour les réactions dans lesquelles les molécules sont liées entre elles par l'introduction de liaisons covalentes et la formation de réseaux tridimensionnels.durcissement est contrôlé par la diffusion et Kchem >> Kdiff est vrai.
Tous les calculs, modélisations, ajustements et prédictions pour cette application ont été effectués dans le logiciel NETZSCH Kinetics Neo.
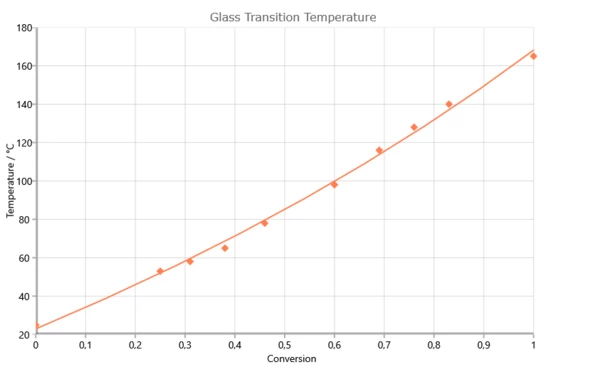
Dépendance de la température de transition vitreuse par rapport au degré de réaction pour le système 2,2¥,6,6¥-tétrabrom-bisphénol-A-diglycidyléther (RUETAPOX VE 3579) + 5% Zn(OCN)2 [Flammersheim, Opfermann : Thermochim. Acta 337(1999)141]
La dépendance de Kchem par rapport à la température est calculée par l'équation d'Arrhenius. Kdiff étant inversement proportionnel à la viscosité, sa dépendance par rapport à la température est utilisée. Si (a) la base d'analyse est constituée par des mesures DSC, la température de transition vitreuse et sa dépendance par rapport au degré de réaction sont utilisées comme valeur de contrôle de la viscosité. Selon une proposition spéciale de Wise [C.W.Wise, W.D.Cook, A.A.Goodwin : Polymer 38 (1997) 3251], la vitesse de diffusion est calculée au moyen d'une équation Williams-Landel-Ferry (WLF) modifiée
Pour les températures T inférieures à Tg, l'équation WLF est transformée en une équation d'Arrhenius, à condition que le transfert et la première dérivation soient continus. L'énergie d'activation actuelle pour T<Tg est :
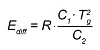
Sinon, si (b) la base de l'analyse est constituée par des mesures de viscosité, la viscosité calculée est utilisée comme valeur de contrôle. La viscosité est alors calculée au moyen d'une équation d'Arrhenius avec différentes énergies d'activation pour le matériau non polymérisé et polymérisé.
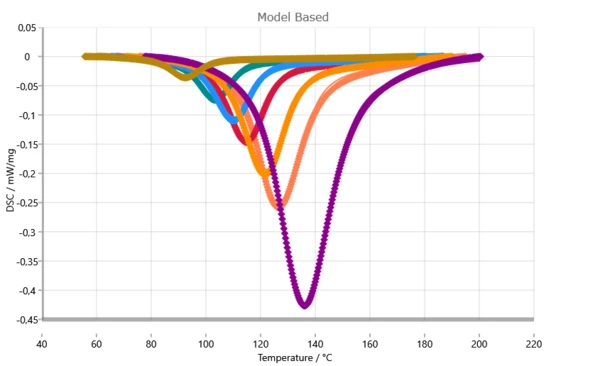
Comparaison entre les courbes DSC mesurées (symboles) et calculées (lignes pleines).
En tenant compte du contrôle de la diffusion dans l'analyse cinétique, on obtient un ajustement presque parfait. Cette qualité d'ajustement élevée est la condition de base pour des prédictions avec un niveau de confiance élevé.
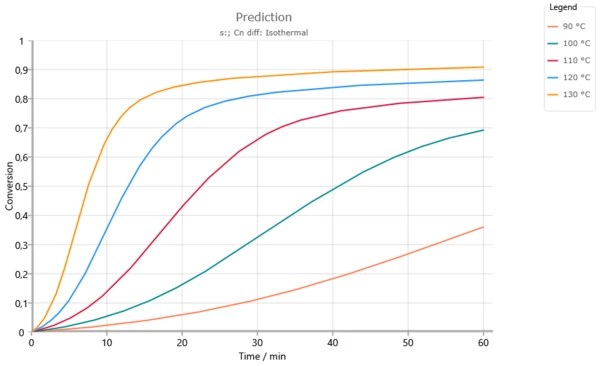
Prédictions isothermes pour des températures inférieures à la température de transition vitreuse Tg = 165°C. L'augmentation du degré de réaction s'infléchit lorsque la température de transition vitreuse atteint la température de réaction (voir l'image suivante). Sans l'utilisation d'un contrôle de la diffusion au-dessus de 120°C, la conversion totale serait déjà atteinte après 60 minutes.
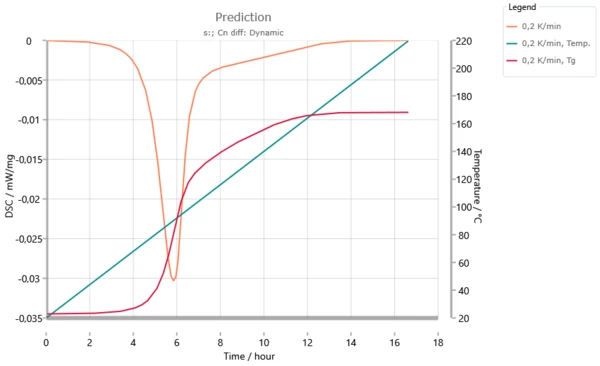
Cette information devient plus compréhensible à l'aide de l'image suivante, une simulation pour une vitesse de chauffage de 0,2 K/min : la température de transition vitreuse atteint la température de réaction après 6 heures. À partir de là et jusqu'à un temps de réaction de 12 heures, la réaction est telle que l'augmentation de la température de transition vitreuse est égale à l'augmentation de la température de réaction. Dans cette plage, la réaction est contrôlée par la diffusion.
Prévision dynamique pour une vitesse de chauffage de 0,2 K/min. La température de transition vitreuse atteint la température de réaction après 6 heures. Le signal DSC s'interrompt à l'exception d'une valeur constante. Au-delà de 12 heures, la température de transition vitreuse Tg augmente moins que la température de réaction. Le système arrête la condition de "vitrification".