Introduzione
Riscaldando i liquidi in un equilibrio termico, anche la pressione di vapore del liquido aumenta all'aumentare della velocità di riscaldamento. Il tasso di evaporazione - la velocità con cui il liquido passa alla fase gassosa - aumenta con l'aumentare della temperatura. Il tasso di perdita di massa, che consente di seguire l'evaporazione in una termobilancia, aumenta nella stessa misura. La termobilancia può funzionare a pressione normale con un flusso di gas di spurgo che elimina i gas di formazione dalla camera del campione.
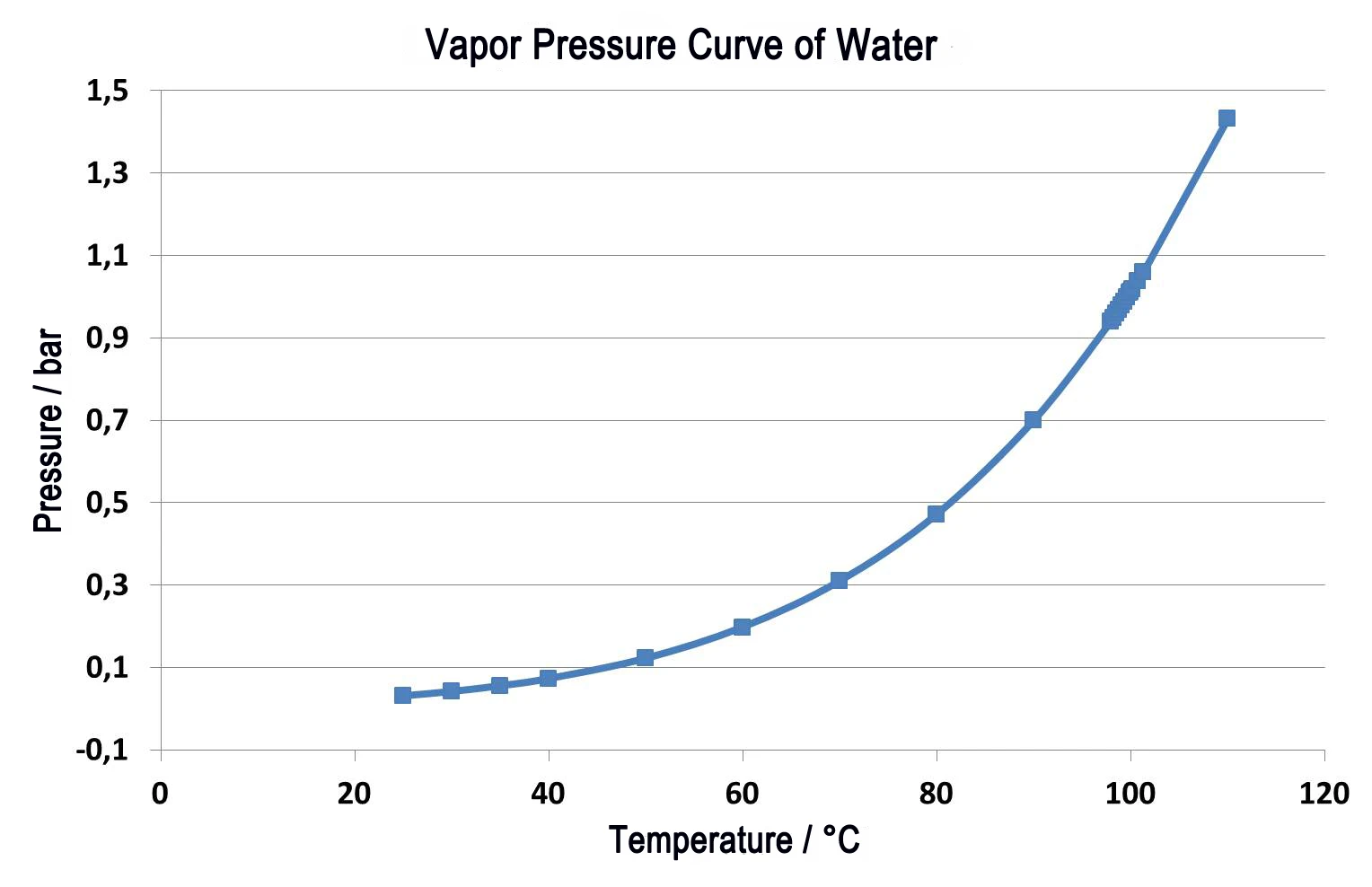
Un liquido bolle quando la pressione di vapore del liquido corrisponde alla pressione ambiente. In condizioni di pressione normale (1013 mbar), l'acqua bolle a 100°C poiché anche la pressione di vapore è pari a 1013 mbar. Se la pressione ambiente cambia, cambia anche la temperatura di ebollizione. La figura 1 presenta questa correlazione per l'acqua nell'intervallo di temperatura compreso tra la temperatura ambiente e 110°C [1].
Come si vede chiaramente nella figura 1, l'acqua bolle già a 50°C se la pressione ambiente di 1013 mbar viene ridotta a 123 mbar. Questa correlazione viene utilizzata in applicazioni come l'essiccazione sottovuoto, in quanto il materiale da essiccare viene esposto a una pressione inferiore a quella ambiente e i liquidi (di solito l'acqua) possono quindi evaporare delicatamente a basse temperature. Questa tecnica è particolarmente utilizzata nel settore alimentare.
Esiste anche una correlazione simile a quella descritta per la riduzione del punto di ebollizione dei liquidi - anche se in forma leggermente più debole - per la sublimazione e la Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. decomposizione dei solidi.
Condizioni di misura
| Campione | SEBS | SEBS |
|---|---|---|
| Peso | 8.635 mg | 10.130 mg |
| Crogiolo | Al2O3 | Al2O3 |
| Atmosfera | Azoto | Vuoto |
| Portata del gas | 40 ml/min | 0 ml/min |
| Velocità di riscaldamento | 5 K/min | 5 K/min |
Indagini termogravimetriche a pressione ridotta
Come nel caso del processo di ebollizione, anche altre reazioni in cui si liberano sostanze gassose dipendono dalla pressione ambiente. Anche gli intervalli di temperatura delle Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. reazioni di decomposizione si spostano verso valori più bassi al diminuire della pressione ambiente. Questo spostamento di temperatura varia a seconda del processo o della sostanza. Ciò significa che l'applicazione di un'atmosfera a pressione negativa può influenzare in misura diversa il rilascio di prodotti di Reazione di decomposizioneUna reazione di decomposizione è una reazione termicamente indotta di un composto chimico che forma prodotti solidi e/o gassosi. decomposizione gassosa per le diverse reazioni. Questa procedura può essere particolarmente vantaggiosa se i processi di degradazione termica si sovrappongono, ossia se si verificano in stretta prossimità temporale l'uno dall'altro. La riduzione della pressione ambiente può quindi migliorare la separazione degli eventi che si sovrappongono.
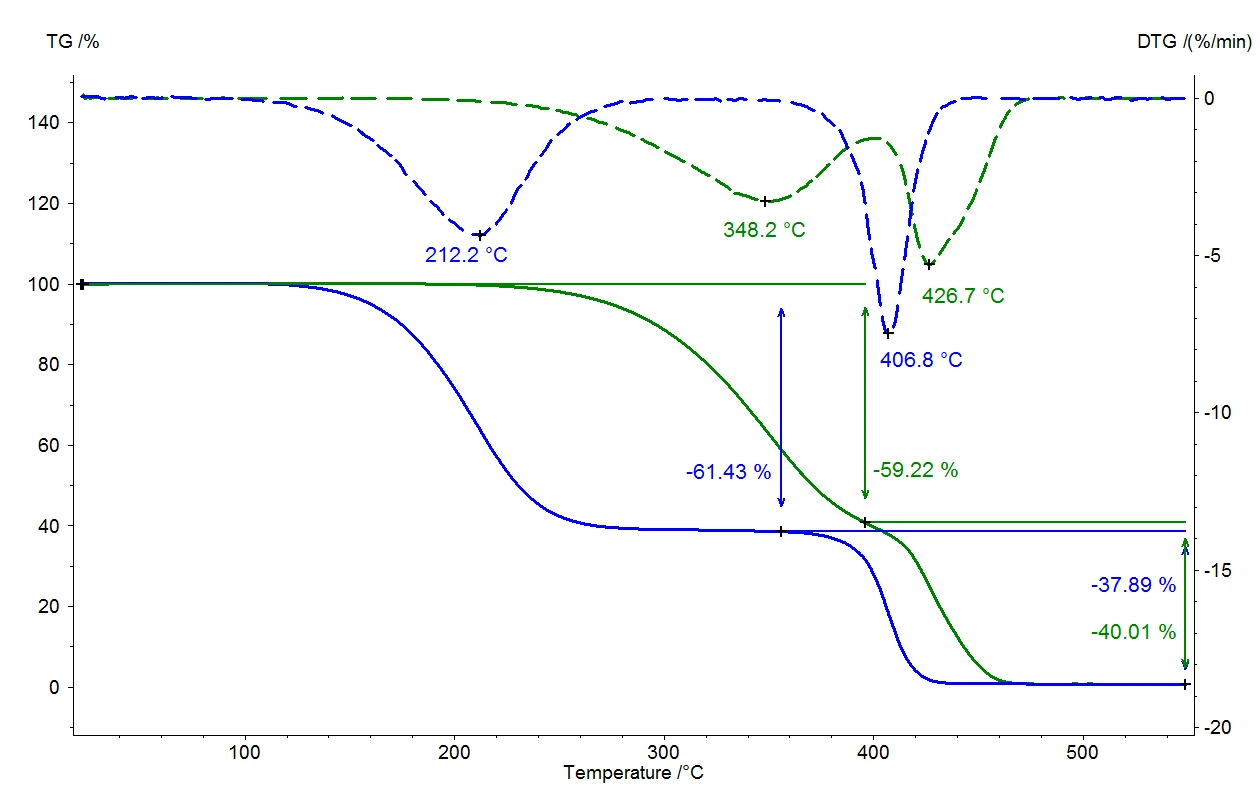
La Figura 2 mostra il confronto di due misure su un elastomero termoplastico. Le linee solide rappresentano la variazione di massa relativa in funzione della temperatura. La curva verde rappresenta i risultati della misurazione a pressione normale con una velocità di spurgo di 40 ml/min in azoto. Si notano due fasi di perdita di massa, che si sovrappongono anche alla bassa velocità di riscaldamento di 5 K/min. La quantificazione delle fasi è difficile in questo caso. Se questa indagine viene condotta nel vuoto - alla stessa velocità di riscaldamento di 5 K/min (curva blu) - tutte le temperature di rilascio si spostano su valori inferiori rispetto alla misurazione sotto pressione normale. La fine della reazione viene raggiunta a 480°C sotto pressione normale, ma nel vuoto la reazione è già terminata a 440°C. Le curve tratteggiate (DTG) mostrano la derivata prima per ciascuna delle variazioni di massa relativa (TG). I risultati del DTG indicano la velocità di perdita di massa e sono quindi una misura della velocità di reazione. Le temperature dei tassi massimi di perdita di massa (massimi DTG) confermano che entrambe le reazioni parziali sono spostate a temperature più basse quando avvengono nel vuoto. Tuttavia, poiché la prima reazione parziale (da 348°C a 212°C) è spostata a temperature notevolmente inferiori rispetto alla seconda (da 427°C a 407°C), le due reazioni parziali sono meglio separate. La quantificazione delle due fasi di perdita di massa è quindi notevolmente facilitata.