27.03.2023 by Dr. Ligia de Souza
이상적인 용해도를 결정하기 위한 DSC? 방법을 알려주세요!
시차 주사 열량 측정(DSC)은 제약 산업에서 약물 물질의 열적 특성을 조사하기 위해 널리 사용되는 분석 기술입니다. DSC의 주요 응용 분야 중 하나는 효과적이고 안전한 의약품 제형을 개발하는 데 중요한 약물의 이상적인 용해도를 결정하는 것입니다. 이 문서에서는 DSC를 사용하여 약물의 이상적인 용해도를 결정하는 방법과 용해도 거동에 영향을 미칠 수 있는 요인에 대해 살펴봅니다. 제약 업계의 연구자, 과학자 또는 제형 제작자라면 이 글( NETZSCH 이상적인 용해도 결정을 위한 분석 및 테스트)을 통해 DSC 기기 사용에 대한 귀중한 통찰력을 얻을 수 있을 것입니다. 이제 이 주제에 대해 자세히 알아봅시다!
용해도에 따른 약물 분류
용해율은 약물 생체 이용률에 직접적인 영향을 미치기 때문에 약물이 치료 목표에 도달하기 위해서는 수용성이 필수적입니다. 미국 약전과 유럽 약전은 대략적인 용해도 범위(mg/ml)를 기준으로 약물을 분류합니다. 예를 들어, 100-1000 mg/ml는 수용성으로 간주되는 분자의 용해도 범위이며, 0.1-1 mg/ml는 수용성이 매우 약한 약물 분자의 용해도 범위입니다. 따라서 수용성 및 비수용성 용해도를 결정하면 좋은 약물 후보를 위한 최상의 제형 접근법을 정의할 수 있습니다.
이상적인 용해도는 이상적인 용매를 사용할 때 용질의 포화 농도를 몰 분율로 나타낸 것으로, 용해 과정에서 에너지 손실 없이 용매에 용해되는 이론적인 경우를 말합니다. 실제로는 용질-용매 상호작용이 일반적으로 이상적이지 않고 용질과 용매 사이의 화학적 상호작용이 용해 과정을 방해할 수 있기 때문에 이를 달성할 수 없습니다. 이러한 분자 간 상호작용의 예로는 수소 결합, 유전체 특성, 쌍극자 모멘트가 있습니다.
분자의 용해도를 결정하기 위해 선택하는 방법은 UV 분광광도법이지만, 물질의 녹는점과 융합 엔탈피를 알면 이상적인 용해도를 계산할 수 있습니다.
하지만 열역학적 측면에서 이상적인 용해도는 무엇을 의미할까요?
용해 과정에서는 용질과 용질의 결합이 끊어져야 합니다. 이러한 결합을 끊는 데 필요한 에너지 투입량은 고체를 녹이는 데 필요한 에너지, 즉 융합 엔탈피(∆Hf)와 같습니다. 반면 용매-용매 결합은 용질-용매 결합이 형성되는 동안에도 끊어져야 합니다. 이 마지막 단계에 투입되는 에너지를 혼합 엔탈피(∆Hmix)라고 부를 수 있습니다. 따라서 용해 엔탈피는 융합 엔탈피와 혼합 엔탈피의 합입니다:
∆Hsol = ∆Hf + ∆Hmix
혼합 엔탈피가 0이면 용해 엔탈피는 융합 엔탈피와 같고, 혼합 엔탈피가 0이면 용해 엔탈피는 융합 엔탈피와 같습니다:
∆Hsol = ∆Hf
이것이 결정성 물질의 이상적인 용해에 대한 주요 열역학적 가정입니다. 이상적인 용해는 이상적인 용해도로 이어집니다.
다른 가정으로는 ∆Hf가 양수이고(핵융합은 흡열 현상) ∆Hsol도 양수라는 가정이 있습니다. 그러나 자발 반응이 일어나기 위해서는 깁스 자유 에너지(∆G = ∆Hf -T∆S)가 음수여야 하며, 따라서 엔트로피(S)는 양수여야 합니다. 용융 온도와 융합 엔탈피가 실험 온도와 무관하고 용해가 포화 용액을 제공한다는 점을 고려하면 반트 호프 방정식을 다음과 같이 적용할 수 있습니다:
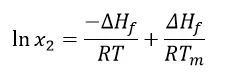
참고: x2 = 약물의 포화 농도(몰 분획 단위)
∆Hf = 융합 엔탈피(J/mol)
r = 기체 상수(J/K∙몰)
t = 주어진 온도(K)
tm = 용융 온도(K)
결과는 이상적인 용매에서 용질의 포화 농도를 몰 분율로 산출합니다. 즉, 이것은 가능한 최상의 용매에서 달성할 수 있는 약물의 최대 농도입니다. Aulton의 약학 책[1]에서는 아세틸살리실산의 예를 인용하고 있습니다. 아세틸살리실산의 (계산된) 이상적인 용해도는 0.037 몰 분획이며, 가장 좋은 용매는 실험적으로 결정된 용해도가 0.036 몰 분획인 테트라하이드로푸란(THF)입니다. 따라서 THF는 아세틸살리실산에 가장 이상적인 용매에 가깝습니다. 그러나 분자 간 상호작용이 용해에 유리하게 작용하여 반트 호프 방정식으로 추정된 것보다 더 높은 실험 용해도를 제공할 수도 있다는 점을 염두에 두어야 합니다.
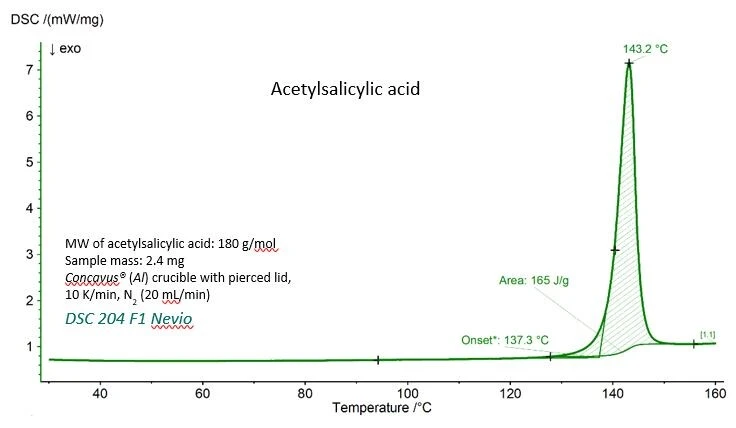
아세틸살리실산에 대한 용융 온도(추정 시작 온도) 및 융합 엔탈피(피크 아래 면적)에 대한 실험값이 포함된 DSC 곡선은 그림 1에 나와 있습니다. 표 1에서 볼 수 있듯이 두 값 모두 미국표준기술연구소(NIST)에서 제공하는 기준값과 매우 잘 일치합니다.
표 1 - 아세틸살리실산의 용융 온도 및 융합 엔탈피에 대한 실험값과 기준값.
파라미터 | 실험값 | 참조 (NIST 화학 웹북) |
| 미팅 온도(추정 시작 온도) | 410.4 K(137.3 °C) | 405±10 K |
융합 엔탈피 (피크 아래 면적) | 29.7 kJ/mol(165 J/g) | 29.17 - 31.01 kJ/mol |
아스피린(nist.gov)https://webbook.nist.gov/cgi/cbook.cgi?ID=C50782&Units=SI&Mask=4#Thermo-Phase
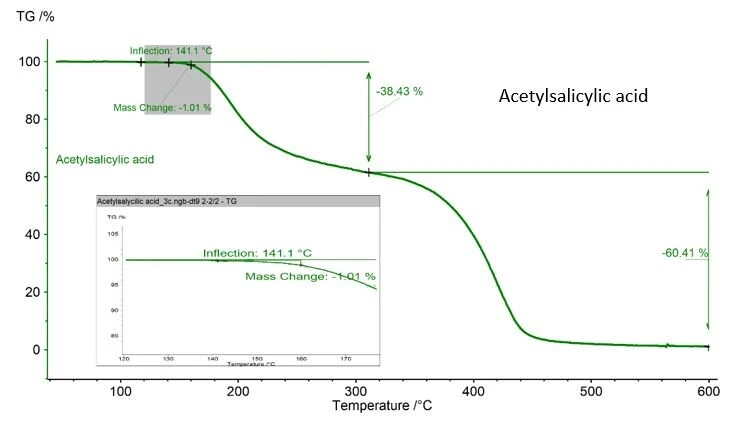
분석 물질이 DSC 측정 중에 열 분해될 수 있으므로 주의해야 합니다. 여기에 표시된 아세틸살리실산 예의 경우, NETZSCH TGA로 측정한 결과 1.01%의 질량 손실이 기록되었습니다(그림 2). 이 값은 ASTM 928에서 용융 범위의 최대 질량으로 1%를 규정하고 있으므로 허용되는 값입니다. TGA를 사용할 수 없는 경우, 측정 전후에 도가니와 샘플의 무게를 측정하는 것이 질량 손실을 모니터링하는 가장 좋은 방법입니다.
상 전이, 고체와 고체의 상호작용, 화학 성분의 변화, purity determination 등은 정확하고 정밀한 결과를 제공하는 민감한 기술인 DSC의 응용 분야입니다.
참조:
[1] Aulton의 약리학, 6판, ISBN: 9780702081545
아스피린(nist.gov)https://webbook.nist.gov/cgi/cbook.cgi?ID=C50782&Units=SI&Mask=4#Thermo-Phase
요약
결론적으로, NETZSCH 분석 및 테스트의 기기를 사용하면 제약 개발 프로세스에서 약물의 이상적인 용해도를 결정하는 데 크게 기여할 수 있습니다. 약물 물질의 열적 특성에 대한 귀중한 통찰력을 제공함으로써 DSC와 TGA는 제제 제조자와 과학자가 약물 제형을 최적화하여 생체 이용률과 효능을 개선하는 데 도움을 줄 수 있습니다.
NETZSCH 분석 및 테스트가 귀사의 제약 개발 요구 사항을 어떻게 지원할 수 있는지 자세히 알아보려면 당사 웹사이트를 방문하여 자세한 정보를 확인하세요. 전문가가 모든 단계에서 도움을 드릴 수 있습니다.
"제약 분야의 열 분석" 애플리케이션 북을 이미 알고 계십니까?
이 응용서에서는 다양한 구체적인 응용 사례를 통해 해당 실험을 수행하는 방법과 그 결과에서 어떤 결론을 도출할 수 있는지 설명합니다.

이 책은 260페이지가 넘는 8개의 챕터로 구성되어 있습니다:
- 열 분석 방법(DSC, TGA, STA 및 가스 분석)
- 비정질 및 결정상의 특성 분석
- 순도
- 열 안정성
- 산화 안정성
- 보관 조건 및 보관 수명
- 다형성 및 호환성