Introduzione
Gli ossalati sono sali dell'acido ossalico C2H2O4 (COOH)2 (acido etanedicarbossilico). Il sale di calcio dell'acido ossalico, l'ossalato di calcio, cristallizza in forma anidra e come solvato con una molecola d'acqua per formula, come ossalato di calcio monoidrato CaC2O4*H2O.
Ricorrenza e applicazione
Sebbene l'ossalato di calcio monoidrato sia il sale di un aicd organico, può essere trovato in natura come minerale primario. La Figura 1 mostra un cristallo di Whewellite proveniente dalla località di Schlema, nella catena montuosa dell'Erzgebirge in Germania. Oltre alla Whewellite, la weddellite è nota anche come seconda specie minerale [1].

L'ossalato di calcio è anche il componente principale dei calcoli renali.
In analisi termica, l'ossalato di calcio monoidrato viene utilizzato per verificare la funzionalità delle termobilance. Questa sostanza ha una buona stabilità allo stoccaggio; non è soggetta a variazioni nel tempo, né ha la tendenza ad assorbire l'umidità dell'atmosfera del laboratorio. Queste caratteristiche la rendono una sostanza di riferimento ideale per il controllo della funzionalità termo-base di una termobilancia.
Condizioni di misura
- Strumento
- TG 209 F1 Libra®
- Campione
- CaC2O4*H2O
- Peso del campione
- 8.43 mg (curva nera in figura 2) e
- 8.67 mg (curva rossa in figura 2)
- Crogiolo
- Al2O3
- Atmosfera
- Azoto
- Portata del gas
- 40 ml/min
- Velocità di riscaldamento
- 10 K/min (curva nera in figura 2) e
- 200 K/min (curva rossa in figura 2)
Termogravimetria
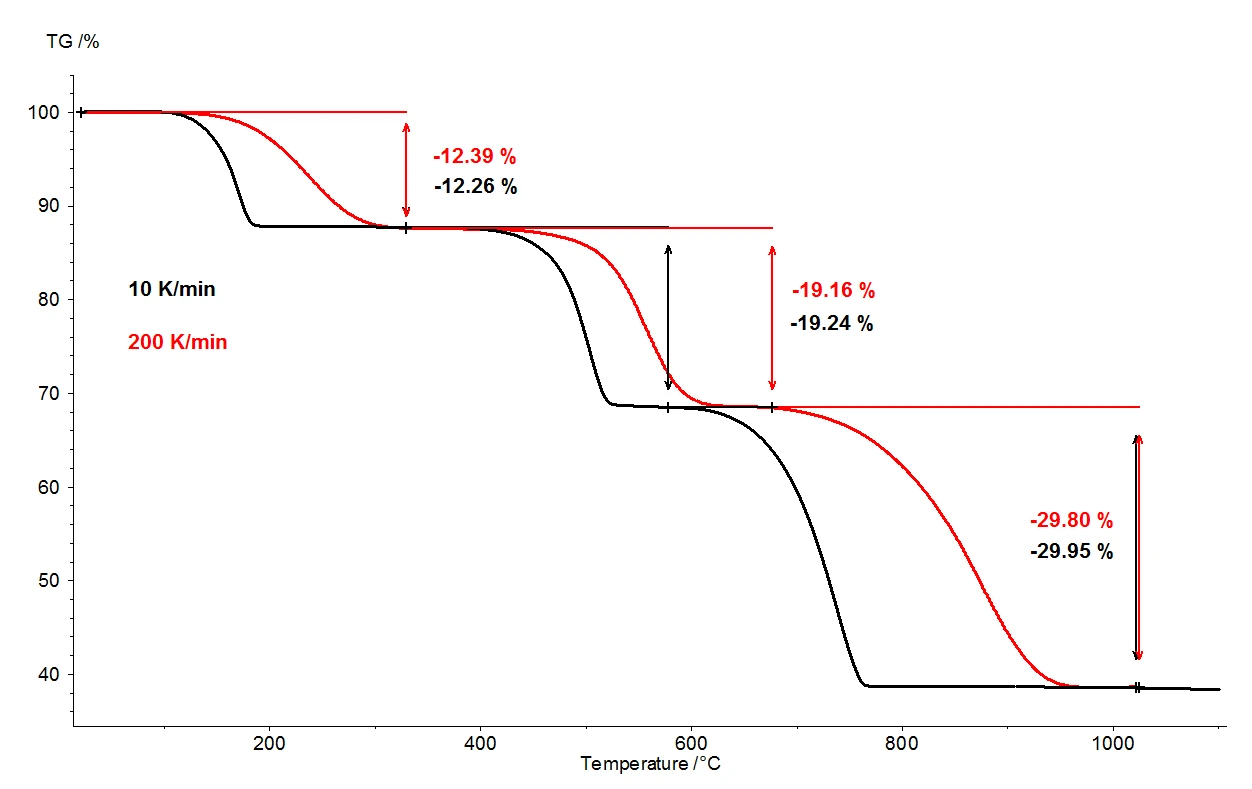
Quando l'ossalato di calcio monoidrato viene riscaldato a 1100°C, la termobilancia consente di rilevare tre fasi di perdita di massa chiaramente separate. La Figura 2 mostra un confronto dei risultati termogravimetrici di due misurazioni su campioni di ossalato di calcio monoidrato. Le variazioni di massa relativa dei campioni sono registrate in base alla temperatura. La figura 3 mostra l'analogo confronto tra le due misure, in funzione della temperatura, per la derivata prima dei risultati termogravimetrici (DTG).
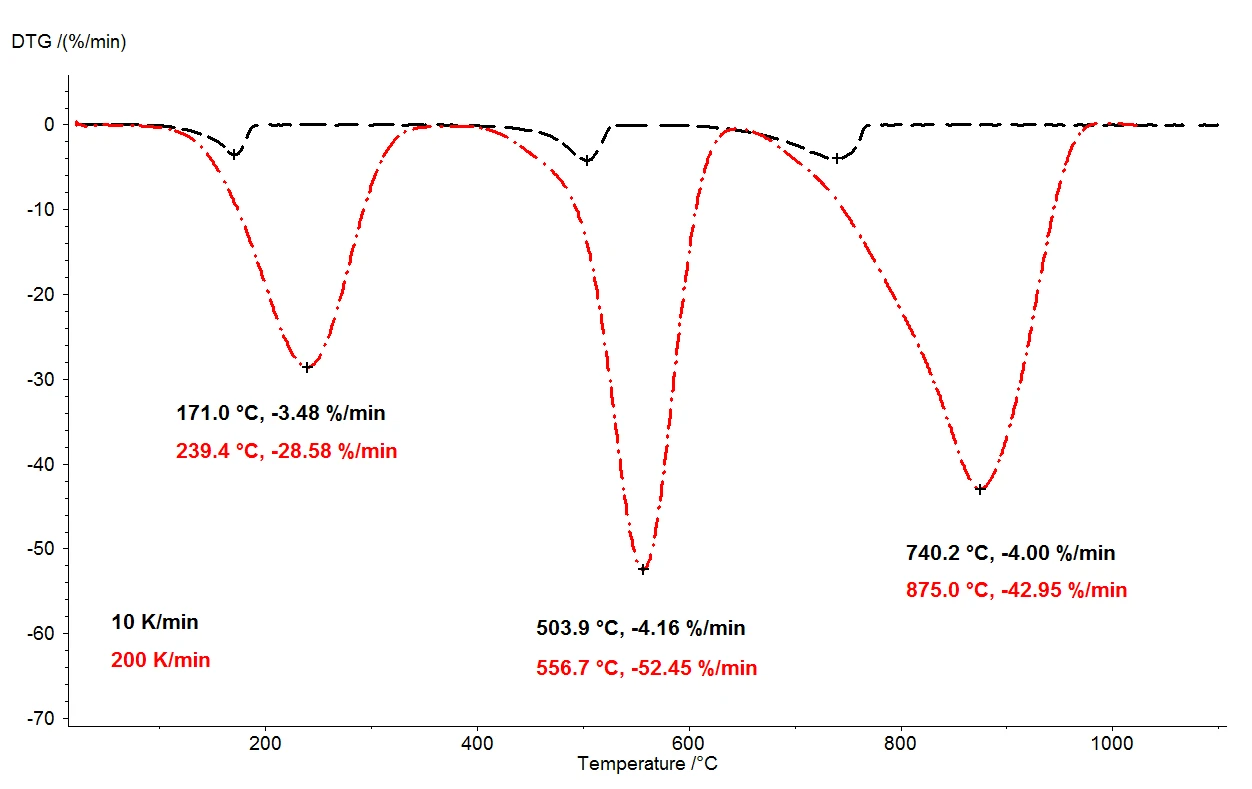
In condizioni altrimenti identiche, sono state selectdue diverse velocità di riscaldamento: 10 K/min (curva nera) e 200 K/min (curva rossa). Con l'aumento della velocità di riscaldamento, le temperature delle fasi di perdita di massa si spostano verso valori più elevati e le velocità di rilascio - la velocità di rilascio del gas - aumentano di circa dieci volte (minimi DTG, figura 3). Lo spostamento della temperatura che avviene al variare della velocità di riscaldamento è un fenomeno ben noto che può essere applicato per un'ulteriore valutazione dei dati cinetici [2]. Oltre allo spostamento di temperatura, è importante notare che la quantificazione delle fasi di perdita di massa è indipendente dalla velocità di riscaldamento. La velocità di riscaldamento di 200 K/min fornisce quindi tutte le stesse informazioni sulla degradazione termica dell'ossalato di calcio monoidrato rispetto alla più consueta velocità di riscaldamento di 10 K/min; nessuna informazione viene persa accelerando la velocità di riscaldamento. Pur fornendo lo stesso contenuto informativo, tuttavia, la velocità di riscaldamento più rapida si traduce in un enorme risparmio di tempo: una misurazione a 10 K/min richiede quasi due ore per coprire l'intervallo di temperatura da temperatura ambiente a 1100°C, ma la stessa misurazione a 200 K/min viene completata già in cinque minuti.
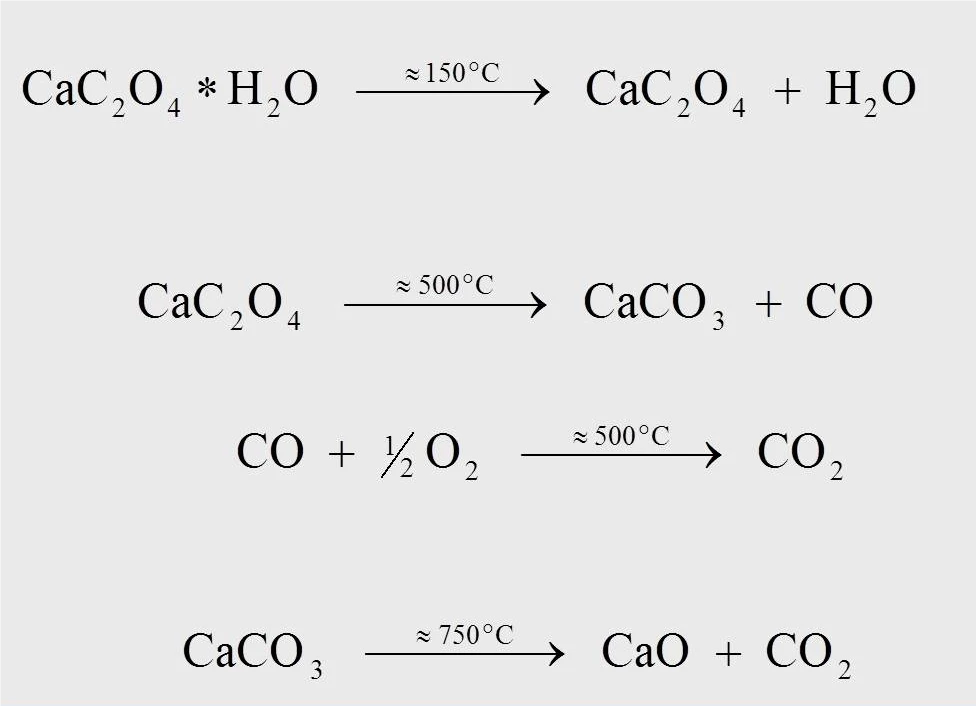
Le equazioni di reazione per la reazione di degradazione termica dell'ossalato di calcio monoidrato sono riportate nella figura 4. A circa 170°C, per la misurazione a 10 K/min, si forma ossalato di calcio anidro quando l'acqua si separa dal monoidrato (1). A circa 500°C, l'ossalato di calcio si trasforma in carbonato di calcio (CaCO3) e il monossido di carbonio (CO) si separa (2). La reazione successiva, in cui il monossido di carbonio rilasciato viene ossidato ad anidride carbonica (CO2) (3), può avvenire solo in un flusso di gas di lavaggio contenente ossigeno (ad esempio, aria sintetica o ossigeno). A una temperatura di 750°C, il carbonato di calcio si decompone in ossido di calcio con il rilascio diCO2 (4).