Wprowadzenie
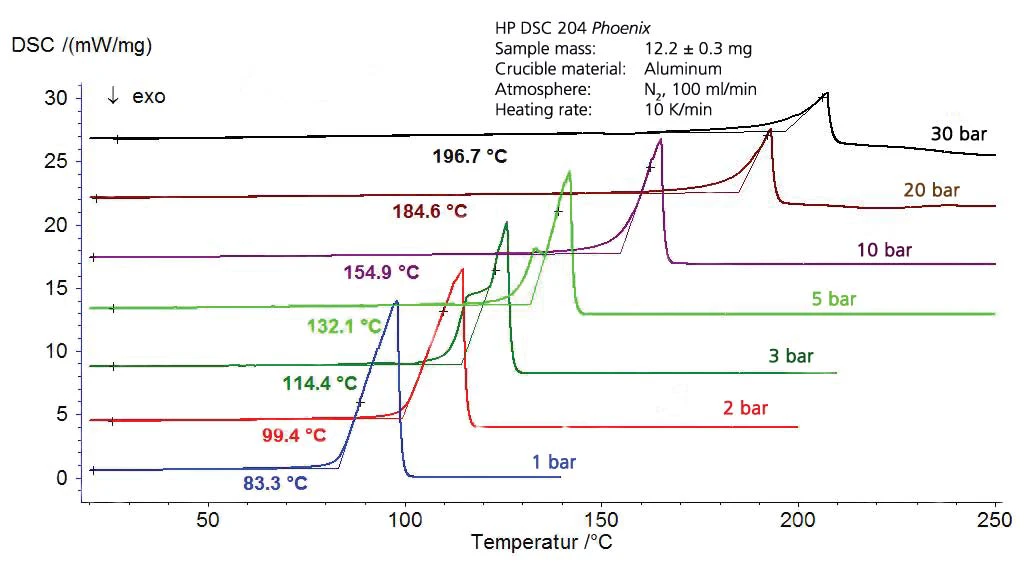
Różnicowa kalorymetria skaningowa (DSC) pozwala nie tylko na określenie temperatury przemiany fazowej, ale także na ilościowe określenie entalpii przemiany. Próbki są zazwyczaj analizowane w aluminiowych tyglach z przebitą pokrywą pod ciśnieniem atmosferycznym w stałym przepływie gazu oczyszczającego. W przypadku zmodyfikowanych przyrządów - w których cela pomiarowa jest zainstalowana w autoklawie (tzw. ciśnieniowa DSC) - możliwe są dodatkowo pomiary w zakresie ciśnień od 5 kPa do 15 MPa [1]. W niniejszej nocie aplikacyjnej ciecze są analizowane pod kątem ich parowania w tym zakresie ciśnienia.
Ponieważ parowanie cieczy przed osiągnięciem temperatury wrzenia i równowaga między cieczą a gazem podczas wrzenia są parametrami krytycznymi, które mogą mieć negatywny wpływ na reakcję i późniejszą ocenę, do tych pomiarów zastosowano specjalne tygle. Dobre doświadczenia uzyskano z tyglami aluminiowymi spawanymi na zimno z otworem small o średnicy 50 μm.
Równanie Antoine'a opisuje zależność prężności pary nasyconej czystej substancji od temperatury:
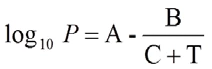
gdzie P jest ciśnieniem w barach, T jest temperaturą w K, a zmienne A, B i C są stałymi specyficznymi dla danego składnika. Nie można ich jednak użyć do opisania całego procesu krzywej temperatury wrzenia substancji. Dlatego istnieje kilka zestawów parametrów dla zakresu od punktu potrójnego do punktu krytycznego.
Poniższa tabela podsumowuje badane ciecze: wodę, cykloheksan, octan etylu i izopropanol dla zakresu ważności wykorzystanych danych literaturowych:
Tabela 1: Zakres temperatur i współczynniki równania Antoine'a [3, 4, 5]
| Substancja | Zakres temperatur [K] | Zakres temperatur [°C] | A | B | C |
|---|---|---|---|---|---|
| H2O | 313 ... 385 | 40 ... 112 | 6.1680 | 1397.2 | -48.097 |
| C6H12 | 323 ... 523 | 50 ... 250 | 4.1398 | 1316.5 | -35.581 |
| C4H8O2 | 288 ... 348 | 15 ... 75 | 4.2280 | 1245.7 | -55.189 |
| C3H8O | 395 ... 508 | 122 ... 235 | 4.5779 | 1221.4 | -87.474 |
Wyniki
Woda
Wyniki dla wody destylowanej dla zakresu ciśnień powyżej ciśnienia atmosferycznego pokazano na rysunku 1 (ciśnienie pokazano liniami przerywanymi); rysunek 2 przedstawia zakres ciśnień od 45 mbar do 236 mbar. Rysunek 3 pokazuje dobrą zgodność danych literaturowych z [2] (ASTM E782) ze wszystkimi ustalonymi wartościami pomiarowymi.
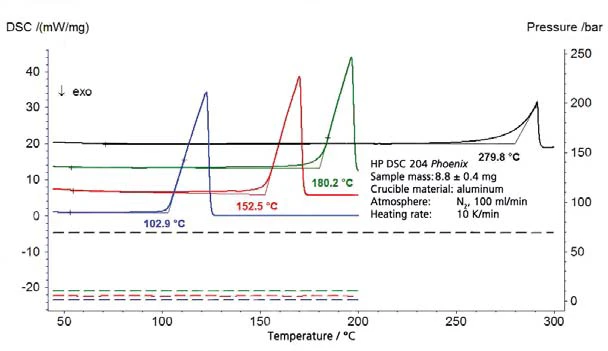
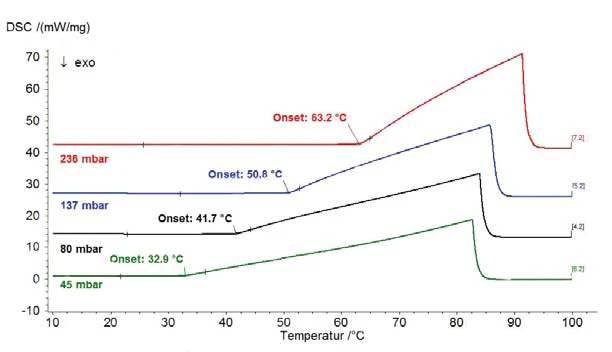
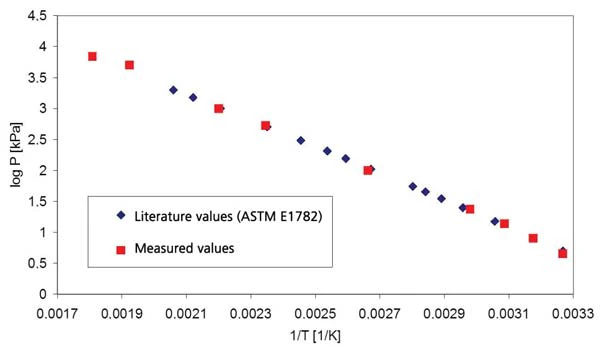
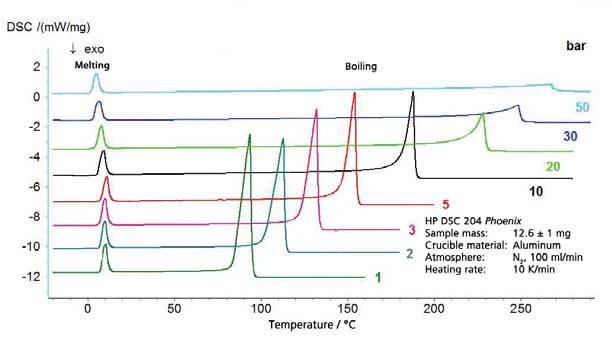
Cykloheksan
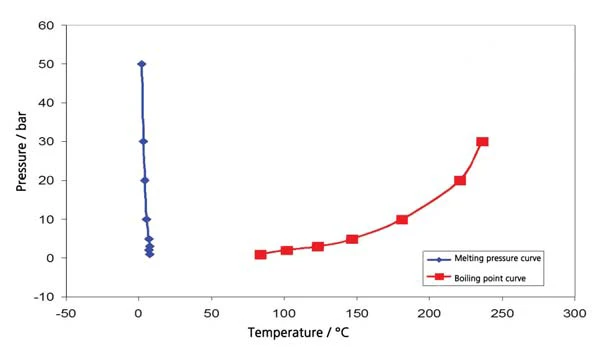
Wyniki dla cykloheksanu w zakresie temperatur od -20°C do 300°C (rysunek 4) obejmują zarówno wrzenie, jak iTemperatury i entalpie topnieniaEntalpia syntezy substancji, znana również jako ciepło utajone, jest miarą nakładu energii, zazwyczaj ciepła, która jest niezbędna do przekształcenia substancji ze stanu stałego w ciekły. Temperatura topnienia substancji to temperatura, w której zmienia ona stan ze stałego (krystalicznego) na ciekły (stopiony izotropowo). topnienie. Skutkuje to segmentem diagramu fazowego, przedstawionym na rysunku 5. Rysunek 6 przedstawia porównanie z literaturą [3].
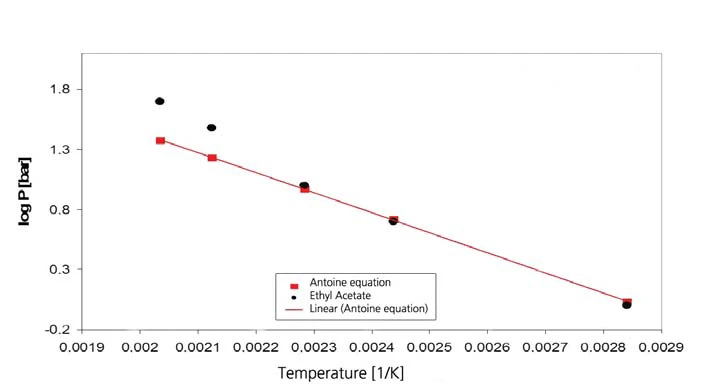
Octan etylu
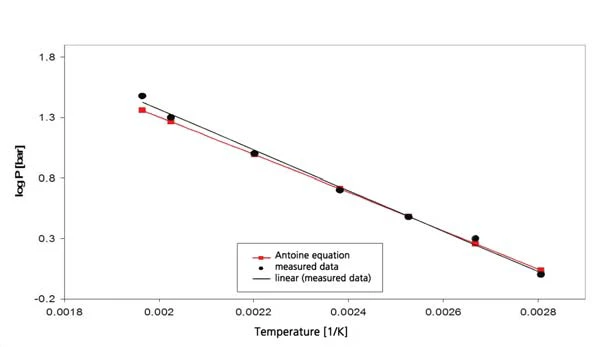
Wyniki dla octanu etylu przedstawiono na rysunkach 7 i 8. Wartości literaturowe są jednak wartościami ekstrapolowanymi, ponieważ zakres ważności równania Antoine'a z [4] jest ograniczony do przedziału od 15°C do 75°C (288 K do 348 K, co odpowiada odwrotnym wartościom temperatury od 0,00347 do 0,00287).
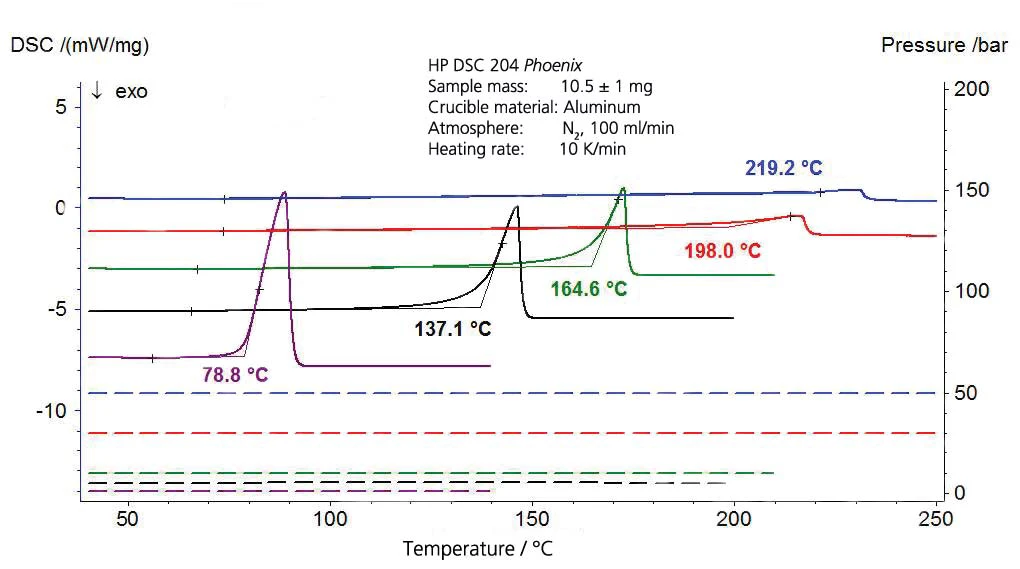
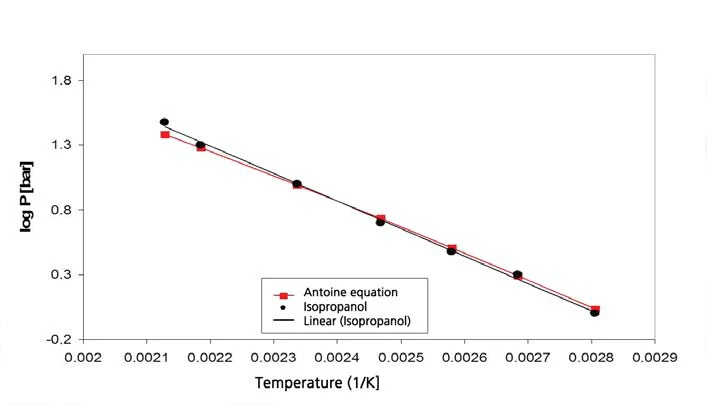
Izopropanol
Rysunki 9 i 10 przedstawiają wyniki pomiarów i porównanie wartości literaturowych [5] dla izopropanolu.
Podsumowanie
Różnicowa kalorymetria skaningowa (DSC) - w połączeniu z możliwością zmian ciśnienia w celi pomiarowej - pozwala na badanie zależności przemian fazowych od ciśnienia. Wyniki dla przejścia ciecz-gaz badanych substancji, wody, cykloheksanu, octanu etylu i izopropanolu są w bardzo dobrej zgodności z literaturą.