
04.12.2023 von Dr. Gabriele Kaiser
IQ, OQ – Gerätequalifizierung im Pharmabereich und ihre Bedeutung für Anwender der thermischen Analyse
Dieser Artikel richtet sich insbesondere an Anwender der dynamischen Differenzkalorimetrie (DSC) und thermogravimetrischen Analyse (TG), basierend auf USP <1058>.
Insbesondere im pharmazeutischen Bereich sind Präzision und Einhaltung von Prozessvorschriften von größter Bedeutung. Geleitet von den Standards des United States Pharmacopeia (USP), stellen die Installationsqualifizierung (IQ) und die Funktionsqualifizierung (OQ) nicht nur Routinekontrollen dar. Sie bilden die Grundlage zur Sicherstellung von Genauigkeit und Zuverlässigkeit in der pharmazeutischen Forschung und Qualitätskontrolle.
IQ und OQ sind Teil des so genannten Qualifizierungsprozesses für Analysegeräte (AIQ) im Labor des Anwenders, um zu bescheinigen, dass ein Gerät ordnungsgemäß installiert ist, einwandfrei funktioniert und die erwarteten Ergebnisse liefert. Ein Schlüsselbegriff in diesem Zusammenhang ist der „Nachweis der Gebrauchstauglichkeit“. Was sich dahinter verbirgt, soll im Folgenden insbesondere anhand von USP <1058>, dem entsprechenden Kapitel der US-Pharmakopöe, näher erläutert werden.
Risikobasierter Ansatz
Abhängig von der Komplexität des Geräts bzw. wie kritisch die damit durchgeführten Messungen sind werden die Geräte in 3 Gruppen eingeteilt: A, B und C. Je nach Verwendungszweck können jedoch ein und derselbe Gerätetyp in die eine oder andere Gruppe fallen.
- Gruppe A umfasst Standardgeräte ohne Messfähigkeit, die vom Anwender nicht kalibriert werden müssen. Ist die Funktionstüchtigkeit gegeben, ist hier keine weitere Qualifizierung erforderlich.
- Zur Gruppe B gehören Geräte, die Messwerte oder Versuchsbedingungen liefern, die eine Messung beeinflussen können und daher eine routinemäßige Kalibrierung, Wartung und Leistungsüberprüfung erfordern. Diese Geräte können über eine Firmware, jedoch nicht über eine Software, verfügen, die vom Anwender aktualisiert wird.
- Gruppe C beinhaltet Geräte mit einem hohen Grad an Computerisierung und Komplexität. Sie sind mit einem Computer verbunden und erzeugen elektronische Aufzeichnungen. Für diese Geräte sind alle Elemente der Qualifizierung (siehe unten) sowie eine Softwarevalidierung erforderlich. Die Softwarevalidierung und Gerätequalifizierung können jedoch in einer Aktivität zusammengefasst werden, da die Software in der Regel zum Betrieb des Gerätes zwingend erforderlich ist.
In USP <1058> wird nur eine begrenzte Anzahl an Gerätebeispielen genannt: pH-Meter und Öfen für Gruppe B sowie Massenspektrometer und HPLC-Geräte für Gruppe C. In älteren Versionen der USP werden DSC und TG explizit als Gruppe C klassifiziert.
Die vier Qualifizierungsphasen
Dies sind DQ (Designqualifizierung), IQ (Installationsqualifizierung), OQ (Funktionsqualifizierung) und PQ (Leistungsqualifizierung). PQ wird manchmal als auch „Benutzerakzeptanztest" (User Acceptance Test, UAT) bezeichnet." Falls erforderlich kann dieser Rahmen bei komplexen Systemen durch Funktionsspezifikationen (FS) und/oder Werksabnahmeprüfungen (Factory Acceptance Test, FAT) erweitert werden. Am wichtigsten ist, dass alle erforderlichen Aktivitäten in logischer Reihenfolge durchgeführt werden. Darüber hinaus sollten alle Qualifizierungsaktionen vordefiniert und zeitnah dokumentiert werden.
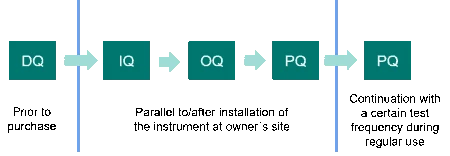
Designqualifizierung
Die DQ findet vor der Kaufentscheidung statt und definiert das Anwenderprofil des DSC- oder TG-Geräts. Sie umfasst alle Spezifikationen sowie den Verwendungszweck des Geräts und zeigt schließlich, dass das ausgewählte Gerät geeignet ist. Die DQ kann durch den Gerätehersteller oder durch den Anwender durchgeführt werden. Einige Laboratorien erstellen zusätzlich Nutzeranforderungslisten (User Requirement Specification Lists, URS), die der DQ vorangehen. In der URS legen die zukünftigen Anwender fest, was das Gerät können soll.
Installationsqualifizierung
IQ steht für den dokumentierten Nachweis, dass das jeweilige DSC- oder TG-Gerät einschließlich Software, Zubehör usw. wie vorgesehen und spezifiziert geliefert wurde, dass die geplante Umgebung geeignet ist und dass das Gerät ordnungsgemäß installiert wurde. Sie gilt für neue oder gebrauchte DSC- oder TG-Geräte und erfolgt nach Installation und Inbetriebnahme des Geräts am Standort des Eigentümers.
Funktionsqualifizierung
Die OQ folgt der Installationsqualifizierung. Sie ist eine dokumentierte Sammlung von Aktivitäten mit dem Ziel nachzuweisen, dass das DSC- oder TG-Gerät in der gewählten Umgebung ordnungsgemäß funktioniert und die in der Designqualifizierung (DQ) und/oder der Benutzeranforderungsliste (URS) angegebenen Spezifikationen erfüllt.
Leistungsqualifizierung
Die PQ ist die letzte der vier Qualifizierungsphasen und dokumentiert die kontinuierliche Eignung des DSC- oder TG-Geräts für den vorgesehenen Einsatz unter realen Betriebsbedingungen. Dies beinhaltet in der Regel typische Vor-Ort-Anwendungen und die Verwendung laboreigener Substanzen. Die Häufigkeit der Tests hängt unter anderem von der Robustheit des DSC- oder TG-Geräts, der Erfahrung des Bedieners sowie der Wichtigkeit der Analysemethode ab. Ein weiterer Teil der Leistungsqualifizierung ist die vorbeugende Wartung und die Dokumentation von Reparaturen und Änderungen an den Geräten. Die vorbeugende Wartung umfasst auch die regelmäßige Kalibrierung des DSC- oder TG-Geräts.
Verantwortung
Die Wartung für die Qualifizierung des DSC- oder TG-Geräts liegt letztlich beim Anwender, wobei der Begriff „Anwender“ nicht nur den Bediener, sondern auch dessen Vorgesetzte, die dazugehörigen Geräteexperten und die Unternehmensleitung mit einschließen. Gerätehersteller und -lieferanten können nur beraten und unterstützen.
Die Angebote von NETZSCH
NETZSCH Analysieren & Prüfen bietet verschiedene Dienstleistungen an, um Anwender bei der Qualifizierung von NETZSCH-DSC- oder TG-Geräten zu unterstützen. Diese sind:
- IQ-OQ-Dokumente (in Standardausführung und – optional – kundenspezifisch), einschließlich einer Vorlage für wiederkehrende PQ-Tests
- Installationen mit anschließender Bearbeitung der IQ-OQ-(PQ)-Dokumente
- Wartungsverträge einschließlich regelmäßiger Kalibrierung der Geräte
Interessiert? Wenden Sie sich gern an Ihren persönlichen Ansprechpartner:
Kennen Sie bereits unser Video "Development and Quality Control of Pharmaceuticals with Thermal Analysis and Kriechen (Rheologie)Creep is one of the earliest “controlled stress” rheometer tests that quite literally “creeps” the material, i.e. we measure over a relatively prolonged period the small movement (the creep defined as creep compliance, J) of the sample by applying a small constant stress.Rheology"? Schauen Sie rein!
Das NETZSCH Pharma-Buch
Das Buch enthält 8 Kapitel auf mehr als 260 Seiten zu:
- Methoden (DSC, TGA, STA und Gasanalyse)
- Charakterisierung von amorphen und kristallinen Phasen
- Reinheit
- Thermische StabilitätEin Material ist thermisch stabil, wenn es sich unter Temperatureinfluss nicht zersetzt. Eine Möglichkeit, die thermische Stabilität einer Substanz zu bestimmen ist die Verwendung eines TGA (thermogravimetrischer Analysator).Thermische Stabilität
- Oxidative Stabilität
- Lagerungsbedingungen und Haltbarkeitsdauer
- Polymorphismus
- Verträglichkeit













