Contrôle de processus intrinsèquement sûr
Les réactions doivent rester contrôlables à tout moment, non seulement à l'échelle du laboratoire (généralement moins d'un litre), mais aussi - et surtout - dans les réacteurs large qui produisent à l'échelle de la tonne. Même si des événements imprévus tels que la défaillance d'une pompe dans le cycle de refroidissement d'un réacteur se produisent, des précautions doivent déjà avoir été prises au stade de la planification de l'usine de production pour éviter que les réacteurs ne deviennent incontrôlables. Cette planification prospective, qui prend également en compte les événements imprévisibles, permet un fonctionnement intrinsèquement sûr des installations de production à tout moment [1].
Scénario le plus défavorable
Avant même de planifier les installations de production, il est essentiel d'évaluer les produits chimiques utilisés et les réactions prévues du point de vue de leur potentiel de risque. Afin d'éviter les mauvaises surprises en ce qui concerne la taille et la capacité des installations, l'augmentation de l'échelle ou même l'ordre dans lequel les réactifs sont ajoutés, des études sont souvent réalisées à cette fin, décrivant le scénario le plus défavorable. La connaissance du cas le plus défavorable permet de mieux contrôler toutes les conditions réelles de production. En ce qui concerne le contrôle de la température d'un réacteur, le cas le plus défavorable est le dépassement de la température prévue pour le processus en raison, par exemple, de la défaillance d'une pompe dans le cycle de refroidissement. Si le système de refroidissement tombe en panne et que la chaleur de réaction ne peut plus être équilibrée, la température dans le réacteur dépasse la température de réaction prévue. Cela peut entraîner des réactions secondaires indésirables. Dans le pire des cas, l'augmentation de la température et/ou de la pression peut provoquer l'éclatement du réacteur. Afin d'étudier ce qui se passe lorsque la température dans le réacteur augmente de manière incontrôlée, la vitesse à laquelle la température augmente et la pression qui s'accumule dans le réacteur, de telles réactions sont simulées à l'échelle small en laboratoire. Un instrument conçu pour étudier ce pire cas est le NETZSCH ARC® 254.
Le NETZSCH ARC® 254
Le NETZSCH ARC® 254 (figure 1) est un calorimètre à accélération capable d'effectuer des tests dits d'Emballement thermiqueUn emballement thermique est la situation dans laquelle un réacteur chimique est hors de contrôle en ce qui concerne la production de température et/ou de pression causée par la réaction chimique elle-même. La simulation d'un emballement thermique est généralement réalisée à l'aide d'un calorimètre selon la méthode de la calorimétrie à taux accéléré (ARC®).emballement thermique. L'objectif de cette technologie de mesure est de déterminer le potentiel dangereux en fonction de la température d'un échantillon ou d'un mélange réactionnel dans des conditions adiabatiques. L'adiabaticité signifie en particulier qu'il n'y a pas d'échange de chaleur. Si toute la chaleur de la réaction reste à l'intérieur d'un récipient de réaction et ne peut pas se dissiper dans l'environnement, la température augmentera et, par conséquent, la vitesse de réaction. Il en résultera un mécanisme de réaction auto-accéléré. L'étude de ces scénarios permet de calculer et de classer toutes les conditions du monde réel qui, en règle générale, ne sont pas totalement adiabatiques, puisqu'une certaine quantité de chaleur est toujours perdue dans l'environnement.

Comment détecter une réaction d'autodécomposition exothermique?
Pour détecter un Emballement thermiqueUn emballement thermique est la situation dans laquelle un réacteur chimique est hors de contrôle en ce qui concerne la production de température et/ou de pression causée par la réaction chimique elle-même. La simulation d'un emballement thermique est généralement réalisée à l'aide d'un calorimètre selon la méthode de la calorimétrie à taux accéléré (ARC®).emballement thermique, la température de la substance ou du mélange réactionnel à étudier est augmentée progressivement. À chaque palier de température, on attend un temps suffisant pour tempérer l'échantillon jusqu'à cette température. Ensuite, on détecte si la température de l'échantillon reste constante à cette température ou si elle augmente lentement, c'est-à-dire s'il y a ou non auto-échauffement de l'échantillon. Si aucun auto-échauffement n'est détecté, cette séquence d'augmentation progressive de la température (Heat-Wait-Search (HWS)Heat-Wait-Search est un mode de mesure utilisé dans les appareils calorimétriques selon la calorimétrie à taux accéléré (ARC).Heat-Wait-Search) se poursuit. Lorsque le Taux d'auto-échauffementUn type particulier de calorimètre est utilisé pour détecter le taux d'auto-échauffement d'une substance. La méthode correspondante est appelée calorimétrie à taux d'accélération (ARC®). taux d'auto-échauffement de 0,02 K/min est dépassé, l'instrument passe en mode dit AdiabatiqueAdiabatique décrit un système ou un mode de mesure sans aucun échange de chaleur avec l'environnement. Ce mode peut être réalisé à l'aide d'un calorimètre selon la méthode de la calorimétrie à taux accéléré (ARC®). L'objectif principal d'un tel dispositif est d'étudier des scénarios et des réactions d'emballement thermique. Une brève description du mode adiabatique est la suivante : "pas d'entrée de chaleur - pas de sortie de chaleur".adiabatique. Ce mode de mesure empêche la perte de chaleur dans l'environnement de l'échantillon, puisque tous les éléments chauffants entourant la chambre d'échantillon suivent la température de l'échantillon. Si tous les éléments chauffants ont la même température que l'échantillon, c'est-à-dire qu'il n'y a pas de gradient de température, aucune chaleur ne peut être perdue dans l'environnement. De cette manière, le site ARC® garantit un environnement d'échantillon AdiabatiqueAdiabatique décrit un système ou un mode de mesure sans aucun échange de chaleur avec l'environnement. Ce mode peut être réalisé à l'aide d'un calorimètre selon la méthode de la calorimétrie à taux accéléré (ARC®). L'objectif principal d'un tel dispositif est d'étudier des scénarios et des réactions d'emballement thermique. Une brève description du mode adiabatique est la suivante : "pas d'entrée de chaleur - pas de sortie de chaleur".adiabatique dans la mesure du possible. Il s'agit là d'une condition préalable importante pour étudier un scénario catastrophe tel que l'Emballement thermiqueUn emballement thermique est la situation dans laquelle un réacteur chimique est hors de contrôle en ce qui concerne la production de température et/ou de pression causée par la réaction chimique elle-même. La simulation d'un emballement thermique est généralement réalisée à l'aide d'un calorimètre selon la méthode de la calorimétrie à taux accéléré (ARC®).emballement thermique.
Comment mesure-t-on une réaction d'emballement thermique ?
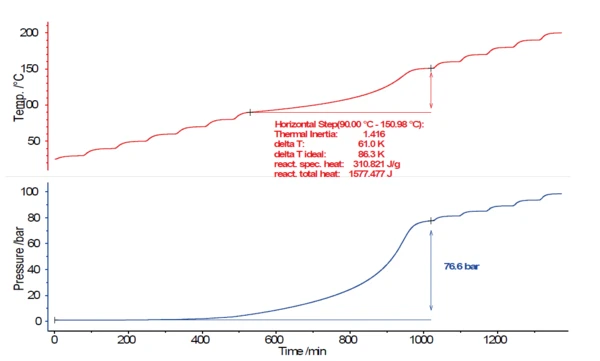
Si un Emballement thermiqueUn emballement thermique est la situation dans laquelle un réacteur chimique est hors de contrôle en ce qui concerne la production de température et/ou de pression causée par la réaction chimique elle-même. La simulation d'un emballement thermique est généralement réalisée à l'aide d'un calorimètre selon la méthode de la calorimétrie à taux accéléré (ARC®).emballement thermique commence à se produire au cours d'une réaction, il est souhaitable de déterminer ce point critique dans le temps ou la température le plus tôt possible. Effectuée de manière séquentielle, la température de l'échantillon n'augmentera d'abord que très lentement au début de l'auto-échauffement. 0.02 K/min est un Taux d'auto-échauffementUn type particulier de calorimètre est utilisé pour détecter le taux d'auto-échauffement d'une substance. La méthode correspondante est appelée calorimétrie à taux d'accélération (ARC®). taux d'auto-échauffement très faible, correspondant à seulement 1,2 K par heure. La Réaction de décompositionUne réaction de décomposition est une réaction thermiquement induite d'un composé chimique formant des produits solides et/ou gazeux. réaction de décomposition commence lentement, mais sa vitesse augmente continuellement avec l'augmentation de la température jusqu'à ce qu'elle atteigne sa vitesse d'auto-échauffement maximale et finalement la température maximale. La figure 3 montre les résultats pour la température (rouge) et la pression (bleu) d'un test Heat-Wait-Search (HWS)Heat-Wait-Search est un mode de mesure utilisé dans les appareils calorimétriques selon la calorimétrie à taux accéléré (ARC®).HWS sur une solution de peroxyde d'hydrogène (H2O2) à 17,5 %. Pour ce faire, un volume de 5,0757 g de la solution de peroxyde d'hydrogène a été placé dans un récipient sphérique en titane (8,7 ml).
Comme mentionné précédemment, le critère pour reconnaître une Réaction de décompositionUne réaction de décomposition est une réaction thermiquement induite d'un composé chimique formant des produits solides et/ou gazeux. réaction de décompositionExothermiqueUne transition d'échantillon ou une réaction est exothermique si elle produit de la chaleur.exothermique est un Taux d'auto-échauffementUn type particulier de calorimètre est utilisé pour détecter le taux d'auto-échauffement d'une substance. La méthode correspondante est appelée calorimétrie à taux d'accélération (ARC®). taux d'auto-échauffement de > 0,02 K/min. Cette valeur seuil a été dépassée à 90°C (début), puis la température de l'échantillon a augmenté jusqu'à 151°C dans des conditions adiabatiques. Au cours de la Réaction de décompositionUne réaction de décomposition est une réaction thermiquement induite d'un composé chimique formant des produits solides et/ou gazeux. réaction de décomposition, la pression à l'intérieur du récipient d'échantillonnage a augmenté jusqu'à 76,6 bars.
Existe-t-il un moyen d'arrêter l'emballement thermique ?
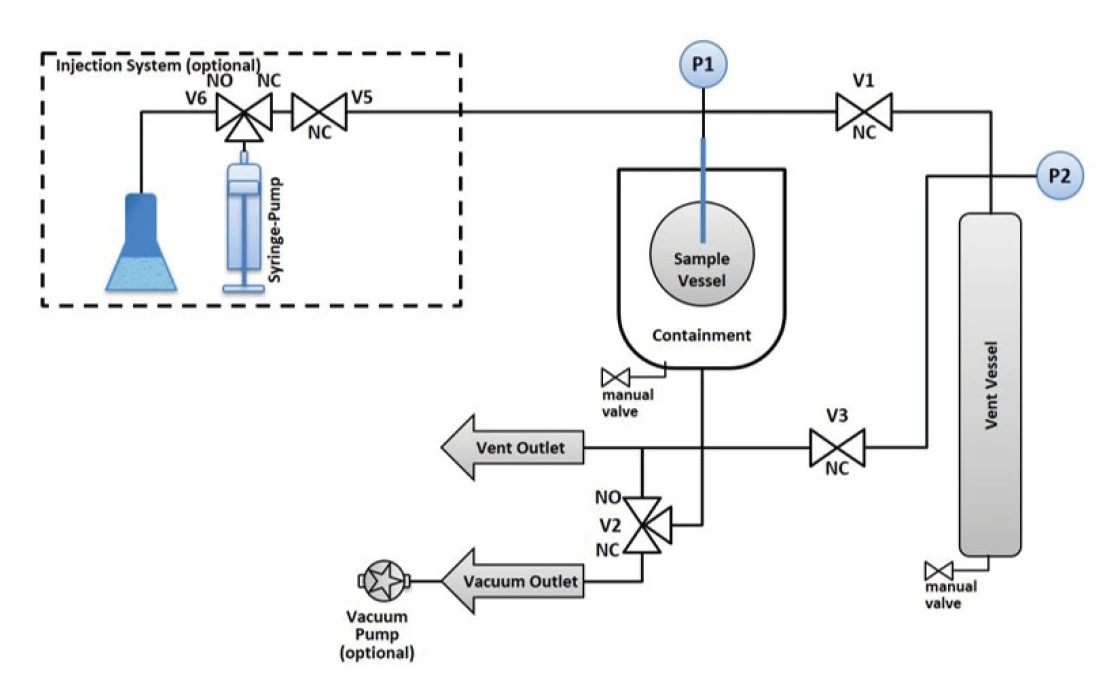
La question de savoir si l'Emballement thermiqueUn emballement thermique est la situation dans laquelle un réacteur chimique est hors de contrôle en ce qui concerne la production de température et/ou de pression causée par la réaction chimique elle-même. La simulation d'un emballement thermique est généralement réalisée à l'aide d'un calorimètre selon la méthode de la calorimétrie à taux accéléré (ARC®).emballement thermique peut être arrêté ou non est, bien sûr, fortement liée au Taux d'auto-échauffementUn type particulier de calorimètre est utilisé pour détecter le taux d'auto-échauffement d'une substance. La méthode correspondante est appelée calorimétrie à taux d'accélération (ARC®). taux d'auto-échauffement. Il est nécessaire de détecter la température critique ou le début de l'Emballement thermiqueUn emballement thermique est la situation dans laquelle un réacteur chimique est hors de contrôle en ce qui concerne la production de température et/ou de pression causée par la réaction chimique elle-même. La simulation d'un emballement thermique est généralement réalisée à l'aide d'un calorimètre selon la méthode de la calorimétrie à taux accéléré (ARC®).emballement thermique, mais il n'est peut-être pas toujours souhaitable de laisser la Réaction de décompositionUne réaction de décomposition est une réaction thermiquement induite d'un composé chimique formant des produits solides et/ou gazeux. réaction de décomposition suivre son cours. Il serait beaucoup plus important de connaître la température ou la pression jusqu'à laquelle une réaction qui a déjà commencé à s'emballer peut être arrêtée à nouveau et maîtrisée. La possibilité de détecter le début de l'Emballement thermiqueUn emballement thermique est la situation dans laquelle un réacteur chimique est hors de contrôle en ce qui concerne la production de température et/ou de pression causée par la réaction chimique elle-même. La simulation d'un emballement thermique est généralement réalisée à l'aide d'un calorimètre selon la méthode de la calorimétrie à taux accéléré (ARC®).emballement thermique d'une réaction et d'empêcher la poursuite de l'auto-échauffement en fermant l'environnement AdiabatiqueAdiabatique décrit un système ou un mode de mesure sans aucun échange de chaleur avec l'environnement. Ce mode peut être réalisé à l'aide d'un calorimètre selon la méthode de la calorimétrie à taux accéléré (ARC®). L'objectif principal d'un tel dispositif est d'étudier des scénarios et des réactions d'emballement thermique. Une brève description du mode adiabatique est la suivante : "pas d'entrée de chaleur - pas de sortie de chaleur".adiabatique, évitant ainsi la Réaction de décompositionUne réaction de décomposition est une réaction thermiquement induite d'un composé chimique formant des produits solides et/ou gazeux. réaction de décomposition, a déjà été évoquée ailleurs [2]. Il s'agit ici de montrer une autre façon d'arrêter une réaction de Réaction de décompositionUne réaction de décomposition est une réaction thermiquement induite d'un composé chimique formant des produits solides et/ou gazeux. décomposition qui vient de commencer en adoptant une stratégie différente. La cuve de réaction est reliée par une conduite de pression et une vanne à une autre cuve, dite cuve d'évent (figure 3). Lorsqu'une pression d'échantillonnage librement sélectionnable est atteinte, le logiciel de mesure ouvre la vanne du récipient de mise à l'air libre. En évacuant l'air dans ce récipient, la pression dans la cuve de réaction devrait également diminuer. Cela pourrait être suffisant pour arrêter l'auto-échauffement et donc les réactions consécutives et secondaires incontrôlées.
Mise à l'air libre
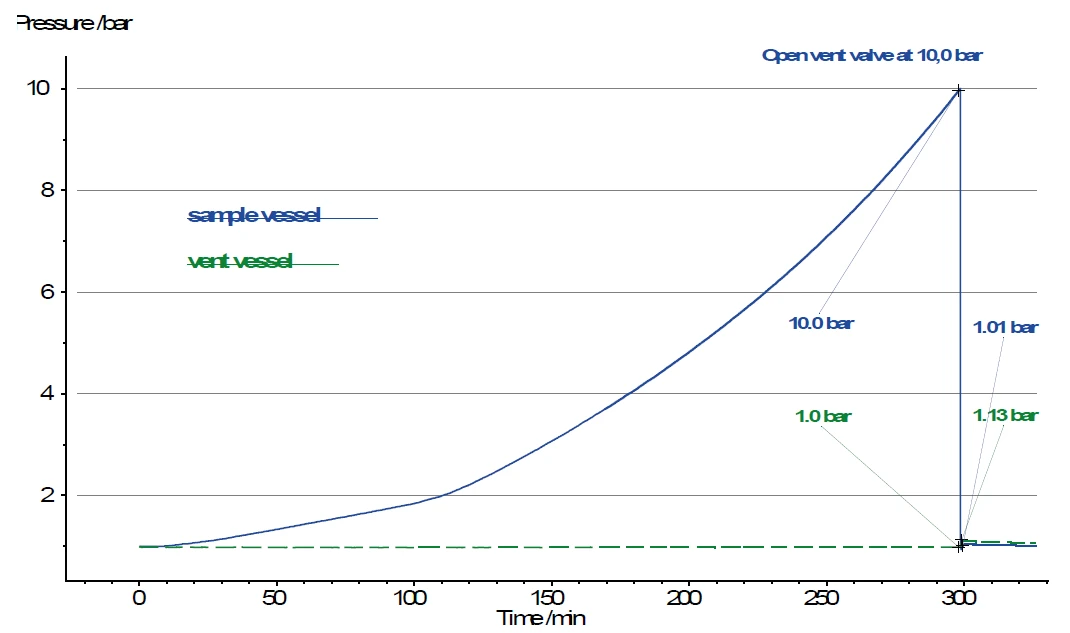
L'enceinte de réaction et l'enceinte de mise à l'air libre sont toutes deux équipées d'un manomètre individuel. Ainsi, l'augmentation de la pression peut être suivie après l'ouverture de la vanne (voir V1 dans la figure 3). Le volume du récipient de mise à l'air libre (250 ml) est toutefois plusieurs fois supérieur au volume du récipient d'échantillonnage, dans lequel il reste généralement environ 5 ml de gaz au-dessus de l'échantillon. C'est pourquoi la pression dans le récipient de mise à l'air libre n'augmente que de 1,0 bar à 1,13 bar après l'ouverture de la soupape, alors que la pression dans le récipient d'échantillonnage diminue de 10,0 bar à 1,0 bar au même moment (figure 4).
La figure 5 montre les résultats d'une mesure Heat-Wait-Search (HWS)Heat-Wait-Search est un mode de mesure utilisé dans les appareils calorimétriques selon la calorimétrie à taux accéléré (ARC®).HWS avec de l'eau comme substance échantillon, dans laquelle le signal de pression augmente de manière analogue au signal de température et en fonction des étapes de température du programme Heat-Wait-Search (HWS)Heat-Wait-Search est un mode de mesure utilisé dans les appareils calorimétriques selon la calorimétrie à taux accéléré (ARC®).HWS. Dans cet exemple, l'ouverture de la vanne d'aération a été programmée par le logiciel de mesure à 2,0 bar. Il est facile de constater qu'en ouvrant le récipient de mise à l'air libre, non seulement la pression dans le récipient d'échantillonnage diminue de 2,0 bar à 1,0 bar, mais la température dans le récipient d'échantillonnage diminue également fortement. Au cours d'une période de 60 minutes pendant laquelle le robinet d'aération reste ouvert, les éléments chauffants entourant le calorimètre suivent également la température de l'échantillon. Celle-ci passe de 108,4°C à 96,8°C et - bien que le mode de mesure AdiabatiqueAdiabatique décrit un système ou un mode de mesure sans aucun échange de chaleur avec l'environnement. Ce mode peut être réalisé à l'aide d'un calorimètre selon la méthode de la calorimétrie à taux accéléré (ARC®). L'objectif principal d'un tel dispositif est d'étudier des scénarios et des réactions d'emballement thermique. Une brève description du mode adiabatique est la suivante : "pas d'entrée de chaleur - pas de sortie de chaleur".adiabatique reste activé pendant cette période, c'est-à-dire que les éléments chauffants environnants suivent la température de l'échantillon - aucune autre augmentation de la température de l'échantillon ne peut être déterminée.
Lorsqu'on étudie l'eau comme substance échantillon, on peut s'attendre à ce qu'il n'y ait pas de réaction ExothermiqueUne transition d'échantillon ou une réaction est exothermique si elle produit de la chaleur.exothermique. Au contraire, il a été confirmé que lorsqu'il n'y a pas de réaction ExothermiqueUne transition d'échantillon ou une réaction est exothermique si elle produit de la chaleur.exothermique de l'échantillon, la température de l'échantillon diminue après l'ouverture de la soupape d'aération et reste ensuite constante en raison de l'environnement AdiabatiqueAdiabatique décrit un système ou un mode de mesure sans aucun échange de chaleur avec l'environnement. Ce mode peut être réalisé à l'aide d'un calorimètre selon la méthode de la calorimétrie à taux accéléré (ARC®). L'objectif principal d'un tel dispositif est d'étudier des scénarios et des réactions d'emballement thermique. Une brève description du mode adiabatique est la suivante : "pas d'entrée de chaleur - pas de sortie de chaleur".adiabatique. Ceci est également confirmé par le Taux d'auto-échauffementUn type particulier de calorimètre est utilisé pour détecter le taux d'auto-échauffement d'une substance. La méthode correspondante est appelée calorimétrie à taux d'accélération (ARC®). taux d'auto-échauffement de l'échantillon dans la partie inférieure de la figure.
L'étude d'une solution de peroxyde d'hydrogène à un pour cent ne montre pas non plus d'augmentation de la température après l'ouverture du robinet de mise à l'air libre à une pression de 3 bars dans le récipient d'échantillonnage. Dans le cas d'une solution de peroxyde d'hydrogène à deux pour cent, on peut déjà constater que la réaction de Réaction de décompositionUne réaction de décomposition est une réaction thermiquement induite d'un composé chimique formant des produits solides et/ou gazeux. décompositionExothermiqueUne transition d'échantillon ou une réaction est exothermique si elle produit de la chaleur.exothermique provoquée par l'ouverture de la soupape de mise à l'air libre et la dépressurisation du système à la pression atmosphérique n'est pas suffisante pour supprimer entièrement la Réaction de décompositionUne réaction de décomposition est une réaction thermiquement induite d'un composé chimique formant des produits solides et/ou gazeux. décomposition ultérieure. Il en résulte un Taux d'auto-échauffementUn type particulier de calorimètre est utilisé pour détecter le taux d'auto-échauffement d'une substance. La méthode correspondante est appelée calorimétrie à taux d'accélération (ARC®). taux d'auto-échauffement de 0,02 K/min. Pour une solution de peroxyde d'hydrogène à quatre pour cent (figure 6), un Taux d'auto-échauffementUn type particulier de calorimètre est utilisé pour détecter le taux d'auto-échauffement d'une substance. La méthode correspondante est appelée calorimétrie à taux d'accélération (ARC®). taux d'auto-échauffement de 0,04 K/min est encore détecté après l'ouverture de la soupape de mise à l'air libre. Les températures et les Taux d'auto-échauffementUn type particulier de calorimètre est utilisé pour détecter le taux d'auto-échauffement d'une substance. La méthode correspondante est appelée calorimétrie à taux d'accélération (ARC®). taux d'auto-échauffement des solutions de peroxyde d'hydrogène examinées sont résumés dans le tableau 1.
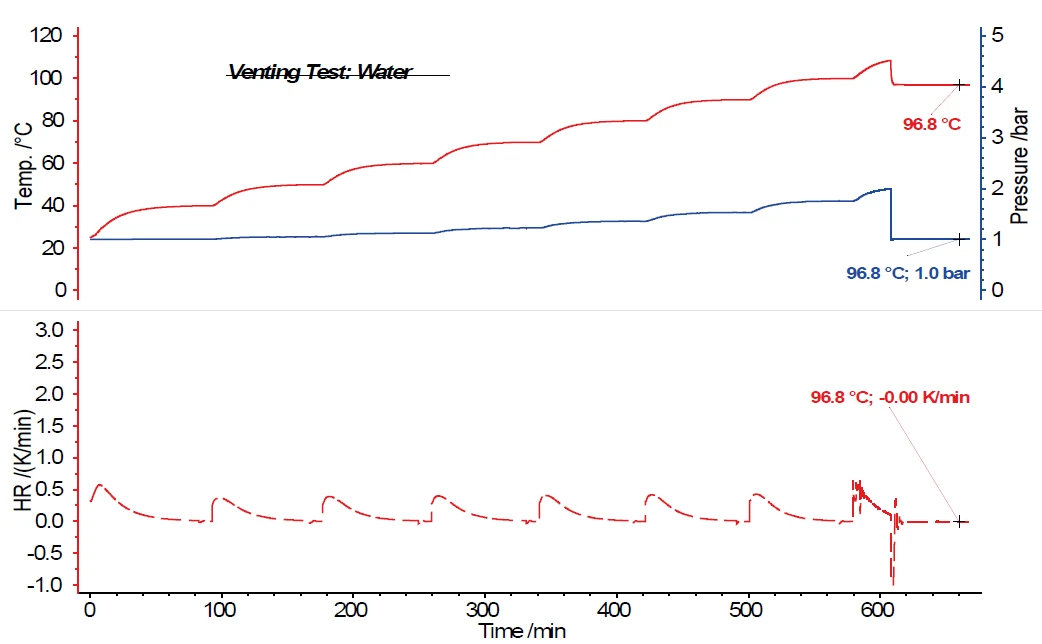
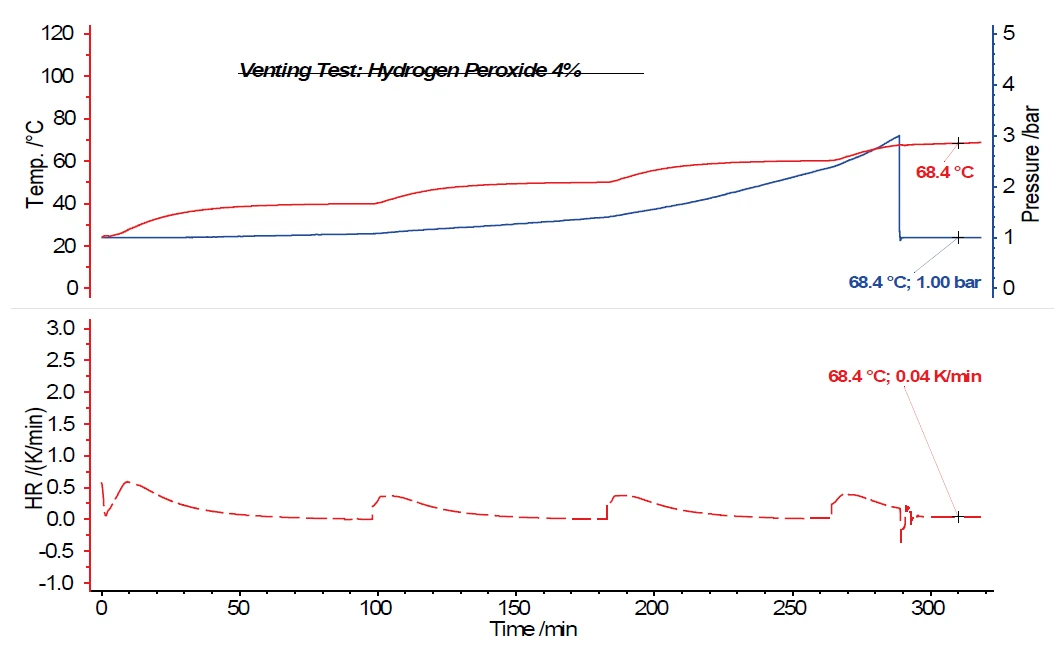
Tableau 1 : Résumé de la température et du Taux d'auto-échauffementUn type particulier de calorimètre est utilisé pour détecter le taux d'auto-échauffement d'une substance. La méthode correspondante est appelée calorimétrie à taux d'accélération (ARC®). taux d'auto-échauffement pour différentes solutions de peroxyde d'hydrogène
| Échantillon | Température pendant la mise à l'air libre | Taux d'auto-échauffementUn type particulier de calorimètre est utilisé pour détecter le taux d'auto-échauffement d'une substance. La méthode correspondante est appelée calorimétrie à taux d'accélération (ARC®). Taux d'auto-échauffement après la mise à l'air libre |
| H2O | 108.4°C (2 bar) | 0.00 K/min |
| H2O2 (1%) | 81.8°C (3 bar) | 0.00 K/min |
| H2O2 (2%) | 70.8°C (3 bar) | 0.02 K/min |
| H2O2 (4%) | 67.6°C (3 bar) | 0.04 K/min |
Résumé
Le site NETZSCH ARC® 254 offre deux possibilités pour reprendre le contrôle, si nécessaire, des réactions où l'Emballement thermiqueUn emballement thermique est la situation dans laquelle un réacteur chimique est hors de contrôle en ce qui concerne la production de température et/ou de pression causée par la réaction chimique elle-même. La simulation d'un emballement thermique est généralement réalisée à l'aide d'un calorimètre selon la méthode de la calorimétrie à taux accéléré (ARC®).emballement thermique a déjà commencé. La première possibilité consiste à éteindre les éléments chauffants environnants lorsque l'échantillon atteint un Taux d'auto-échauffementUn type particulier de calorimètre est utilisé pour détecter le taux d'auto-échauffement d'une substance. La méthode correspondante est appelée calorimétrie à taux d'accélération (ARC®). taux d'auto-échauffement donné, ce qui élimine l'environnement AdiabatiqueAdiabatique décrit un système ou un mode de mesure sans aucun échange de chaleur avec l'environnement. Ce mode peut être réalisé à l'aide d'un calorimètre selon la méthode de la calorimétrie à taux accéléré (ARC®). L'objectif principal d'un tel dispositif est d'étudier des scénarios et des réactions d'emballement thermique. Une brève description du mode adiabatique est la suivante : "pas d'entrée de chaleur - pas de sortie de chaleur".adiabatique de l'échantillon et permet à nouveau les pertes de chaleur ; l'emballement de la réaction est alors empêché par ces pertes de chaleur [2]. L'autre possibilité, dans laquelle la pression peut être évacuée du récipient d'échantillonnage vers un autre récipient d'échantillonnage (récipient d'évent) en ouvrant une soupape de décharge (soupape d'évent), a été présentée dans cette note d'application. En mesurant la pression indépendamment, il est possible de surveiller l'augmentation de la pression dans le récipient de mise à l'air libre. Il a été démontré que la progression des Réaction de décompositionUne réaction de décomposition est une réaction thermiquement induite d'un composé chimique formant des produits solides et/ou gazeux. réactions de décomposition faiblement exothermiques peut être stoppée par cette mesure, tandis que les réactions plus fortement exothermiques continuent à montrer un auto-échauffement détectable même après que la pression a été relâchée.